よむ、つかう、まなぶ。
04資料1-2サノフィ株式会社提出資料 (20 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_52445.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第29回 2/20)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
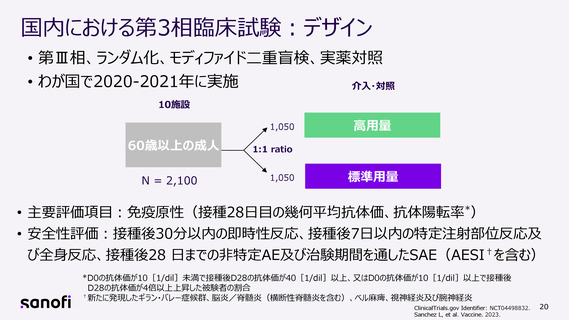
国内における第3相臨床試験:デザイン
• 第Ⅲ相、ランダム化、モディファイド二重盲検、実薬対照
• わが国で2020-2021年に実施
介入・対照
10施設
1,050
60歳以上の成人
N = 2,100
高用量
1:1 ratio
1,050
標準用量
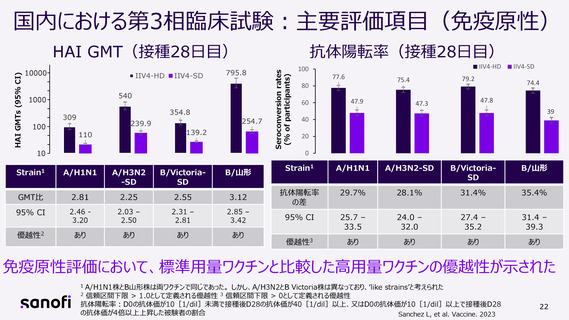
• 主要評価項目:免疫原性(接種28日目の幾何平均抗体価、抗体陽転率*)
• 安全性評価:接種後30分以内の即時性反応、接種後7日以内の特定注射部位反応及
び全身反応、接種後28 日までの非特定AE及び治験期間を通したSAE(AESI†を含む)
*D0の抗体価が10[1/dil]未満で接種後D28の抗体価が40[1/dil]以上、又はD0の抗体価が10[1/dil]以上で接種後
D28の抗体価が4倍以上上昇した被験者の割合
†新たに発現したギラン・バレー症候群、脳炎/脊髄炎(横断性脊髄炎を含む)、ベル麻痺、視神経炎及び腕神経炎
ClinicalTrials.gov Identifier: NCT04498832.
Sanchez L, et al. Vaccine. 2023.
20
• 第Ⅲ相、ランダム化、モディファイド二重盲検、実薬対照
• わが国で2020-2021年に実施
介入・対照
10施設
1,050
60歳以上の成人
N = 2,100
高用量
1:1 ratio
1,050
標準用量
• 主要評価項目:免疫原性(接種28日目の幾何平均抗体価、抗体陽転率*)
• 安全性評価:接種後30分以内の即時性反応、接種後7日以内の特定注射部位反応及
び全身反応、接種後28 日までの非特定AE及び治験期間を通したSAE(AESI†を含む)
*D0の抗体価が10[1/dil]未満で接種後D28の抗体価が40[1/dil]以上、又はD0の抗体価が10[1/dil]以上で接種後
D28の抗体価が4倍以上上昇した被験者の割合
†新たに発現したギラン・バレー症候群、脳炎/脊髄炎(横断性脊髄炎を含む)、ベル麻痺、視神経炎及び腕神経炎
ClinicalTrials.gov Identifier: NCT04498832.
Sanchez L, et al. Vaccine. 2023.
20