よむ、つかう、まなぶ。
資料2-1 医薬品等の使用上の注意の改訂について [289KB] (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
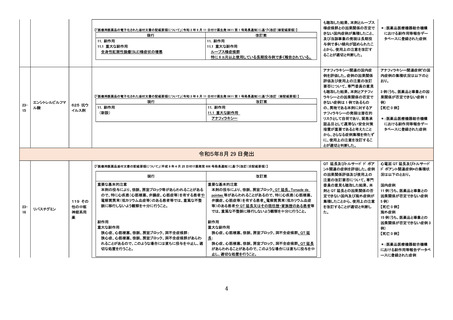
【「医療用医薬品の電子化された添付文書の記載要領について」(令和 3 年 6 月 11 日付け薬生発 0611 第 1 号局長通知)に基づく改訂(新記載要領)】
現行
改訂案
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
心筋梗塞、弁膜症、心筋症等の心疾患や電解質異常(低カリウ
ム血症等)等のある患者
徐脈、房室ブロック等が起こるおそれがあるため、重篤な不整脈
に移行しないよう観察を十分に行うこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
心筋梗塞、弁膜症、心筋症等の心疾患、電解質異常(低カリウム
血症等)等のある患者、QT 延長又はその既往歴・家族歴のある
患者
徐脈、房室ブロック、QT 延長、Torsade de pointes 等が起こるお
それがあるため、重篤な不整脈に移行しないよう観察を十分に
行うこと。
11. 副作用
11.1 重大な副作用
狭心症、心筋梗塞、徐脈、房室ブロック、洞不全症候群
11. 副作用
11.1 重大な副作用
狭心症、心筋梗塞、徐脈、房室ブロック、洞不全症候群、QT 延長
【「医療用医薬品添付文書の記載要領について」(平成 9 年 4 月 25 日付け薬発第 606 号局長通知)に基づく改訂(旧記載要領)】
現行
慎重投与
(新設)
2317
フィナステリド
249 その
他のホル
モン剤
重要な基本的注意
(新設)
改訂案
慎重投与
うつ病、うつ状態又はその既往歴、自殺念慮又は自殺企図の既
往歴を有する患者〔本剤との因果関係は明らかではないが、自
殺念慮、自殺企図、自殺既遂が報告されている。〕
重要な基本的注意
本剤との因果関係は明らかではないが、自殺念慮、自殺企図、
自殺既遂が報告されている。患者の状態を十分に観察するとと
もに、自殺念慮又は自殺企図があらわれた場合には本剤の服用
を中止し、速やかに医師等に連絡するよう患者に指導すること。
(注)患者向医薬品ガイドを作成する医薬品に特定する。
5
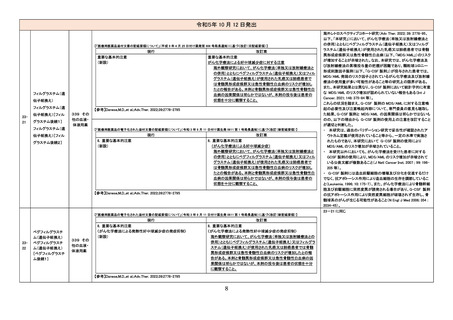
自殺関連事象について、国内症
例、WHO 個別症例安全性報告
グローバルデータベース
(VigiBase)*を用いた不均衡分析
結果等を評価した。
専門委員の意見も聴取した結
果、以下の内容を踏まえ、使用
上の注意を改訂することが適切
と判断した。
・ 国内副作用症例において、フ
ィナステリドと自殺関連事象と
の因果関係が否定できない症
例は認められていないもの
の、機構で実施した VigiBase
の 2023 年 5 月 28 日時点の
データセットを用いた不均衡分
析における IC025†が、希死念
慮を有するうつ病:3.5、自殺念
慮:3.3、自殺既遂:1.6、自殺行
為:1.3、自傷念慮:0.5、自殺企
図:0.4 を示し、これらの事象
に関する副作用報告数がデー
タベース全体から予測される
値より統計学的に有意に高か
自殺関連症例§の国内症例の
集積状況は以下のとおり。
7 例(うち、医薬品と事象との因
果関係が否定できない症例 0
例)
【死亡 1 例(うち、医薬品と事象
による死亡との因果関係が否
定できない症例 0 例)】
§:医薬品医療機器総合機構
における副作用等報告デー
タベースに登録された症例
現行
改訂案
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
心筋梗塞、弁膜症、心筋症等の心疾患や電解質異常(低カリウ
ム血症等)等のある患者
徐脈、房室ブロック等が起こるおそれがあるため、重篤な不整脈
に移行しないよう観察を十分に行うこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
心筋梗塞、弁膜症、心筋症等の心疾患、電解質異常(低カリウム
血症等)等のある患者、QT 延長又はその既往歴・家族歴のある
患者
徐脈、房室ブロック、QT 延長、Torsade de pointes 等が起こるお
それがあるため、重篤な不整脈に移行しないよう観察を十分に
行うこと。
11. 副作用
11.1 重大な副作用
狭心症、心筋梗塞、徐脈、房室ブロック、洞不全症候群
11. 副作用
11.1 重大な副作用
狭心症、心筋梗塞、徐脈、房室ブロック、洞不全症候群、QT 延長
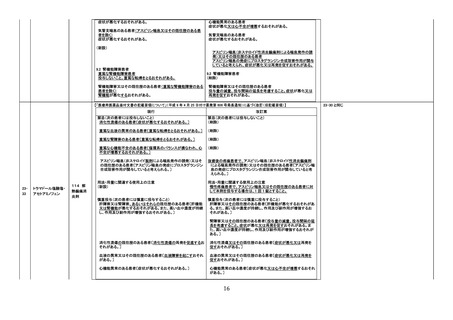
【「医療用医薬品添付文書の記載要領について」(平成 9 年 4 月 25 日付け薬発第 606 号局長通知)に基づく改訂(旧記載要領)】
現行
慎重投与
(新設)
2317
フィナステリド
249 その
他のホル
モン剤
重要な基本的注意
(新設)
改訂案
慎重投与
うつ病、うつ状態又はその既往歴、自殺念慮又は自殺企図の既
往歴を有する患者〔本剤との因果関係は明らかではないが、自
殺念慮、自殺企図、自殺既遂が報告されている。〕
重要な基本的注意
本剤との因果関係は明らかではないが、自殺念慮、自殺企図、
自殺既遂が報告されている。患者の状態を十分に観察するとと
もに、自殺念慮又は自殺企図があらわれた場合には本剤の服用
を中止し、速やかに医師等に連絡するよう患者に指導すること。
(注)患者向医薬品ガイドを作成する医薬品に特定する。
5
自殺関連事象について、国内症
例、WHO 個別症例安全性報告
グローバルデータベース
(VigiBase)*を用いた不均衡分析
結果等を評価した。
専門委員の意見も聴取した結
果、以下の内容を踏まえ、使用
上の注意を改訂することが適切
と判断した。
・ 国内副作用症例において、フ
ィナステリドと自殺関連事象と
の因果関係が否定できない症
例は認められていないもの
の、機構で実施した VigiBase
の 2023 年 5 月 28 日時点の
データセットを用いた不均衡分
析における IC025†が、希死念
慮を有するうつ病:3.5、自殺念
慮:3.3、自殺既遂:1.6、自殺行
為:1.3、自傷念慮:0.5、自殺企
図:0.4 を示し、これらの事象
に関する副作用報告数がデー
タベース全体から予測される
値より統計学的に有意に高か
自殺関連症例§の国内症例の
集積状況は以下のとおり。
7 例(うち、医薬品と事象との因
果関係が否定できない症例 0
例)
【死亡 1 例(うち、医薬品と事象
による死亡との因果関係が否
定できない症例 0 例)】
§:医薬品医療機器総合機構
における副作用等報告デー
タベースに登録された症例