よむ、つかう、まなぶ。
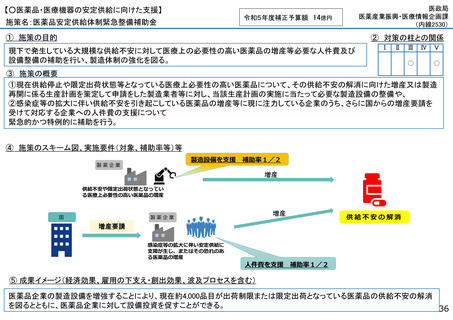
【資料2】医薬品の安定供給確保の現状と課題 (30 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36723.html |
| 出典情報 | 医療用医薬品の安定確保策に関する関係者会議(第9回 12/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
日本薬局方について
「日本薬局方」は、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第41条第1項の規定に基づ
き、承認されている医薬品の性状及び品質の適正を図るため、厚生労働大臣が薬事・食品衛生審議会の意見を聴いて定
める規格基準書
具体的な活用事例
• 公定書として日本国内の医薬品製造にかかる規格基準や試験の根拠として使用される。
• 医薬品の開発及び承認審査にかかる時間やコストの縮減に活用される。
• 有害物質が混入された医薬品の国内流通を阻止する品質基準を設定することにより、公衆衛生の確保に資する。
•
(ヘパリンへの過硫酸化コンドロイチン硫酸混入、グリセリンへのエチレングリコールやジエチレングリコールの混入)
国際基準(ICH Q3C(残留溶媒)、Q3D(元素不純物)等)の国内規制への取り込み。
広く汎用される試験として日本薬局方に規定することによって国内の医薬品の品質を底上げし、国際的な医薬品の品質の信頼性を確
保することができる。
○日本薬局方の規格等が海外薬局方と異なることにより、医薬品の安定供給に影響した事例が報告されている。
• 日本薬局方で定められた赤外吸収スペクトルによる確認試験の規定が、欧州薬局方や米国薬局方と異なるため、そ
れらに適合した海外原薬が使用できず製品の供給に影響があった。
• 国内の日本薬局方適合原薬の製造中止に伴い、海外原薬の使用を検討したところ、日本薬局方で定められているpH
の規格が米国薬局方では定められていないため、日本薬局方適合品の入手ができず、製品の供給が滞った。
○海外薬局方適合品を輸入したところ、日本薬局方の規格に適合しなかった事例が報告されている。
→
⑴中長期的な対応
現在進められている、薬局方調和国際会議(PDG)等を通じた海外薬局方との国際調和の取組をより一層推進し
ていく(別紙参照)。
⑵短期的な対応
安定供給に係る支障の状況(製品の流通状況及び今後の見込み)、市場に与える影響の程度等、個別の品目の状
況に応じた対応を実施(「医療用医薬品の供給不足に伴う審査及び調査の迅速処理について」令和5年10月16日
付け通知)。
30
「日本薬局方」は、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第41条第1項の規定に基づ
き、承認されている医薬品の性状及び品質の適正を図るため、厚生労働大臣が薬事・食品衛生審議会の意見を聴いて定
める規格基準書
具体的な活用事例
• 公定書として日本国内の医薬品製造にかかる規格基準や試験の根拠として使用される。
• 医薬品の開発及び承認審査にかかる時間やコストの縮減に活用される。
• 有害物質が混入された医薬品の国内流通を阻止する品質基準を設定することにより、公衆衛生の確保に資する。
•
(ヘパリンへの過硫酸化コンドロイチン硫酸混入、グリセリンへのエチレングリコールやジエチレングリコールの混入)
国際基準(ICH Q3C(残留溶媒)、Q3D(元素不純物)等)の国内規制への取り込み。
広く汎用される試験として日本薬局方に規定することによって国内の医薬品の品質を底上げし、国際的な医薬品の品質の信頼性を確
保することができる。
○日本薬局方の規格等が海外薬局方と異なることにより、医薬品の安定供給に影響した事例が報告されている。
• 日本薬局方で定められた赤外吸収スペクトルによる確認試験の規定が、欧州薬局方や米国薬局方と異なるため、そ
れらに適合した海外原薬が使用できず製品の供給に影響があった。
• 国内の日本薬局方適合原薬の製造中止に伴い、海外原薬の使用を検討したところ、日本薬局方で定められているpH
の規格が米国薬局方では定められていないため、日本薬局方適合品の入手ができず、製品の供給が滞った。
○海外薬局方適合品を輸入したところ、日本薬局方の規格に適合しなかった事例が報告されている。
→
⑴中長期的な対応
現在進められている、薬局方調和国際会議(PDG)等を通じた海外薬局方との国際調和の取組をより一層推進し
ていく(別紙参照)。
⑵短期的な対応
安定供給に係る支障の状況(製品の流通状況及び今後の見込み)、市場に与える影響の程度等、個別の品目の状
況に応じた対応を実施(「医療用医薬品の供給不足に伴う審査及び調査の迅速処理について」令和5年10月16日
付け通知)。
30