よむ、つかう、まなぶ。
資料No.1_第十八改正日本薬局方第二追補(案)について (30 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000174942_00008.html |
| 出典情報 | 薬事・食品衛生審議会 日本薬局方部会(令和5年度第1回 1/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別添2
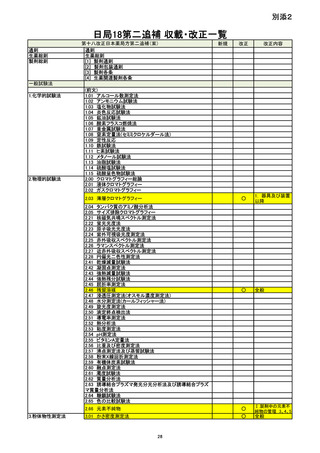
第十八改正日本薬局方第二追補(案)
3.02 比表面積測定法
3.03 粉体の粒子密度測定法
3.04 粒度測定法
3.05 収着-脱着等温線測定法及び水分活性測定法
3.06 レーザー回折・散乱法による粒子径測定法
3.07 動的光散乱法による液体中の粒子径測定法
4.生物学的試験法/生化 4.01 エンドトキシン試験法
学的試験法/微生物学的
4.02 抗生物質の微生物学的力価試験法
試験法
5.生薬試験法
新規
改正
○
改正内容
新規
○
1.10 操作法、2.1 穿
孔カンテン平板の調
整、2.2 操作法
○
3. 鏡検
9.01 標準品
○
新規(1):13、
削除(1) :2、(2) :1
(2)→(1)へ移行:6
9.21 容量分析用標準液
9.22 標準液
9.23 色の比較液
9.41 試薬・試液
9.42 クロマトグラフィー用担体/充塡剤
9.43 ろ紙,ろ過フィルター,試験紙,るつぼ等
9.44 標準粒子等
9.61 波長及び透過率校正用光学フィルター
○
○
別紙5
新規:2
9.62 計量器・用器
○
はかり(天秤)及び
分銅
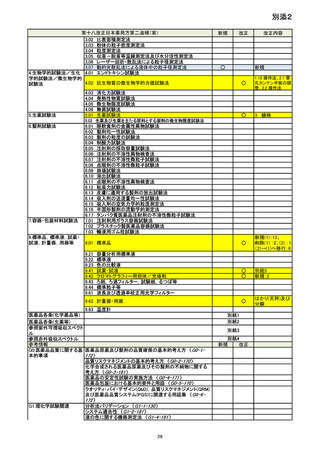
4.03 消化力試験法
4.04 発熱性物質試験法
4.05 微生物限度試験法
4.06 無菌試験法
5.01 生薬試験法
5.02 生薬及び生薬を主たる原料とする製剤の微生物限度試験法
6.製剤試験法
7.容器・包装材料試験法
9.標準品,標準液,試薬・
試液,計量器,用器等
6.01 眼軟膏剤の金属性異物試験法
6.02 製剤均一性試験法
6.03 製剤の粒度の試験法
6.04 制酸力試験法
6.05 注射剤の採取容量試験法
6.06 注射剤の不溶性異物検査法
6.07 注射剤の不溶性微粒子試験法
6.08 点眼剤の不溶性微粒子試験法
6.09 崩壊試験法
6.10 溶出試験法
6.11 点眼剤の不溶性異物検査法
6.12 粘着力試験法
6.13 皮膚に適用する製剤の放出試験法
6.14 吸入剤の送達量均一性試験法
6.15 吸入剤の空気力学的粒度測定法
6.16 半固形製剤の流動学的測定法
6.17 タンパク質医薬品注射剤の不溶性微粒子試験法
7.01 注射剤用ガラス容器試験法
7.02 プラスチック製医薬品容器試験法
7.03 輸液用ゴム栓試験法
9.63 温度計
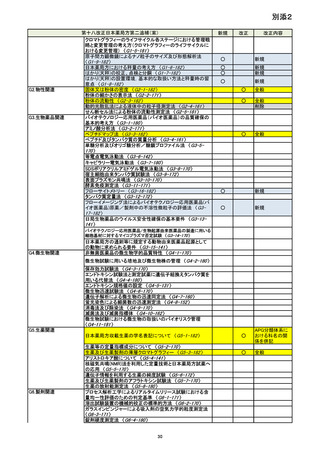
医薬品各条(化学薬品等)
医薬品各条(生薬等)
参照紫外可視吸収スペクト
ル
参照赤外吸収スペクトル
参考情報
G0.医薬品品質に関する基 医薬品原薬及び製剤の品質確保の基本的考え方 〈G0-1本的事項
172 〉
品質リスクマネジメントの基本的考え方 〈G0-2-170 〉
化学合成される医薬品原薬及びその製剤の不純物に関する
考え方 〈G0-3-181 〉
医薬品の安定性試験の実施方法 〈G0-4-171 〉
医薬品包装における基本的要件と用語 〈G0-5-170 〉
クオリティ・バイ・デザイン(QbD),品質リスクマネジメント(QRM)
及び医薬品品質システム(PQS)に関連する用語集 〈G0-6172 〉
G1.理化学試験関連
分析法バリデーション 〈G1-1-130 〉
システム適合性 〈G1-2-181 〉
液の色に関する機器測定法 〈G1-4-181 〉
29
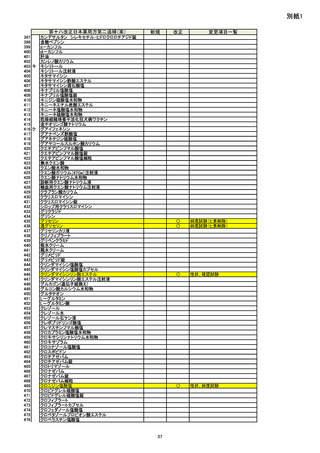
別紙1
別紙2
別紙3
別紙4
新規
改正
第十八改正日本薬局方第二追補(案)
3.02 比表面積測定法
3.03 粉体の粒子密度測定法
3.04 粒度測定法
3.05 収着-脱着等温線測定法及び水分活性測定法
3.06 レーザー回折・散乱法による粒子径測定法
3.07 動的光散乱法による液体中の粒子径測定法
4.生物学的試験法/生化 4.01 エンドトキシン試験法
学的試験法/微生物学的
4.02 抗生物質の微生物学的力価試験法
試験法
5.生薬試験法
新規
改正
○
改正内容
新規
○
1.10 操作法、2.1 穿
孔カンテン平板の調
整、2.2 操作法
○
3. 鏡検
9.01 標準品
○
新規(1):13、
削除(1) :2、(2) :1
(2)→(1)へ移行:6
9.21 容量分析用標準液
9.22 標準液
9.23 色の比較液
9.41 試薬・試液
9.42 クロマトグラフィー用担体/充塡剤
9.43 ろ紙,ろ過フィルター,試験紙,るつぼ等
9.44 標準粒子等
9.61 波長及び透過率校正用光学フィルター
○
○
別紙5
新規:2
9.62 計量器・用器
○
はかり(天秤)及び
分銅
4.03 消化力試験法
4.04 発熱性物質試験法
4.05 微生物限度試験法
4.06 無菌試験法
5.01 生薬試験法
5.02 生薬及び生薬を主たる原料とする製剤の微生物限度試験法
6.製剤試験法
7.容器・包装材料試験法
9.標準品,標準液,試薬・
試液,計量器,用器等
6.01 眼軟膏剤の金属性異物試験法
6.02 製剤均一性試験法
6.03 製剤の粒度の試験法
6.04 制酸力試験法
6.05 注射剤の採取容量試験法
6.06 注射剤の不溶性異物検査法
6.07 注射剤の不溶性微粒子試験法
6.08 点眼剤の不溶性微粒子試験法
6.09 崩壊試験法
6.10 溶出試験法
6.11 点眼剤の不溶性異物検査法
6.12 粘着力試験法
6.13 皮膚に適用する製剤の放出試験法
6.14 吸入剤の送達量均一性試験法
6.15 吸入剤の空気力学的粒度測定法
6.16 半固形製剤の流動学的測定法
6.17 タンパク質医薬品注射剤の不溶性微粒子試験法
7.01 注射剤用ガラス容器試験法
7.02 プラスチック製医薬品容器試験法
7.03 輸液用ゴム栓試験法
9.63 温度計
医薬品各条(化学薬品等)
医薬品各条(生薬等)
参照紫外可視吸収スペクト
ル
参照赤外吸収スペクトル
参考情報
G0.医薬品品質に関する基 医薬品原薬及び製剤の品質確保の基本的考え方 〈G0-1本的事項
172 〉
品質リスクマネジメントの基本的考え方 〈G0-2-170 〉
化学合成される医薬品原薬及びその製剤の不純物に関する
考え方 〈G0-3-181 〉
医薬品の安定性試験の実施方法 〈G0-4-171 〉
医薬品包装における基本的要件と用語 〈G0-5-170 〉
クオリティ・バイ・デザイン(QbD),品質リスクマネジメント(QRM)
及び医薬品品質システム(PQS)に関連する用語集 〈G0-6172 〉
G1.理化学試験関連
分析法バリデーション 〈G1-1-130 〉
システム適合性 〈G1-2-181 〉
液の色に関する機器測定法 〈G1-4-181 〉
29
別紙1
別紙2
別紙3
別紙4
新規
改正