よむ、つかう、まなぶ。
資料1 これまでの議論で出された主な意見.pdf (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43571.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和6年度第6回 9/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
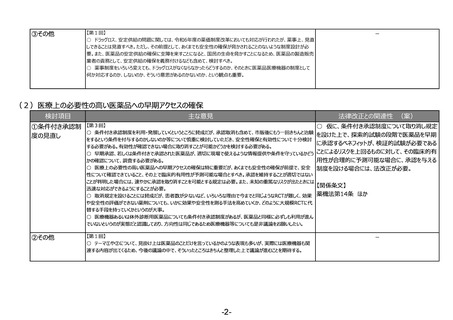
③その他
【第1回】
○ ドラッグロス、安定供給の問題に関しては、令和6年度の薬価制度改革においても対応が行われたが、薬事上、見直
しできることは見直すべき。ただし、その前提として、あくまでも安全性の確保が脅かされることのないような制度設計が必
要。また、医薬品の安定供給の確保に支障を来すことになると、国民の生命を脅かすことになるため、医薬品の製造販売
業者の責務として、安定供給の確保を義務付けるなども含めて、検討すべき。
○ 薬事制度をいろいろ変えても、ドラッグロスがなくならなかったらどうするのか、そのときに医薬品医療機器の制度として
何か対応するのか、しないのか、そういう意思があるのかないのか、という観点も重要。
-
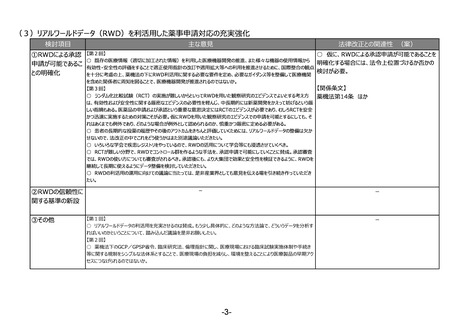
(2)医療上の必要性の高い医薬品への早期アクセスの確保
検討項目
主な意見
法律改正との関連性 (案)
①条件付き承認制
度の見直し
【第3回】
○ 仮に、条件付き承認制度について取り消し規定
○ 条件付き承認制度を利用・発展していくというところに賛成だが、承認取消も含めて、市販後にもう一回きちんと治験
を設けた上で、探索的試験の段階で医薬品を早期
をするという条件を付与するのかしないのか等について慎重に検討していただき、安全性確保と有効性について十分検討
に承認するベネフィットが、検証的試験が必要である
する必要がある。有効性が確認できない場合に取り消すことが可能かどうかを検討する必要がある。
○ 早期承認、若しくは条件付きで承認された医薬品が、適切に現場で使えるような情報提供や条件を守っているかどう ことによるリスクを上回るものに対して、その臨床的有
用性が合理的に予測可能な場合に、承認を与える
かの確認について、調査する必要がある。
○ 医療上の必要性の高い医薬品への早期アクセスの確保は特に重要だが、あくまでも安全性の確保が前提で、安全 制度を設ける場合には、法改正が必要。
性について確認できていること、その上で臨床的有用性が予測可能な場合とすべき。承認を維持することが適切ではない
ことが判明した場合には、速やかに承認を取り消すことを可能とする規定は必要。また、未知の重篤なリスクが出たときには
【関係条文】
迅速な対応ができるようにすることが必要。
○ 取消規定を設けることには賛成だが、患者数が少ないなど、いろいろな理由で今までと同じようなRCTが難しく、効果 薬機法第14条 ほか
や安全性の評価ができない薬剤についても、いかに効果や安全性を測る手法を高めていくか、どのように大規模RCTに代
替する手段を持っていくかというのが大事。
○ 医療機器あるいは体外診断用医薬品についても条件付き承認制度があるが、医薬品と同様に必ずしも利用が進ん
でいないというのが実態だと認識しており、方向性は同じであるため医療機器等についても是非議論をお願いしたい。
②その他
【第1回】
○ テーマ①や②について、見掛け上は医薬品のことだけを言っているかのような表現も多いが、実際には医療機器も関
連する内容が出てくるため、今後の議論の中で、そういったところはきちんと整理した上で議論が進むことを期待する。
-2-
-
【第1回】
○ ドラッグロス、安定供給の問題に関しては、令和6年度の薬価制度改革においても対応が行われたが、薬事上、見直
しできることは見直すべき。ただし、その前提として、あくまでも安全性の確保が脅かされることのないような制度設計が必
要。また、医薬品の安定供給の確保に支障を来すことになると、国民の生命を脅かすことになるため、医薬品の製造販売
業者の責務として、安定供給の確保を義務付けるなども含めて、検討すべき。
○ 薬事制度をいろいろ変えても、ドラッグロスがなくならなかったらどうするのか、そのときに医薬品医療機器の制度として
何か対応するのか、しないのか、そういう意思があるのかないのか、という観点も重要。
-
(2)医療上の必要性の高い医薬品への早期アクセスの確保
検討項目
主な意見
法律改正との関連性 (案)
①条件付き承認制
度の見直し
【第3回】
○ 仮に、条件付き承認制度について取り消し規定
○ 条件付き承認制度を利用・発展していくというところに賛成だが、承認取消も含めて、市販後にもう一回きちんと治験
を設けた上で、探索的試験の段階で医薬品を早期
をするという条件を付与するのかしないのか等について慎重に検討していただき、安全性確保と有効性について十分検討
に承認するベネフィットが、検証的試験が必要である
する必要がある。有効性が確認できない場合に取り消すことが可能かどうかを検討する必要がある。
○ 早期承認、若しくは条件付きで承認された医薬品が、適切に現場で使えるような情報提供や条件を守っているかどう ことによるリスクを上回るものに対して、その臨床的有
用性が合理的に予測可能な場合に、承認を与える
かの確認について、調査する必要がある。
○ 医療上の必要性の高い医薬品への早期アクセスの確保は特に重要だが、あくまでも安全性の確保が前提で、安全 制度を設ける場合には、法改正が必要。
性について確認できていること、その上で臨床的有用性が予測可能な場合とすべき。承認を維持することが適切ではない
ことが判明した場合には、速やかに承認を取り消すことを可能とする規定は必要。また、未知の重篤なリスクが出たときには
【関係条文】
迅速な対応ができるようにすることが必要。
○ 取消規定を設けることには賛成だが、患者数が少ないなど、いろいろな理由で今までと同じようなRCTが難しく、効果 薬機法第14条 ほか
や安全性の評価ができない薬剤についても、いかに効果や安全性を測る手法を高めていくか、どのように大規模RCTに代
替する手段を持っていくかというのが大事。
○ 医療機器あるいは体外診断用医薬品についても条件付き承認制度があるが、医薬品と同様に必ずしも利用が進ん
でいないというのが実態だと認識しており、方向性は同じであるため医療機器等についても是非議論をお願いしたい。
②その他
【第1回】
○ テーマ①や②について、見掛け上は医薬品のことだけを言っているかのような表現も多いが、実際には医療機器も関
連する内容が出てくるため、今後の議論の中で、そういったところはきちんと整理した上で議論が進むことを期待する。
-2-
-