よむ、つかう、まなぶ。
資料7 先進医療合同会議の審議結果について【報告事項】 (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_25067.html |
| 出典情報 | 先進医療会議 先進医療技術審査部会(第132回 4/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
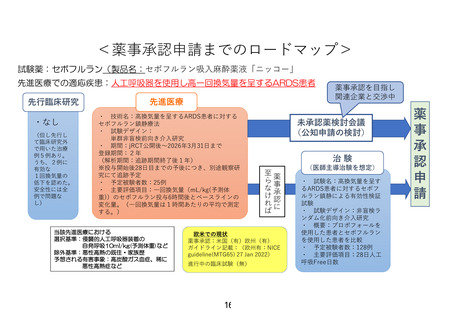
<薬事承認申請までのロードマップ>
試験薬:セボフルラン(製品名:セボフルラン吸入麻酔薬液「ニッコー」
先進医療での適応疾患:人工呼吸器を使用し高一回換気量を呈するARDS患者
先行臨床研究
・なし
・ 技術名:高換気量を呈するARDS患者に対する
セボフルラン鎮静療法
・ 試験デザイン:
単群非盲検前向き介入研究
・ 期間:jRCT公開後~2026年3月31日まで
登録期間:2年
(解析期間:追跡期間終了後1年)
※投与開始後28日目までの予後につき、別途観察研
究にて追跡予定
・ 予定被験者数:25例
・ 主要評価項目:一回換気量(mL/kg(予測体
重))のセボフルラン投与6時間後とベースラインの
変化量。(一回換気量は1時間あたりの平均で測定
する。)
当該先進医療における
選択基準:侵襲的人工呼吸器装着の
自発呼吸10ml/kg(予測体重)など
除外基準:悪性高熱の既往・家族歴
予想される有害事象:高炭酸ガス血症、稀に
悪性高熱症など
未承認薬検討会議
(公知申請の検討)
薬事承認に
至らなければ
(但し先行し
て臨床研究外
で用いた治療
例5例あり。
うち、2例に
有効な
1回換気量の
低下を認めた。
安全性には全
例で問題な
し)
先進医療
欧米での現状
薬事承認:米国(有)欧州(有)
ガイドライン記載:(欧州有:NICE
guideline(MTG65) 27 Jan 2022)
進行中の臨床試験(無)
16
薬事承認を目指し
関連企業と交渉中
治験
(医師主導治験を想定)
・ 試験名:高換気量を呈す
るARDS患者に対するセボフ
ルラン鎮静による有効性検証
試験
・ 試験デザイン:非盲検ラ
ンダム化前向き介入研究
・ 概要:プロポフォールを
使用した患者とセボフルラン
を使用した患者を比較
・ 予定被験者数:128例
・ 主要評価項目:28日人工
呼吸Free日数
薬
事
承
認
申
請
試験薬:セボフルラン(製品名:セボフルラン吸入麻酔薬液「ニッコー」
先進医療での適応疾患:人工呼吸器を使用し高一回換気量を呈するARDS患者
先行臨床研究
・なし
・ 技術名:高換気量を呈するARDS患者に対する
セボフルラン鎮静療法
・ 試験デザイン:
単群非盲検前向き介入研究
・ 期間:jRCT公開後~2026年3月31日まで
登録期間:2年
(解析期間:追跡期間終了後1年)
※投与開始後28日目までの予後につき、別途観察研
究にて追跡予定
・ 予定被験者数:25例
・ 主要評価項目:一回換気量(mL/kg(予測体
重))のセボフルラン投与6時間後とベースラインの
変化量。(一回換気量は1時間あたりの平均で測定
する。)
当該先進医療における
選択基準:侵襲的人工呼吸器装着の
自発呼吸10ml/kg(予測体重)など
除外基準:悪性高熱の既往・家族歴
予想される有害事象:高炭酸ガス血症、稀に
悪性高熱症など
未承認薬検討会議
(公知申請の検討)
薬事承認に
至らなければ
(但し先行し
て臨床研究外
で用いた治療
例5例あり。
うち、2例に
有効な
1回換気量の
低下を認めた。
安全性には全
例で問題な
し)
先進医療
欧米での現状
薬事承認:米国(有)欧州(有)
ガイドライン記載:(欧州有:NICE
guideline(MTG65) 27 Jan 2022)
進行中の臨床試験(無)
16
薬事承認を目指し
関連企業と交渉中
治験
(医師主導治験を想定)
・ 試験名:高換気量を呈す
るARDS患者に対するセボフ
ルラン鎮静による有効性検証
試験
・ 試験デザイン:非盲検ラ
ンダム化前向き介入研究
・ 概要:プロポフォールを
使用した患者とセボフルラン
を使用した患者を比較
・ 予定被験者数:128例
・ 主要評価項目:28日人工
呼吸Free日数
薬
事
承
認
申
請