よむ、つかう、まなぶ。
資料51-1-1:CSTI第三次報告を踏まえたヒト胚関係指針の見直しの検討について (32 ページ)
出典
| 公開元URL | https://www.mext.go.jp/kaigisiryo/2022/mext_00058.html |
| 出典情報 | 科学技術・学術審議会 生命倫理・安全部会(第51回 2/8)《文部科学省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
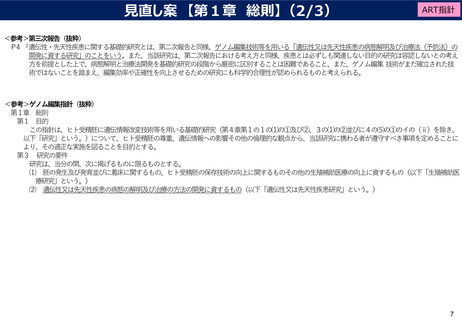
見直し案
【第一条 人クローン胚の作成の届出・第二条動物性集合胚の作成の届出】
特定胚指針
/施行規則
<見直し案>
•
デジタル原則に基づき、電磁的方法による同意の取得ができるよう特定胚指針を見直すことに伴い、紙媒体を意味する「書
面」に限定した記載となっている箇所を「説明書」に修正
見直し案(赤字見え消し)
(人クローン胚の作成の届出)
第一条 [略]
2 [略]
3 第一項に規定する届出書には、細胞の提供者の同意を得るに当たり人クローン胚を作成しようとする者又は体細胞提供
機関(人クローン胚の作成に用いるヒトの体細胞の提供を受け、作成者に当該体細胞を移送する機関をいう。)に所属す
る者が行う説明において、当該提供者に対して交付することが予定されている当該説明に関する事項を記載した書面 説明
書及び人クローン胚の取扱場所を示す図面を添付しなければならない。
(動物性集合胚の作成の届出)
第三条 [略]
2 [略]
3 第一項に規定する届出書には、細胞の提供者の同意を得るに当たり動物性集合胚を作成しようとする者が行う説明にお
いて、当該提供者に対して交付することが予定されている当該説明に関する事項を記載した書面 説明書を添付しなければ
ならない。
31
【第一条 人クローン胚の作成の届出・第二条動物性集合胚の作成の届出】
特定胚指針
/施行規則
<見直し案>
•
デジタル原則に基づき、電磁的方法による同意の取得ができるよう特定胚指針を見直すことに伴い、紙媒体を意味する「書
面」に限定した記載となっている箇所を「説明書」に修正
見直し案(赤字見え消し)
(人クローン胚の作成の届出)
第一条 [略]
2 [略]
3 第一項に規定する届出書には、細胞の提供者の同意を得るに当たり人クローン胚を作成しようとする者又は体細胞提供
機関(人クローン胚の作成に用いるヒトの体細胞の提供を受け、作成者に当該体細胞を移送する機関をいう。)に所属す
る者が行う説明において、当該提供者に対して交付することが予定されている当該説明に関する事項を記載した書面 説明
書及び人クローン胚の取扱場所を示す図面を添付しなければならない。
(動物性集合胚の作成の届出)
第三条 [略]
2 [略]
3 第一項に規定する届出書には、細胞の提供者の同意を得るに当たり動物性集合胚を作成しようとする者が行う説明にお
いて、当該提供者に対して交付することが予定されている当該説明に関する事項を記載した書面 説明書を添付しなければ
ならない。
31