議題3 参考資料 (128 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_41117.html |
| 出典情報 | 先進医療会議(第133回 7/4)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
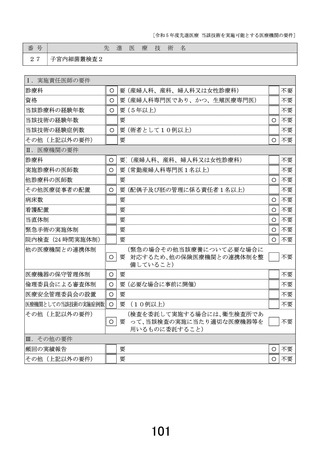
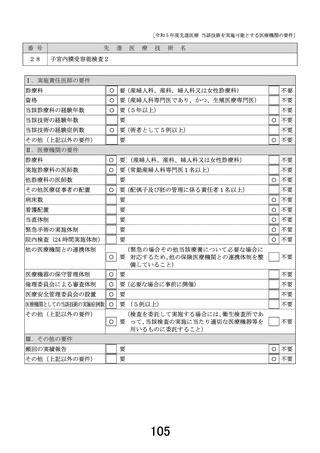
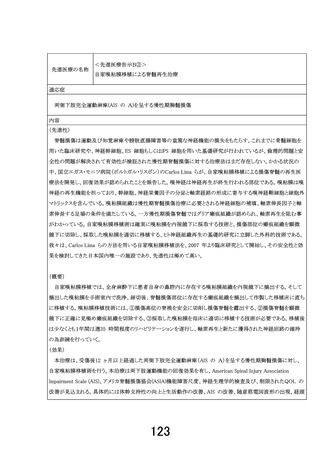
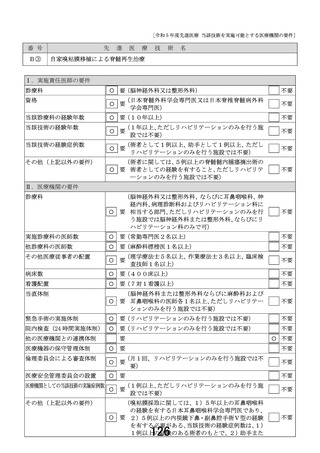
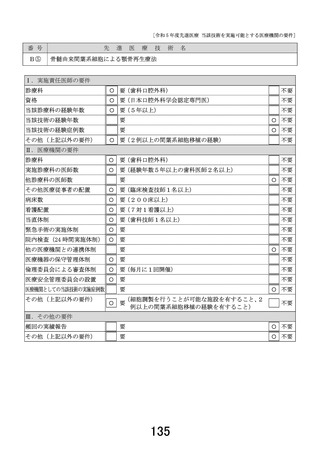
<先進医療告示B④>
マルチプレックス遺伝子パネル検査
適応症
全身化学療法未施行の切除不能進行・再発癌(消化器・肺・乳腺・婦人科・悪性黒色腫)
内容
(概要)
がん遺伝子パネル検査は2019 年6月から保険診療で実施できるようになったが、その適応は標準治療がない、
もしくは終了した(終了見込み含む)症例に限られている。一方で、Precision Medicine のコンセプトからは、初回治
療の段階から症例毎にがん細胞の遺伝子異常に合わせた治療を選択したほうが、より効果的である可能性が考えら
れてきた。
本研究では、腫瘍組織検体から作成されたホルマリン固定パラフィン包埋(FFPE)検体を米国Foundation
medicine 社に提出し解析を行い、解析結果のレポートを得る。レポートをもとにエキスパートパネルにおいて、
Actionable/Druggable な遺伝子異常の割合等を求め、初回治療法選択における遺伝子プロファイリング検査の臨
床的有用性を検証する。
・主要評価項目:
コンパニオン診断を含むActionable な遺伝子異常を有する症例の割合
・副次評価項目:
1)エキスパートパネルによる推奨治療が提示できる症例の割合、2)遺伝子異常に基づく推奨治療のマッチング
スコア、3)Druggable な遺伝子異常を有する症例の割合、4)コンパニオン診断の遺伝子異常を有する症例の割
合、5)シークエンス成功割合、6)エキスパートパネルによる推奨治療を実際に受けた症例の割合、7)全生存期
間
予定試験期間:承認日から15か月(登録期間:承認日から6か月)
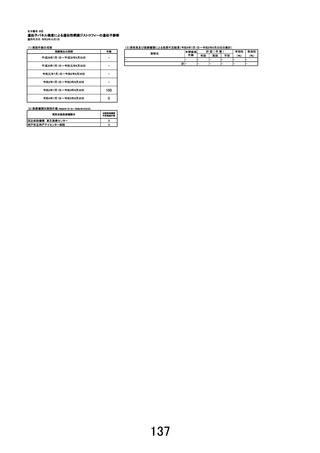
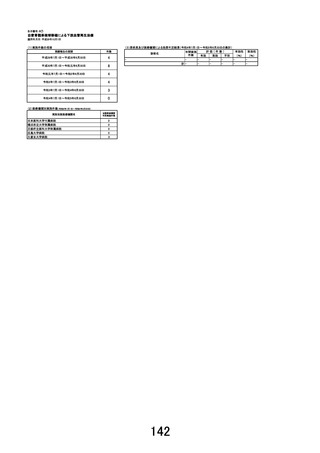
予定症例数:180 例
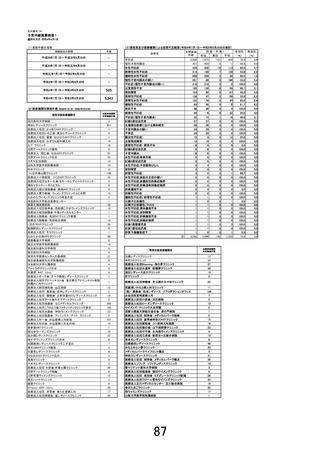
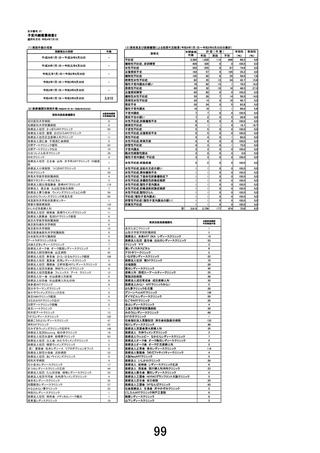
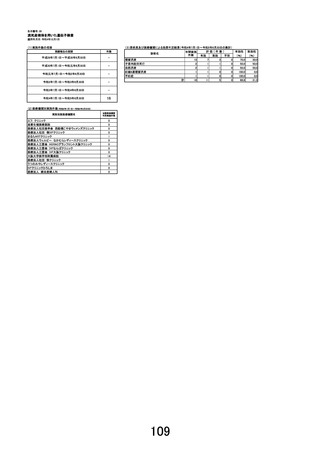
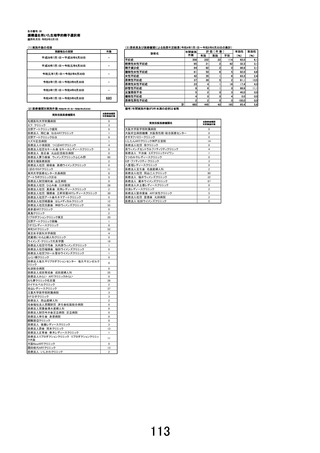
(先進医療にかかる費用)
本技術に係る総費用は487,130 円である。このうち、遺伝子解析にかかる費用462,000円は企業が負担するため、
患者負担額は25,130 円となる。
128