よむ、つかう、まなぶ。
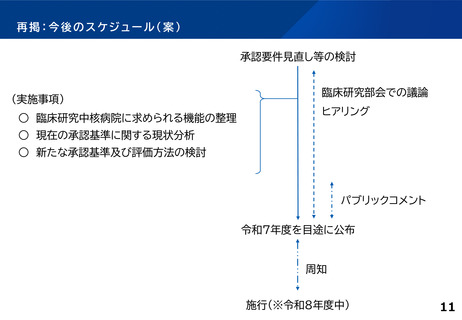
資料1:臨床研究中核病院の承認要件見直しについて (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44426.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第37回 10/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
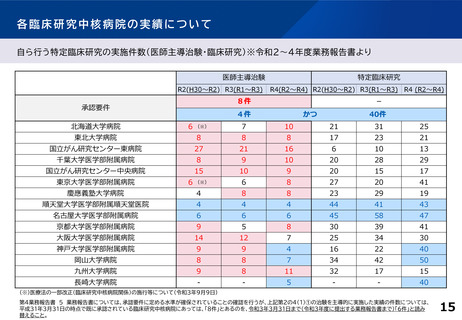
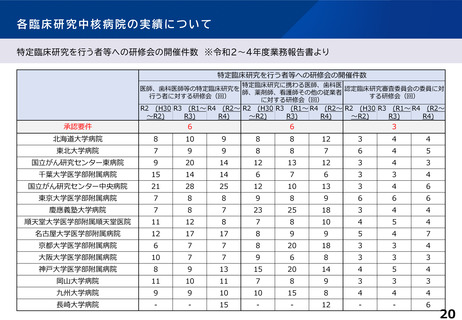
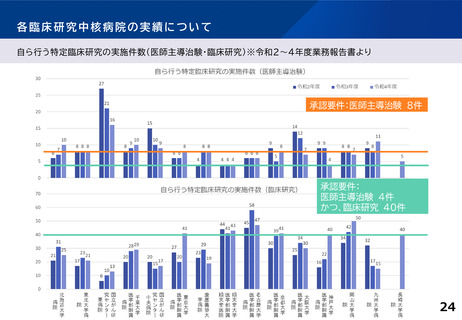
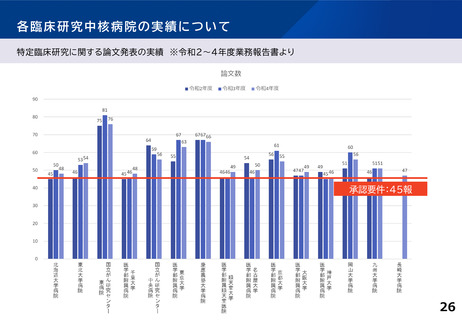
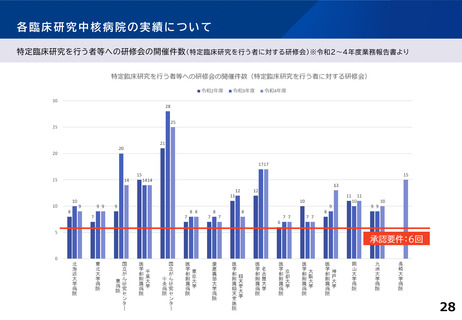
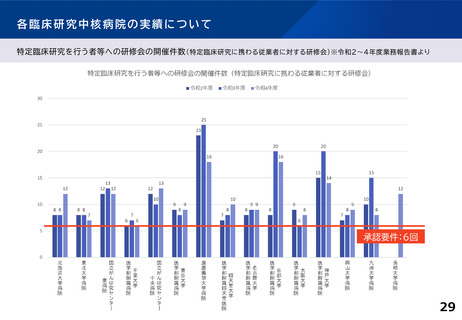
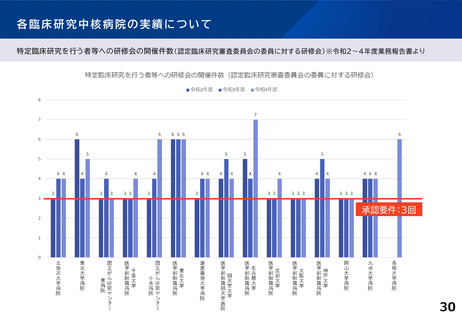
各臨床研究中核病院の実績について
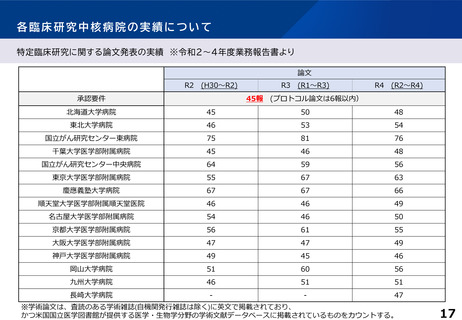
特定臨床研究に関する論文発表の実績 ※令和2~4年度業務報告書より
論文
R2
(H30~R2)
承認要件
R3
(R1~R3)
R4
(R2~R4)
45報 (プロトコル論文は6報以内)
北海道大学病院
45
50
48
東北大学病院
46
53
54
国立がん研究センター東病院
75
81
76
千葉大学医学部附属病院
45
46
48
国立がん研究センター中央病院
64
59
56
東京大学医学部附属病院
55
67
63
慶應義塾大学病院
67
67
66
順天堂大学医学部附属順天堂医院
46
46
49
名古屋大学医学部附属病院
54
46
50
京都大学医学部附属病院
56
61
55
大阪大学医学部附属病院
47
47
49
神戸大学医学部附属病院
49
45
46
岡山大学病院
51
60
56
九州大学病院
46
51
51
長崎大学病院
-
-
47
※学術論文は、査読のある学術雑誌(自機関発行雑誌は除く)に英文で掲載されており、
かつ米国国立医学図書館が提供する医学・生物学分野の学術文献データベースに掲載されているものをカウントする。
17
特定臨床研究に関する論文発表の実績 ※令和2~4年度業務報告書より
論文
R2
(H30~R2)
承認要件
R3
(R1~R3)
R4
(R2~R4)
45報 (プロトコル論文は6報以内)
北海道大学病院
45
50
48
東北大学病院
46
53
54
国立がん研究センター東病院
75
81
76
千葉大学医学部附属病院
45
46
48
国立がん研究センター中央病院
64
59
56
東京大学医学部附属病院
55
67
63
慶應義塾大学病院
67
67
66
順天堂大学医学部附属順天堂医院
46
46
49
名古屋大学医学部附属病院
54
46
50
京都大学医学部附属病院
56
61
55
大阪大学医学部附属病院
47
47
49
神戸大学医学部附属病院
49
45
46
岡山大学病院
51
60
56
九州大学病院
46
51
51
長崎大学病院
-
-
47
※学術論文は、査読のある学術雑誌(自機関発行雑誌は除く)に英文で掲載されており、
かつ米国国立医学図書館が提供する医学・生物学分野の学術文献データベースに掲載されているものをカウントする。
17