よむ、つかう、まなぶ。
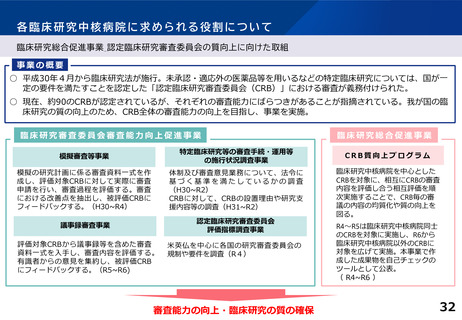
資料1:臨床研究中核病院の承認要件見直しについて (36 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44426.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第37回 10/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
小児医薬品開発ネットワーク支援事業
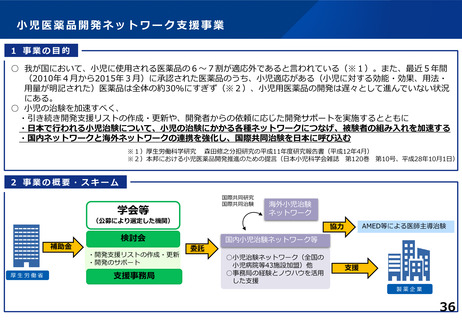
1 事業の目的
○ 我が国において、小児に使用される医薬品の6~7割が適応外であると言われている(※1)。また、最近5年間
(2010年4月から2015年3月)に承認された医薬品のうち、小児適応がある(小児に対する効能・効果、用法・
用量が明記された)医薬品は全体の約30%にすぎず(※2)、小児用医薬品の開発は遅々として進んでいない状況
にある。
○ 小児の治験を加速すべく、
・引き続き開発支援リストの作成・更新や、開発者からの依頼に応じた開発サポートを実施するとともに
・日本で行われる小児治験について、小児の治験にかかる各種ネットワークにつなげ、被験者の組み入れを加速する
・国内ネットワークと海外ネットワークの連携を強化し、国際共同治験を日本に呼び込む
※1)厚生労働科学研究 森田修之分担研究の平成11年度研究報告書(平成12年4月)
※2)本邦における小児医薬品開発推進のための提言(日本小児科学会雑誌 第120巻 第10号、平成28年10月1日)
2 事業の概要・スキーム
国際共同研究
国際共同治験
学会等
海外小児治験
ネットワーク
(公募により選定した機関)
補助金
検討会
・開発支援リストの作成・更新
・開発のサポート
厚生労働省
支援事務局
AMED等による医師主導治験
協力
国内小児治験ネットワーク等
委託
○小児治験ネットワーク(全国の
小児病院等43施設加盟)他
○事務局の経験とノウハウを活用
した支援
支援
製薬企業
36
1 事業の目的
○ 我が国において、小児に使用される医薬品の6~7割が適応外であると言われている(※1)。また、最近5年間
(2010年4月から2015年3月)に承認された医薬品のうち、小児適応がある(小児に対する効能・効果、用法・
用量が明記された)医薬品は全体の約30%にすぎず(※2)、小児用医薬品の開発は遅々として進んでいない状況
にある。
○ 小児の治験を加速すべく、
・引き続き開発支援リストの作成・更新や、開発者からの依頼に応じた開発サポートを実施するとともに
・日本で行われる小児治験について、小児の治験にかかる各種ネットワークにつなげ、被験者の組み入れを加速する
・国内ネットワークと海外ネットワークの連携を強化し、国際共同治験を日本に呼び込む
※1)厚生労働科学研究 森田修之分担研究の平成11年度研究報告書(平成12年4月)
※2)本邦における小児医薬品開発推進のための提言(日本小児科学会雑誌 第120巻 第10号、平成28年10月1日)
2 事業の概要・スキーム
国際共同研究
国際共同治験
学会等
海外小児治験
ネットワーク
(公募により選定した機関)
補助金
検討会
・開発支援リストの作成・更新
・開発のサポート
厚生労働省
支援事務局
AMED等による医師主導治験
協力
国内小児治験ネットワーク等
委託
○小児治験ネットワーク(全国の
小児病院等43施設加盟)他
○事務局の経験とノウハウを活用
した支援
支援
製薬企業
36