よむ、つかう、まなぶ。
【参考資料】これまでの議論で出された主な意見.pdf (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46170.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和6年度第9回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
②その他
【第8回】
○ 都道府県が実施する調査件数が減ってくると、都道府県の人材育成が難しくなるといった問題が出てくるため、厚生
労働省においては継続的に都道府県に対する調査支援の取組をお願いしたい。
○ 後発医薬品の新規承認時の調査について、不正事案の製造管理上の根本原因として上流問題、製剤開発・工
業化検討・技術移転等が適切に行われていないことが挙げられているが、現在のGMP省令ではこれらを確認するとの明
確な規定はない。今後、GMP調査時に重点的に確認すべき事項を改めて整理及び周知するとともに、製剤開発等を
担う製造販売業者にも承認申請の段階で確認すべき事項等があれば対応を検討いただきたい。都道府県によっては調
査件数が減少して、リーダー調査員の育成確保が難しくなることが想定されるため、調査員が必要な経験を積むことがで
きるよう、都道府県の状況に応じた支援をお願いしたい。また、区分適合性調査について、支援が不要な都道府県は自
ら調査を行うこととして、支援を必要とする都道府県に対してのみ例外的にPMDAが調査を行うような運用にしていただき
たい。制度の詳細を詰める際は、都道府県と意見交換をお願いしたい。
○ 日本の査察官のレベルがグローバルに通用するには、都道府県のキャリアパスだけでは難しい。大きな流れとして、グ
ローバルなキャリアパスになるような方向で検討するほう良いのではないか。
○ 今後の調査、監視をより充実するというのは重要なことであるため、是非都道府県と連携いただき、支援に関しては
国にお願いしたい。
-
【第2回】
○ 製薬企業が取り組むべき事項を実現できる企業体制、ガバナンスが必要になってくる。同時に、そうしたことを担保す
る都道府県における薬事監視体制の強化が必要。
-
(6)医薬品医療機器等法違反と製品回収の関係の明確化
検討項目
主な意見
法律改正との関連性 (案)
医薬品医療機器
等法違反と製品回収
の関係の明確化(運
用の改善)
ー
-
-18-
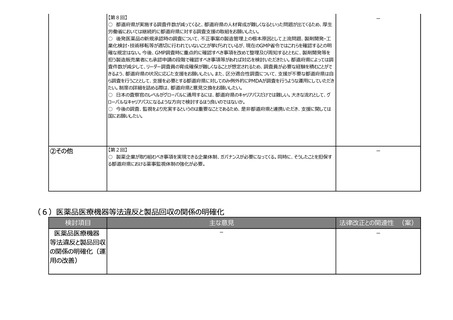
【第8回】
○ 都道府県が実施する調査件数が減ってくると、都道府県の人材育成が難しくなるといった問題が出てくるため、厚生
労働省においては継続的に都道府県に対する調査支援の取組をお願いしたい。
○ 後発医薬品の新規承認時の調査について、不正事案の製造管理上の根本原因として上流問題、製剤開発・工
業化検討・技術移転等が適切に行われていないことが挙げられているが、現在のGMP省令ではこれらを確認するとの明
確な規定はない。今後、GMP調査時に重点的に確認すべき事項を改めて整理及び周知するとともに、製剤開発等を
担う製造販売業者にも承認申請の段階で確認すべき事項等があれば対応を検討いただきたい。都道府県によっては調
査件数が減少して、リーダー調査員の育成確保が難しくなることが想定されるため、調査員が必要な経験を積むことがで
きるよう、都道府県の状況に応じた支援をお願いしたい。また、区分適合性調査について、支援が不要な都道府県は自
ら調査を行うこととして、支援を必要とする都道府県に対してのみ例外的にPMDAが調査を行うような運用にしていただき
たい。制度の詳細を詰める際は、都道府県と意見交換をお願いしたい。
○ 日本の査察官のレベルがグローバルに通用するには、都道府県のキャリアパスだけでは難しい。大きな流れとして、グ
ローバルなキャリアパスになるような方向で検討するほう良いのではないか。
○ 今後の調査、監視をより充実するというのは重要なことであるため、是非都道府県と連携いただき、支援に関しては
国にお願いしたい。
-
【第2回】
○ 製薬企業が取り組むべき事項を実現できる企業体制、ガバナンスが必要になってくる。同時に、そうしたことを担保す
る都道府県における薬事監視体制の強化が必要。
-
(6)医薬品医療機器等法違反と製品回収の関係の明確化
検討項目
主な意見
法律改正との関連性 (案)
医薬品医療機器
等法違反と製品回収
の関係の明確化(運
用の改善)
ー
-
-18-