よむ、つかう、まなぶ。
資料2.セルフケア・セルフメディケーション推進の取組 (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_48502.html |
| 出典情報 | セルフケア・セルフメディケーション推進に関する有識者検討会(第1回 1/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
ス イ ッ チ OTC の 審 査 の 改 善 方 策 等 に つ い て
要指導・⼀般⽤医薬品部会(令和6年9⽉4⽇開催)において、スイッチOTC WG(※1)から以下の報告を⾏った。
•
スイッチOTCの申請において、①元となる医療⽤医薬品と⽣物学的同等性が確認されている場合であり、また、②元
となる医療⽤医薬品と同⼀成分及び分量並びに剤形で、かつ、③効能⼜は効果が元となる医療⽤医薬品の承認事項の
範囲内であり、各々の効能⼜は効果について⽤法及び⽤量が元となる医療⽤医薬品の承認事項と同⼀であるスイッチ
OTCについては、医療⽤医薬品の臨床試験結果の再解析やスイッチOTCとしての新たな臨床試験を⾏うことなく、ま
た 医療⽤医薬品の臨床試験結果に関する承認申請資料を提出することなく、スイッチOTCの申請を⾏えることとすべ
きである。(※2)
•
「規制改⾰実施計画(令和6年6⽉21日)」(閣議決定)において、スイッチOTC化の承認申請から承認の可否判断
までの総期間を1年以内に設定すると定められたことを確実に達成するためには、当局側及び申請企業側双⽅がそれ
に向けて努⼒を⾏う必要があるため、照会・回答に際して期限を設定する等、今後、詳細な標準的プロセスの検討を
開始することとする。更に、業界側では、各企業が適切な申請を⾏えるようにするための申請ガイダンスを今後作成
し、それに則した申請を実施するとともに、当局側では、PMDAにおいて、スイッチOTCに関してその妥当性等を申
請前から申請企業が判断しやすくするように、新たな対面助言の枠組みを設置し、申請企業がその枠組みを十分活用
することとする。なお、この両者の取組は、定期的にフォローアップし、改善方策を両者で協議することとする。
•
引き続き、製造販売後の安全確保方策を実施するにあたり、製造販売後調査は重要であることには変わりないが、今
後の調査に際しては、
①
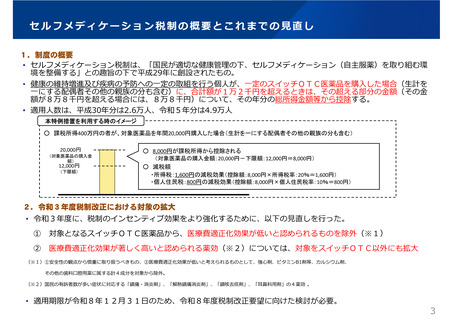
従来、製造販売後安全性調査における副作⽤頻度調査の調査予定症例数について、原則として内服薬は3,000
例、外⽤薬は1,000例の収集を指導してきたところであるが、品⽬の特性に応じた、より適切な調査予定症例
数の設定等や、
②
調査⽅法について、従来のモニター店舗を介した⽅法に加え、例えばQRコードを利⽤した購⼊者からの直接回
答等、電子化を含むより効率的・効果的な方法の追加
について、検討を⾏い、所要の措置を講じることとする。
※1
※2
厚⽣労働省・PMDA及び日本OTC医薬品協会からなる検討会議
令和6年10月9日付で関係通知等を改正済み。
23
要指導・⼀般⽤医薬品部会(令和6年9⽉4⽇開催)において、スイッチOTC WG(※1)から以下の報告を⾏った。
•
スイッチOTCの申請において、①元となる医療⽤医薬品と⽣物学的同等性が確認されている場合であり、また、②元
となる医療⽤医薬品と同⼀成分及び分量並びに剤形で、かつ、③効能⼜は効果が元となる医療⽤医薬品の承認事項の
範囲内であり、各々の効能⼜は効果について⽤法及び⽤量が元となる医療⽤医薬品の承認事項と同⼀であるスイッチ
OTCについては、医療⽤医薬品の臨床試験結果の再解析やスイッチOTCとしての新たな臨床試験を⾏うことなく、ま
た 医療⽤医薬品の臨床試験結果に関する承認申請資料を提出することなく、スイッチOTCの申請を⾏えることとすべ
きである。(※2)
•
「規制改⾰実施計画(令和6年6⽉21日)」(閣議決定)において、スイッチOTC化の承認申請から承認の可否判断
までの総期間を1年以内に設定すると定められたことを確実に達成するためには、当局側及び申請企業側双⽅がそれ
に向けて努⼒を⾏う必要があるため、照会・回答に際して期限を設定する等、今後、詳細な標準的プロセスの検討を
開始することとする。更に、業界側では、各企業が適切な申請を⾏えるようにするための申請ガイダンスを今後作成
し、それに則した申請を実施するとともに、当局側では、PMDAにおいて、スイッチOTCに関してその妥当性等を申
請前から申請企業が判断しやすくするように、新たな対面助言の枠組みを設置し、申請企業がその枠組みを十分活用
することとする。なお、この両者の取組は、定期的にフォローアップし、改善方策を両者で協議することとする。
•
引き続き、製造販売後の安全確保方策を実施するにあたり、製造販売後調査は重要であることには変わりないが、今
後の調査に際しては、
①
従来、製造販売後安全性調査における副作⽤頻度調査の調査予定症例数について、原則として内服薬は3,000
例、外⽤薬は1,000例の収集を指導してきたところであるが、品⽬の特性に応じた、より適切な調査予定症例
数の設定等や、
②
調査⽅法について、従来のモニター店舗を介した⽅法に加え、例えばQRコードを利⽤した購⼊者からの直接回
答等、電子化を含むより効率的・効果的な方法の追加
について、検討を⾏い、所要の措置を講じることとする。
※1
※2
厚⽣労働省・PMDA及び日本OTC医薬品協会からなる検討会議
令和6年10月9日付で関係通知等を改正済み。
23