よむ、つかう、まなぶ。
資料1-2 調査結果報告書 (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27607.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第10回) |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
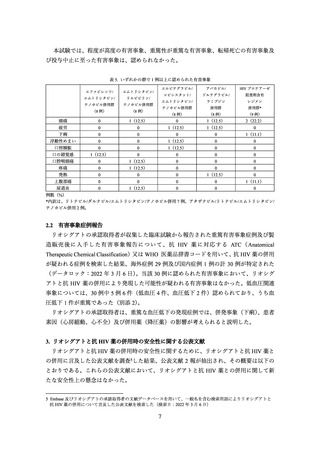
ヒストリカルコントロールとして 11261 試験及び 13009 試験の両試験を用いた場合(食
後及び空腹時投与)のリオシグアト単独投与時に対する抗 HIV 薬併用投与時のリオシグア
トの AUC の比は、表 3 のとおりであった。リオシグアトの Cmax は食事の影響を受けること
が示されているため、Cmax の比は算出されていない。
表 3.リオシグアト単独投与時(食後及び空腹時)に対する抗 HIV 薬併用時の
リオシグアトの AUC の比
AUC
比
エファビレンツ
/エムトリシタビン
/テノホビル併用群
(7 例)
エムトリシタビン
/リルピビリン
/テノホビル併用群
(8 例)
エルビテグラビル
/コビシスタット
/エムトリシタビン
/テノホビル併用群
(8 例)
アバカビル
/ドルテグラビル/
ラミブジン
併用群
(8 例)
HIV プロテアーゼ
阻害剤含有レジメ
ン併用群
(8 例)
1.0639
(0.6197, 1.8263)
2.0617
(1.2368, 3.4367)
2.0647
(1.2386, 3.4418)
2.8402
(1.7038 , 4.7345)
1.2900
(0.7739, 2.1504)
最小二乗平均値の比(90%信頼区間)
また、ヒストリカルコントロールとして 13009 試験のみを用いた場合(空腹時投与)のリ
オシグアト単独投与時に対する抗 HIV 薬併用投与時のリオシグアトの AUC 及び Cmax の比
は、表 4 のとおりであった。
表 4.リオシグアト単独投与時(空腹時)に対する抗 HIV 薬併用時の
リオシグアトの AUC 及び Cmax の比
エファビレンツ
/エムトリシタビン
/テノホビル併用群
(7 例)
エムトリシタビン
/リルピビリン
/テノホビル併用群
(8 例)
エルビテグラビル
/コビシスタット
/エムトリシタビン
/テノホビル併用群
(8 例)
アバカビル
/ドルテグラビル/
ラミブジン
併用群
(8 例)
HIV プロテアーゼ
阻害剤含有レジメ
ン併用群
(8 例)
AUC
比
0.9703
(0.5414, 1.7390)
1.8803
(1.0799, 3.2738)
1.8831
(1.0816, 3.2786)
2.5903
(1.4877, 4.5099)
1.1765
(0.6757, 2.0485)
Cmax 比
0.8955
(0.6728, 1.1919)
1.0299
(0.7738, 1.3708)
1.2859
(0.9661, 1.7116)
1.2657
(0.9509, 1.6847)
1.0006
(0.7517, 1.3318)
最小二乗平均値の比(90%信頼区間)
なお、リオシグアトの承認取得者は、17957 試験、11261 試験及び 13009 試験を比較する
ことの適切性について、以下のように説明した。
PAH 患者及び慢性血栓塞栓性肺高血圧症患者を対象とした第Ⅲ相試験のデータを用いて
実施した母集団薬物動態解析(以下、
「PPK 解析」)の結果、リオシグアトの薬物動態の最終
モデルは、見かけのクリアランス(以下、
「CL/F」)、見かけの分布容積(以下、
「V/F」)及び
一次吸収速度定数をパラメータとした経口 1-コンパートメントモデルで示され、CL/F の共
変量としてクレアチニン・クリアランス、ビリルビン、喫煙の有無及びボセンタン併用の有
無が、V/F の共変量として体重が選択されている。
被験者の年齢、体重及び BMI は 3 試験間で同程度であり、性別及び民族の分布は試験間
で異なるが PPK 解析の最終モデルの共変量に選択されておらず、リオシグアトの薬物動態
に大きな影響を及ぼさないと考える。喫煙は CL/F の共変量であるが、喫煙者の割合に試験
4
後及び空腹時投与)のリオシグアト単独投与時に対する抗 HIV 薬併用投与時のリオシグア
トの AUC の比は、表 3 のとおりであった。リオシグアトの Cmax は食事の影響を受けること
が示されているため、Cmax の比は算出されていない。
表 3.リオシグアト単独投与時(食後及び空腹時)に対する抗 HIV 薬併用時の
リオシグアトの AUC の比
AUC
比
エファビレンツ
/エムトリシタビン
/テノホビル併用群
(7 例)
エムトリシタビン
/リルピビリン
/テノホビル併用群
(8 例)
エルビテグラビル
/コビシスタット
/エムトリシタビン
/テノホビル併用群
(8 例)
アバカビル
/ドルテグラビル/
ラミブジン
併用群
(8 例)
HIV プロテアーゼ
阻害剤含有レジメ
ン併用群
(8 例)
1.0639
(0.6197, 1.8263)
2.0617
(1.2368, 3.4367)
2.0647
(1.2386, 3.4418)
2.8402
(1.7038 , 4.7345)
1.2900
(0.7739, 2.1504)
最小二乗平均値の比(90%信頼区間)
また、ヒストリカルコントロールとして 13009 試験のみを用いた場合(空腹時投与)のリ
オシグアト単独投与時に対する抗 HIV 薬併用投与時のリオシグアトの AUC 及び Cmax の比
は、表 4 のとおりであった。
表 4.リオシグアト単独投与時(空腹時)に対する抗 HIV 薬併用時の
リオシグアトの AUC 及び Cmax の比
エファビレンツ
/エムトリシタビン
/テノホビル併用群
(7 例)
エムトリシタビン
/リルピビリン
/テノホビル併用群
(8 例)
エルビテグラビル
/コビシスタット
/エムトリシタビン
/テノホビル併用群
(8 例)
アバカビル
/ドルテグラビル/
ラミブジン
併用群
(8 例)
HIV プロテアーゼ
阻害剤含有レジメ
ン併用群
(8 例)
AUC
比
0.9703
(0.5414, 1.7390)
1.8803
(1.0799, 3.2738)
1.8831
(1.0816, 3.2786)
2.5903
(1.4877, 4.5099)
1.1765
(0.6757, 2.0485)
Cmax 比
0.8955
(0.6728, 1.1919)
1.0299
(0.7738, 1.3708)
1.2859
(0.9661, 1.7116)
1.2657
(0.9509, 1.6847)
1.0006
(0.7517, 1.3318)
最小二乗平均値の比(90%信頼区間)
なお、リオシグアトの承認取得者は、17957 試験、11261 試験及び 13009 試験を比較する
ことの適切性について、以下のように説明した。
PAH 患者及び慢性血栓塞栓性肺高血圧症患者を対象とした第Ⅲ相試験のデータを用いて
実施した母集団薬物動態解析(以下、
「PPK 解析」)の結果、リオシグアトの薬物動態の最終
モデルは、見かけのクリアランス(以下、
「CL/F」)、見かけの分布容積(以下、
「V/F」)及び
一次吸収速度定数をパラメータとした経口 1-コンパートメントモデルで示され、CL/F の共
変量としてクレアチニン・クリアランス、ビリルビン、喫煙の有無及びボセンタン併用の有
無が、V/F の共変量として体重が選択されている。
被験者の年齢、体重及び BMI は 3 試験間で同程度であり、性別及び民族の分布は試験間
で異なるが PPK 解析の最終モデルの共変量に選択されておらず、リオシグアトの薬物動態
に大きな影響を及ぼさないと考える。喫煙は CL/F の共変量であるが、喫煙者の割合に試験
4