よむ、つかう、まなぶ。
資料1-2 チェストベリー乾燥エキスのリスク区分について (26 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31510.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第4回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
なし
4,855
安全性解析対象症例数
副作用等の発現症例数
副作用等の発現割合
アレルギー歴
不明・未記載
112
あり
700
318
91
8
417
6.55%
13.00%
7.14%
7.36%
副作用等の種類
副作用等の種類別発現症例数(発現割合)
-
22 (0.39%)
*
胸痛
1 (0.02%)
-
-
1 (0.02%)
*
顔面浮腫
1 (0.02%)
-
-
1 (0.02%)
*
異常感
1 (0.02%)
-
-
1 (0.02%)
*
倦怠感
4 (0.08%)
-
5 (0.09%)
*
倦怠感 注
浮腫
*
浮腫 注
末梢性浮腫
*
末梢性浮腫 注
顔面腫脹
1 (0.02%)
*
異物感
1 (0.02%)
臨床検査
3 (0.06%)
3 (0.06%)
一般・全身障害および投与部位の状態
)
)
*
20 (0.41%)
体重増加
1 (0.14%)
7 (0.14%)
-
-
7 (0.12%)
1 (0.02%)
-
-
1 (0.02%)
1 (0.02%)
-
-
1 (0.02%)
2 (0.04%)
-
-
2 (0.04%)
-
1 (0.02%)
-
-
1 (0.02%)
-
-
1 (0.02%)
1 (0.14%)
-
4 (0.07%)
1 (0.14%)
-
-
)
2 (0.29%)
1 (0.14%)
*:「使用上の注意」から予測できない副作用・感染症
注):月経前症候群の症状の増悪であるため「使用上の注意」から予測できると判断し「既知」とした
[ ]:重篤
2)
合計
5,667
4 (0.07%)
MedDRA/J version(23.1)
合併症の有無
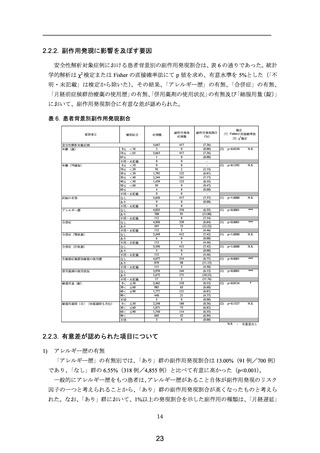
「合併症」の有無別では、
「あり」群の副作用発現割合は 12.23%(73 例/597 例)であり、
「なし」群の 6.84%(339 例/4,958 例)と比べて有意に高かった(p<0.001)。
合併症の有無については、「合併症(腎疾患)」の有無別及び「合併症(肝疾患)」の有無
別の層別解析も実施した(表 6)。それぞれ腎疾患の合併症「あり」の対象症例は 6 例、肝
疾患の合併症「あり」の対象症例は 5 例と少なかったが、それぞれ副作用発現はなく、腎疾
患及び肝疾患の合併症による副作用発現への影響で問題となることはなかった。本剤が服用
される集団では、腎疾患及び肝疾患の合併症を持つ症例は少ないことが推測された。
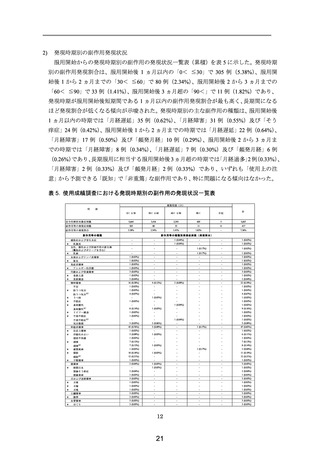
患者背景別の副作用発現割合で有意差が認められた「併用薬剤の使用状況」の有無の割合
が影響した可能性を検討した結果、表 8 のとおり、「併用薬剤の使用状況」の「あり」群の
割合は、「合併症」の「あり」群で 70.69%(422 例/597 例)、「なし」群で 24.55%(1,217
例/4,958 例)であった。
「合併症あり」群において副作用発現割合が高くなった要因として、
合併症に対する薬剤の服用により併用薬剤の使用状況ありの割合が高くなったことが影響
を及ぼした可能性が考えられた。
表 8. 合併症(あり・なし)別の併用薬剤の使用状況ありの割合
あり
併用薬剤の
使用状況あり
422
併用薬剤の
使用状況なし
168
併用薬剤の
使用状況不明・未記載
7
併用薬剤の
使用状況ありの割合
70.69%
なし
1,217
3,732
9
24.55%
合併症
なお、
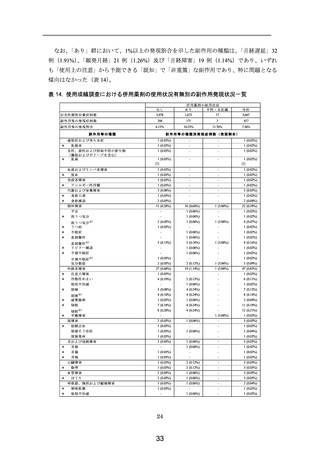
「合併症」の「あり」群において、1%以上の発現割合を示した副作用の種類は、
「月
経障害」12 例(2.01%)、
「月経遅延」9 例(1.51%)、
「頻発月経」9 例(1.51%)、
「そう痒症」
6 例(1.01%)、「月経過多」6 例(1.01%)及び「不正子宮出血」6 例(1.01%)であり、「月
経障害」、
「月経遅延」、
「頻発月経」
、
「そう痒症」及び「月経過多」は「使用上の注意」から
予測できる「既知」で「非重篤」な副作用であり、特に問題となる傾向はなかった。「不正
子宮出血」は予測できない「未知」で「非重篤」な副作用であったが、転帰については「不
17
26
4,855
安全性解析対象症例数
副作用等の発現症例数
副作用等の発現割合
アレルギー歴
不明・未記載
112
あり
700
318
91
8
417
6.55%
13.00%
7.14%
7.36%
副作用等の種類
副作用等の種類別発現症例数(発現割合)
-
22 (0.39%)
*
胸痛
1 (0.02%)
-
-
1 (0.02%)
*
顔面浮腫
1 (0.02%)
-
-
1 (0.02%)
*
異常感
1 (0.02%)
-
-
1 (0.02%)
*
倦怠感
4 (0.08%)
-
5 (0.09%)
*
倦怠感 注
浮腫
*
浮腫 注
末梢性浮腫
*
末梢性浮腫 注
顔面腫脹
1 (0.02%)
*
異物感
1 (0.02%)
臨床検査
3 (0.06%)
3 (0.06%)
一般・全身障害および投与部位の状態
)
)
*
20 (0.41%)
体重増加
1 (0.14%)
7 (0.14%)
-
-
7 (0.12%)
1 (0.02%)
-
-
1 (0.02%)
1 (0.02%)
-
-
1 (0.02%)
2 (0.04%)
-
-
2 (0.04%)
-
1 (0.02%)
-
-
1 (0.02%)
-
-
1 (0.02%)
1 (0.14%)
-
4 (0.07%)
1 (0.14%)
-
-
)
2 (0.29%)
1 (0.14%)
*:「使用上の注意」から予測できない副作用・感染症
注):月経前症候群の症状の増悪であるため「使用上の注意」から予測できると判断し「既知」とした
[ ]:重篤
2)
合計
5,667
4 (0.07%)
MedDRA/J version(23.1)
合併症の有無
「合併症」の有無別では、
「あり」群の副作用発現割合は 12.23%(73 例/597 例)であり、
「なし」群の 6.84%(339 例/4,958 例)と比べて有意に高かった(p<0.001)。
合併症の有無については、「合併症(腎疾患)」の有無別及び「合併症(肝疾患)」の有無
別の層別解析も実施した(表 6)。それぞれ腎疾患の合併症「あり」の対象症例は 6 例、肝
疾患の合併症「あり」の対象症例は 5 例と少なかったが、それぞれ副作用発現はなく、腎疾
患及び肝疾患の合併症による副作用発現への影響で問題となることはなかった。本剤が服用
される集団では、腎疾患及び肝疾患の合併症を持つ症例は少ないことが推測された。
患者背景別の副作用発現割合で有意差が認められた「併用薬剤の使用状況」の有無の割合
が影響した可能性を検討した結果、表 8 のとおり、「併用薬剤の使用状況」の「あり」群の
割合は、「合併症」の「あり」群で 70.69%(422 例/597 例)、「なし」群で 24.55%(1,217
例/4,958 例)であった。
「合併症あり」群において副作用発現割合が高くなった要因として、
合併症に対する薬剤の服用により併用薬剤の使用状況ありの割合が高くなったことが影響
を及ぼした可能性が考えられた。
表 8. 合併症(あり・なし)別の併用薬剤の使用状況ありの割合
あり
併用薬剤の
使用状況あり
422
併用薬剤の
使用状況なし
168
併用薬剤の
使用状況不明・未記載
7
併用薬剤の
使用状況ありの割合
70.69%
なし
1,217
3,732
9
24.55%
合併症
なお、
「合併症」の「あり」群において、1%以上の発現割合を示した副作用の種類は、
「月
経障害」12 例(2.01%)、
「月経遅延」9 例(1.51%)、
「頻発月経」9 例(1.51%)、
「そう痒症」
6 例(1.01%)、「月経過多」6 例(1.01%)及び「不正子宮出血」6 例(1.01%)であり、「月
経障害」、
「月経遅延」、
「頻発月経」
、
「そう痒症」及び「月経過多」は「使用上の注意」から
予測できる「既知」で「非重篤」な副作用であり、特に問題となる傾向はなかった。「不正
子宮出血」は予測できない「未知」で「非重篤」な副作用であったが、転帰については「不
17
26