材ー1参考3○ 令和6年度保険医療材料制度の見直しについて (61 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212455_00041.html |
| 出典情報 | 中央社会保険医療協議会 保険医療材料専門部会(第127回 1/17)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
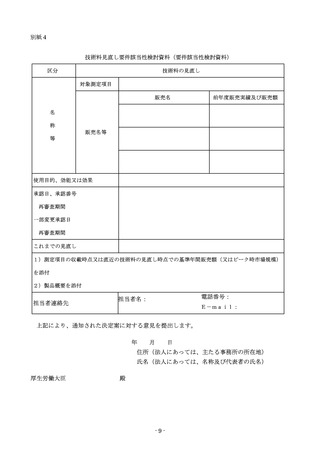
料価格基準の機能区分をいう。以下同じ。)のいずれかが変更となる場合は、最
終一部変更時の薬事承認書又は認証書、あるいは最終の変更計画に従った変更時
の変更計画に従った変更に係る届書(以下「変更届書」という。)の写し並びに
添付文書及び保険適用希望書を提出する。その際、最終一部変更あるいは変更計
画に従った変更時に「使用目的又は効果」、「形状、構造及び原理」、「原材
料」又は「使用方法」の変更がなかった場合はそれらの項目について最新の情報
が記載されている過去の薬事承認書、認証書又は変更届書の写しを併せて提出す
ること。
② 既に保険適用されている医療機器が一部変更承認又は一部変更認証された場合、
あるいは変更計画に従った変更を行う旨を届け出た場合であって、当該一部変更、
あるいは変更計画に従った変更により該当する機能区分等が変更となり、変更後
の機能区分等が既存の機能区分等に該当する場合は、保険適用希望書に変更事項
を明記のうえ提出すること。
③ 既に保険適用されている医療機器が一部変更承認又は一部変更認証された場合、
あるいは変更計画に従った変更を行う旨を届け出た場合であって、当該一部変更
あるいは変更計画に従った変更により該当する機能区分等が変更となり、変更後
の機能区分等が既存の機能区分等に該当しない場合は、決定区分A3(既存技
術・変更あり)、B2(既存機能区分・変更あり)、B3(期限付改良加算・暫
定機能区分)、C1(新機能)又はC2(新機能・新技術)として新たに保険適
用希望書を提出すること。
④ 既に保険適用されている医療機器について、一部変更承認又は一部変更認証、
あるいは変更計画に従った変更以外の理由により、当該保険適用の前提となって
いる既に提出された保険適用希望書の「製品名・製品コード」欄の記載内容に変
更が生じた場合は、保険適用希望書に変更事項を明記のうえ提出すること。
⑤ 既に保険適用されている医療機器が一部変更承認若しくは一部変更認証された
場合、あるいは変更計画に従った変更又は既に保険適用されている機能区分の定
義等が変更された場合であって、当該変更あるいは変更計画に従った変更により
該当する機能区分等が変更となるか否かについて疑義が生じた場合には、医政局
経済課に事前相談すること。
2
製造販売業者からの意見聴取
製造販売業者からの意見聴取の時期及び場所は、医政局経済課から製造販売業者に
対し直接連絡し、随時実施するものとする。
3
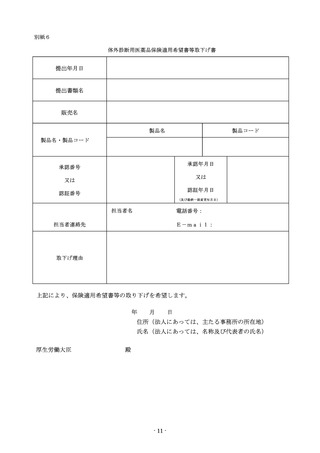
保険適用不服意見書の提出方法について
製造販売業者は、通知された決定案について保険適用不服意見書を提出する場合は、
その根拠となる資料とともに、当該通知を受けた日から起算して7日以内(ただし、
休日等を除いて計算する日数とする。)に医政局経済課へ提出すること。
ただし、根拠となる資料を保険適用不服意見書と併せて提出することが困難と認め
られる場合には、当該不服意見書を提出した日から起算して14日以内(ただし、休
日等を除いて計算する日数とする。)に提出することができる。
なお、通知された決定案について同意する場合には、同意書を、当該通知を受けた
日から7日以内(ただし、休日等を除いて計算する日数とする。)に医政局経済課へ
提出すること。
4
新規品の保険適用等について
取扱い通知の2の(2)、3の(5)及び4の(6)のとおりとする。ただし、3
月 、 6 月 、 9 月 及 び 12 月 を 基 準 と し て 保 険 適 用 す る 場 合 に あ っ て は 保 険 適 用 開 始 月
の1月前の末日までに決定区分B3(期限付改良加算・暫定機能区分)、C1(新機
- 3 -