よむ、つかう、まなぶ。
○先進医療Bに係る新規技術の科学的評価等について別紙3 (36 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00049.html |
| 出典情報 | 先進医療会議(第113回 8/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
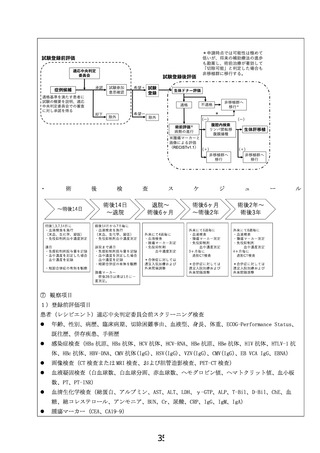
パンチ生検または擦過・胆汁細胞診については胆管造影検査実施時に施行可能な症例で行う
抗体検査(抗核抗体、M2 抗体、抗ミトコンドリア抗体)
肝機能検査(ICG15 分停滞率もしくは 99mTc-GSA15 分値)
尿検査(蛋白、糖、比重、赤血球、白血球)
呼吸機能:Hugh-Jones 呼吸機能分類(肺機能検査、胸部 X 線検査)
心機能:NYHA 機能分類(心エコー検査、心電図)
*適応評価に至るも登録に至らない症例はその事由を記録する
2)登録後から生体肝移植までの評価項目
患者(レシピエント)スクリーニング検査(生体肝移植前)
血液凝固検査(白血球数、白血球分画、赤血球数、ヘモグロビン値、ヘマトクリット値、血小板
数、PT%、PT-INR)
血清生化学検査(総蛋白、アルブミン、AST、ALT、LDH、γ-GTP、ALP、T-Bil、D-Bil、ChE、血
糖、総コレステロール、アンモニア、BUN、Cr、尿酸、CRP、IgG、IgM、IgA)
腫瘍マーカー(CEA、CA19-9)
呼吸機能および心機能については術前治療の有害事象などで悪化が懸念された場合に再検査を行う
術前検査
<研究登録後に施行した治療及び治療後の病勢評価、並びに安全性について>
化学療法:レジメン、初回投与日、最終投与日、治療効果(明らかな肝内転移およびリンパ節を
含む肝外転移の有無、および原発腫瘍について可能な場合には RECISTv1.1 に基づく最良総合効
果(研究担当医師判定))
、CTCAE-Grade3 を超える有害事象の有無と種類(発生時点で評価)
放射線治療:照射量、照射回数、治療開始日、治療終了日、CTCAE-Grade3 を超える有害事象の
有無と種類(発生時点で評価)
病勢評価画像検索:CT 検査または MRI 検査、および PET-CT 検査を術前治療 3 ヶ月終了時点(腹
腔内検索実施前 1 ヶ月以内)で施行する ※経過中の効果判定はベースライン評価と同じ検査方
法で行う。
試験開腹:試験開腹日、アプローチ(開腹 or 腹腔鏡)
、試験開腹所見
生体ドナースクリーニング検査
年齢、性別、患者との関係性、血液型、身長、体重、既往歴、手術歴
感染症検査(HBs 抗原、HBs 抗体、HCV 抗体、HIV 抗体、HTLV-1 抗体、CMV 抗体)
血液凝固検査(白血球数、白血球分画、赤血球数、ヘモグロビン値、ヘマトクリット値、血小板
数、PT%、PT-INR)
血清生化学検査(総蛋白、アルブミン、AST、ALT、LDH、γ-GTP、ALP、T-Bil、D-Bil、ChE、血
糖、総コレステロール、アンモニア、BUN、Cr、尿酸、CRP、IgG、IgM、IgA)
尿検査(蛋白、糖、比重、赤血球、白血球)
呼吸機能:呼吸機能検査(%VC、FEV 1.0%、FEV1.0)、胸部 X 線所見
心機能:心電図検査・心エコー検査
36
抗体検査(抗核抗体、M2 抗体、抗ミトコンドリア抗体)
肝機能検査(ICG15 分停滞率もしくは 99mTc-GSA15 分値)
尿検査(蛋白、糖、比重、赤血球、白血球)
呼吸機能:Hugh-Jones 呼吸機能分類(肺機能検査、胸部 X 線検査)
心機能:NYHA 機能分類(心エコー検査、心電図)
*適応評価に至るも登録に至らない症例はその事由を記録する
2)登録後から生体肝移植までの評価項目
患者(レシピエント)スクリーニング検査(生体肝移植前)
血液凝固検査(白血球数、白血球分画、赤血球数、ヘモグロビン値、ヘマトクリット値、血小板
数、PT%、PT-INR)
血清生化学検査(総蛋白、アルブミン、AST、ALT、LDH、γ-GTP、ALP、T-Bil、D-Bil、ChE、血
糖、総コレステロール、アンモニア、BUN、Cr、尿酸、CRP、IgG、IgM、IgA)
腫瘍マーカー(CEA、CA19-9)
呼吸機能および心機能については術前治療の有害事象などで悪化が懸念された場合に再検査を行う
術前検査
<研究登録後に施行した治療及び治療後の病勢評価、並びに安全性について>
化学療法:レジメン、初回投与日、最終投与日、治療効果(明らかな肝内転移およびリンパ節を
含む肝外転移の有無、および原発腫瘍について可能な場合には RECISTv1.1 に基づく最良総合効
果(研究担当医師判定))
、CTCAE-Grade3 を超える有害事象の有無と種類(発生時点で評価)
放射線治療:照射量、照射回数、治療開始日、治療終了日、CTCAE-Grade3 を超える有害事象の
有無と種類(発生時点で評価)
病勢評価画像検索:CT 検査または MRI 検査、および PET-CT 検査を術前治療 3 ヶ月終了時点(腹
腔内検索実施前 1 ヶ月以内)で施行する ※経過中の効果判定はベースライン評価と同じ検査方
法で行う。
試験開腹:試験開腹日、アプローチ(開腹 or 腹腔鏡)
、試験開腹所見
生体ドナースクリーニング検査
年齢、性別、患者との関係性、血液型、身長、体重、既往歴、手術歴
感染症検査(HBs 抗原、HBs 抗体、HCV 抗体、HIV 抗体、HTLV-1 抗体、CMV 抗体)
血液凝固検査(白血球数、白血球分画、赤血球数、ヘモグロビン値、ヘマトクリット値、血小板
数、PT%、PT-INR)
血清生化学検査(総蛋白、アルブミン、AST、ALT、LDH、γ-GTP、ALP、T-Bil、D-Bil、ChE、血
糖、総コレステロール、アンモニア、BUN、Cr、尿酸、CRP、IgG、IgM、IgA)
尿検査(蛋白、糖、比重、赤血球、白血球)
呼吸機能:呼吸機能検査(%VC、FEV 1.0%、FEV1.0)、胸部 X 線所見
心機能:心電図検査・心エコー検査
36