よむ、つかう、まなぶ。
薬-1○関係業界からの意見聴取について (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212451_00073.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第209回 9/20)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
③ 新薬創出等加算の見直し
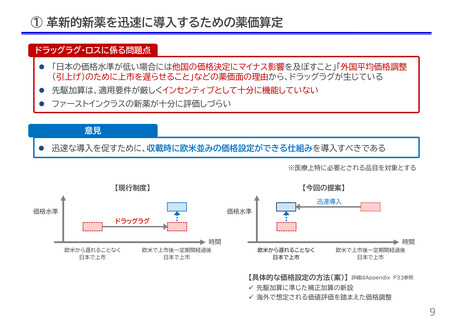
ドラッグラグ・ロスに係る問題点
現行の品目要件では、医療上の必要性が高い医薬品が必ずしも新薬創出等加算の対象とならないこ
とがあり、ドラッグラグ・ロスが多く生じている小児用医薬品なども対象となっていない
現行の企業指標による評価は企業規模の影響を強く受けるため、小規模企業、希少疾病等の専門分
野に特化した企業、日本での事業展開の歴史が浅い外国企業などにとっては、新薬の薬価が維持で
きない。それが日本で上市する魅力をなくしている
意見
【品目要件】
小児用医薬品などの医療上必要性の高い医薬品、およびドラッグラグ・ロス解消に資する日本で早期
上市した品目については、現行の品目要件に追加すべきである
【企業指標・企業区分】
企業指標・企業区分については撤廃し、薬価を維持すべきである
【現行の品目要件】
① 有用性系加算適用品目
② 開発公募品
③ 希少疾病用医薬品
④ 新規作用機序医薬品
⑤ 新規作用機序医薬品から3年以内・3番手以内
⑥ 先駆的医薬品
⑦ 特定用途医薬品
⑧ 薬剤耐性菌の治療薬
追加
〇 小児用医薬品などの医療上必要性の高い医薬品
〇 日本で早期上市した医薬品
【企業要件に係る指標】
A-1) 国内試験(日本を含む国際共同試験を含む)(実施数)(PhaseⅡ以降)
A-2) 新薬収載実績(収載成分数)(過去5年)
A-3) 革新的新薬の収載実績(過去5年)
A-4) 薬剤耐性菌の治療薬の収載実績(過去5年)
A-5) 新型コロナウイルスの治療等に用いる医薬品(過去5年)
B-1) 開発公募品(開発着手数)(過去5年)(B-2分を除く)
B-2) 開発公募品(承認取得数)(過去5年)
C-1) 世界に先駆けた新薬の開発(品目数)(過去5年)
C-2) 特定の用途に係る医薬品の開発(品目数)(過去5年)(A-4分を除く)
11
ドラッグラグ・ロスに係る問題点
現行の品目要件では、医療上の必要性が高い医薬品が必ずしも新薬創出等加算の対象とならないこ
とがあり、ドラッグラグ・ロスが多く生じている小児用医薬品なども対象となっていない
現行の企業指標による評価は企業規模の影響を強く受けるため、小規模企業、希少疾病等の専門分
野に特化した企業、日本での事業展開の歴史が浅い外国企業などにとっては、新薬の薬価が維持で
きない。それが日本で上市する魅力をなくしている
意見
【品目要件】
小児用医薬品などの医療上必要性の高い医薬品、およびドラッグラグ・ロス解消に資する日本で早期
上市した品目については、現行の品目要件に追加すべきである
【企業指標・企業区分】
企業指標・企業区分については撤廃し、薬価を維持すべきである
【現行の品目要件】
① 有用性系加算適用品目
② 開発公募品
③ 希少疾病用医薬品
④ 新規作用機序医薬品
⑤ 新規作用機序医薬品から3年以内・3番手以内
⑥ 先駆的医薬品
⑦ 特定用途医薬品
⑧ 薬剤耐性菌の治療薬
追加
〇 小児用医薬品などの医療上必要性の高い医薬品
〇 日本で早期上市した医薬品
【企業要件に係る指標】
A-1) 国内試験(日本を含む国際共同試験を含む)(実施数)(PhaseⅡ以降)
A-2) 新薬収載実績(収載成分数)(過去5年)
A-3) 革新的新薬の収載実績(過去5年)
A-4) 薬剤耐性菌の治療薬の収載実績(過去5年)
A-5) 新型コロナウイルスの治療等に用いる医薬品(過去5年)
B-1) 開発公募品(開発着手数)(過去5年)(B-2分を除く)
B-2) 開発公募品(承認取得数)(過去5年)
C-1) 世界に先駆けた新薬の開発(品目数)(過去5年)
C-2) 特定の用途に係る医薬品の開発(品目数)(過去5年)(A-4分を除く)
11