よむ、つかう、まなぶ。
【参考資料8】バイオ後続品の品質・安全性・有効性確保のための指針に関する(令和6年1月25日事務連絡) (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_37787.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(第8回 2/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
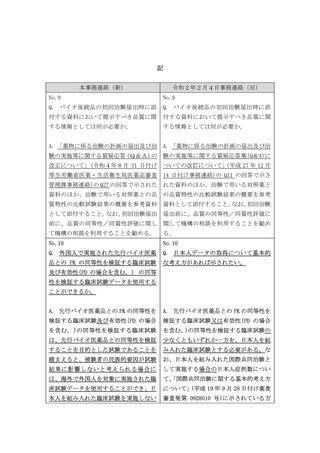
記
本事務連絡(新)
令和2年2月4日事務連絡(旧)
No.9
No.9
Q. バイオ後続品の初回治験届出時に添
Q. バイオ後続品の初回治験届出時に添
付する資料において提示すべき品質に関
付する資料において提示すべき品質に関
する情報としては何が必要か。
する情報としては何が必要か。
A. 「薬物に係る治験の計画の届出及び治 A. 「薬物に係る治験の計画の届出及び治
験の実施等に関する質疑応答(Q&A)の 験の実施等に関する質疑応答集(Q&A)に
改正について」(令和4年8月 31 日付け ついての改訂について」(平成 27 年 12 月
厚生労働省医薬・生活衛生局医薬品審査 14 日付け事務連絡)の Q11 の回答で示さ
管理課事務連絡)の Q27 の回答で示された れた資料のほか、治験で用いる対照薬と
資料のほか、治験で用いる対照薬との品 の品質特性の比較試験結果の概要を参考
質特性の比較試験結果の概要を参考資料 資料として添付すること。なお、初回治験
として添付すること。なお、初回治験届出 届出前に、品質の同等性/同質性評価に
前に、品質の同等性/同質性評価に関し 関して機構の相談を利用することを勧め
て機構の相談を利用することを勧める。
る。
No.10
No.10
Q. 外国人で実施された先行バイオ医薬
Q. 日本人データの取得について基本的
品との PK の同等性を検証する臨床試験
な考え方があれば示されたい。
及び有効性(PD の場合を含む。) の同等
性を検証する臨床試験データを使用する
ことができるか。
A. 先行バイオ医薬品との PK の同等性を
A. 先行バイオ医薬品との PK の同等性を
検証する臨床試験及び有効性(PD の場合
検証する臨床試験又は有効性(PD の場合
を含む。)の同等性を検証する臨床試験
を含む。)の同等性を検証する臨床試験の
は、先行バイオ医薬品との同等性を検証
少なくともいずれか一方を、日本人を組
することを目的とした試験であることを
み入れた臨床試験とする必要がある。な
踏まえると、被験者の民族的要因が試験
お、日本人を組み入れた国際共同治験と
結果に影響しないと考えられる場合に
して実施する場合の日本人症例数につい
は、海外で外国人を対象に実施された臨
て、
「国際共同治験に関する基本的考え方
床試験データを使用することができ、日
について」(平成 19 年 9 月 28 日付け薬食
本人を組み入れた臨床試験を実施しない
審査発第 0928010 号)に示されている方
本事務連絡(新)
令和2年2月4日事務連絡(旧)
No.9
No.9
Q. バイオ後続品の初回治験届出時に添
Q. バイオ後続品の初回治験届出時に添
付する資料において提示すべき品質に関
付する資料において提示すべき品質に関
する情報としては何が必要か。
する情報としては何が必要か。
A. 「薬物に係る治験の計画の届出及び治 A. 「薬物に係る治験の計画の届出及び治
験の実施等に関する質疑応答(Q&A)の 験の実施等に関する質疑応答集(Q&A)に
改正について」(令和4年8月 31 日付け ついての改訂について」(平成 27 年 12 月
厚生労働省医薬・生活衛生局医薬品審査 14 日付け事務連絡)の Q11 の回答で示さ
管理課事務連絡)の Q27 の回答で示された れた資料のほか、治験で用いる対照薬と
資料のほか、治験で用いる対照薬との品 の品質特性の比較試験結果の概要を参考
質特性の比較試験結果の概要を参考資料 資料として添付すること。なお、初回治験
として添付すること。なお、初回治験届出 届出前に、品質の同等性/同質性評価に
前に、品質の同等性/同質性評価に関し 関して機構の相談を利用することを勧め
て機構の相談を利用することを勧める。
る。
No.10
No.10
Q. 外国人で実施された先行バイオ医薬
Q. 日本人データの取得について基本的
品との PK の同等性を検証する臨床試験
な考え方があれば示されたい。
及び有効性(PD の場合を含む。) の同等
性を検証する臨床試験データを使用する
ことができるか。
A. 先行バイオ医薬品との PK の同等性を
A. 先行バイオ医薬品との PK の同等性を
検証する臨床試験及び有効性(PD の場合
検証する臨床試験又は有効性(PD の場合
を含む。)の同等性を検証する臨床試験
を含む。)の同等性を検証する臨床試験の
は、先行バイオ医薬品との同等性を検証
少なくともいずれか一方を、日本人を組
することを目的とした試験であることを
み入れた臨床試験とする必要がある。な
踏まえると、被験者の民族的要因が試験
お、日本人を組み入れた国際共同治験と
結果に影響しないと考えられる場合に
して実施する場合の日本人症例数につい
は、海外で外国人を対象に実施された臨
て、
「国際共同治験に関する基本的考え方
床試験データを使用することができ、日
について」(平成 19 年 9 月 28 日付け薬食
本人を組み入れた臨床試験を実施しない
審査発第 0928010 号)に示されている方