会議資料 (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00035.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第61回 1/29)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
31
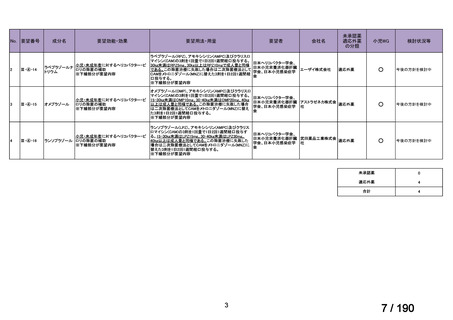
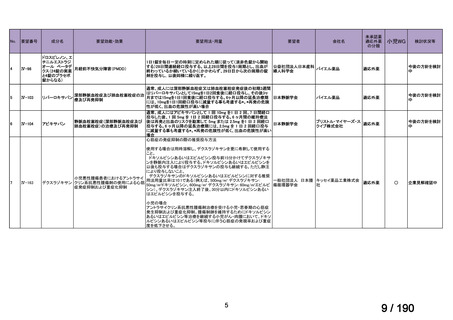
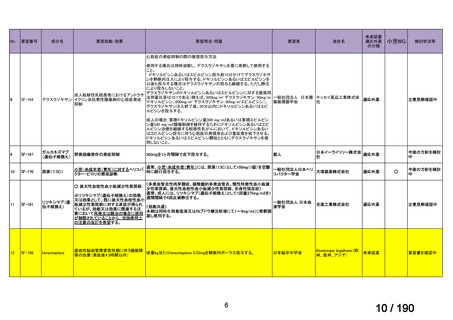
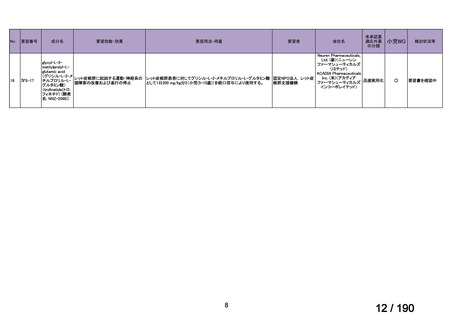
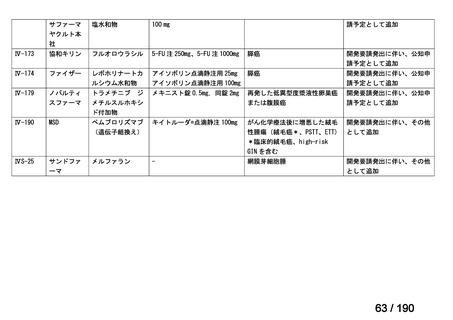
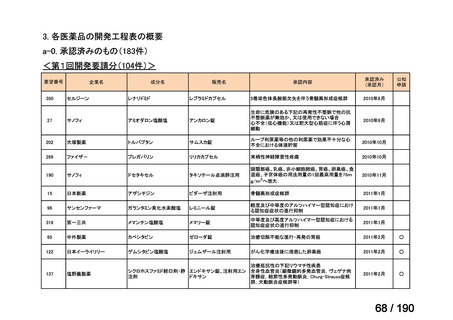
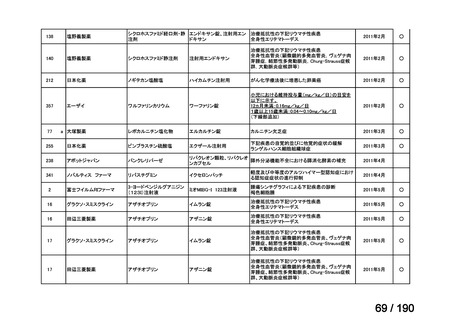
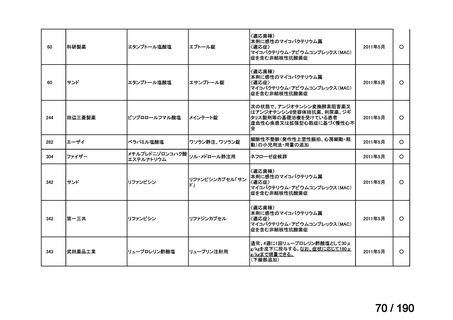
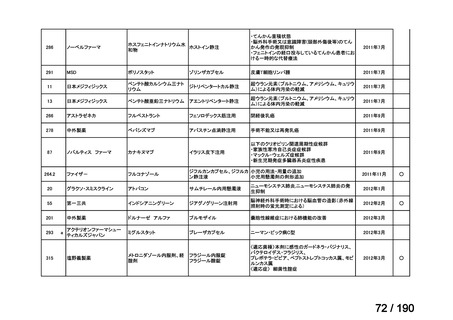
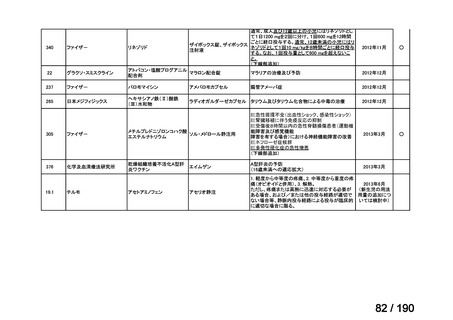
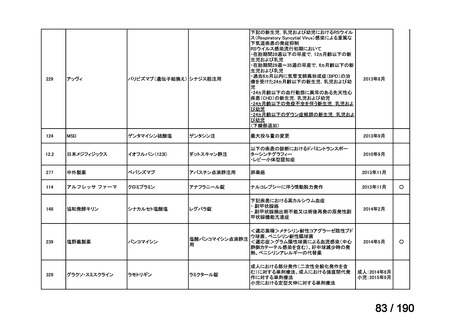
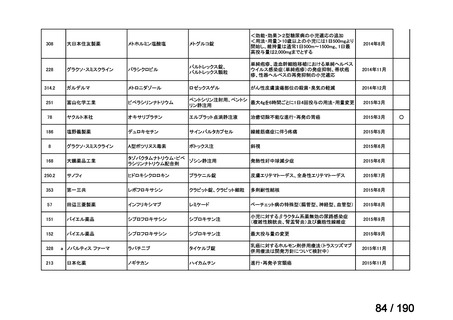
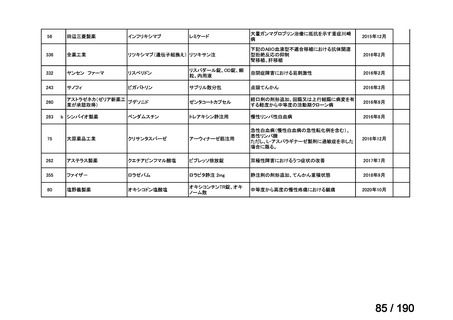
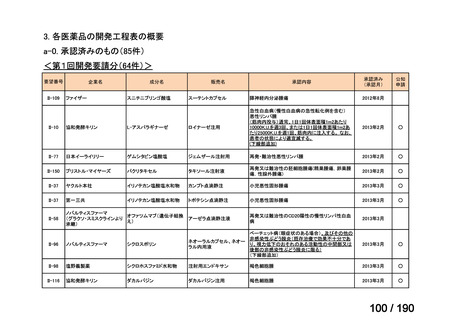
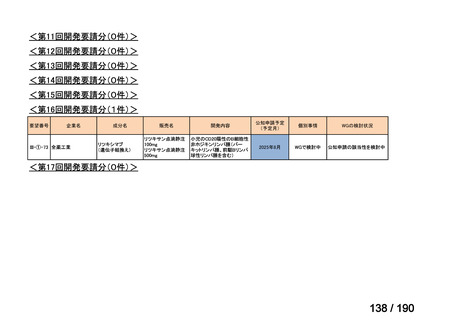
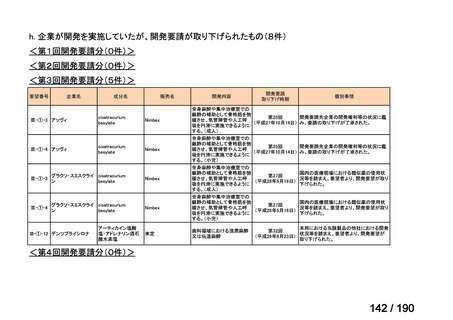
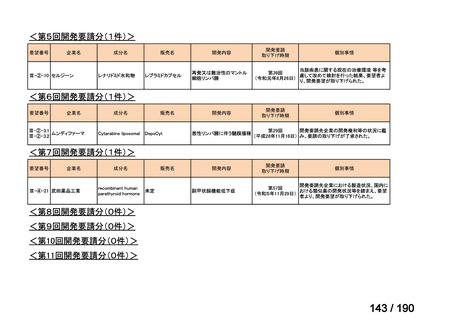
要望番号
成分名
要望効能・効果
要望用法・用量
要望者
会社名
未承認薬
適応外薬
の分類
小児WG
(生後3ヵ月以上)の治療に適応される。 る。腎機能障害のある小児患者におけるデータはない。
エルタペネムは、骨髄炎を合併した糖尿 2.5 血液透析中の患者
病性足感染症では研究されていない[臨 血液透析を受けている成人患者に対して、エルタペネムを1日推奨用
床試験(14)を参照]。
量である500mgを血液透析前6時間以内に投与する場合、血液透析後に
1.3 市中肺炎
150mgを追加投与することが推奨される。エルタペネムを血液透析の6時
エルタペネムは、菌血症、インフルエン 間以上前に投与する場合は、追加投与は必要ない。腹膜透析または血
ザ菌(β-ラクタマーゼ非産生菌のみ)、 液濾過を受けている患者におけるデータはない。血液透析を受けている
モラクセラ・カタラーリスが同時に存在す 小児患者におけるデータはない。
る場合を含む、肺炎球菌(Streptococcus 血清クレアチニンデータのみが入手可能な場合、クレアチニンクリアラ
pneumoniae)(ペニシリン感受性菌のみ) ンスの推定には以下の式 が使用できる。血清クレアチニンは腎機能の
による市中肺炎の成人患者および小児 定常状態を表すはずである。
患者(生後3ヵ月以上)の治療に適応され 男性:(体重(kg)×(140-年齢(歳))/(72)×血清クレアチニン
る。
(mg/100mL)
1.4 腎盂腎炎を含む複雑性尿路感染症 女性:(0.85)×(男性について計算した値)
エルタペネムは、大腸菌(菌血症を合 2.6 肝機能障害のある患者
併している場合を含む)または肺炎桿菌 肝機能障害のある患者では、用量調節の推奨はできない[特定の人口
による腎盂腎炎を含む複雑性尿路感染 における使用(8.7)および臨床薬理学(12.3)を参照]。
症の成人患者および小児患者(生後3ヵ 2.7 投与のための調製及び溶解
月以上)の治療に適応される。
バイアル
1.5 分娩後子宮内膜筋層炎、敗血症性 成人および13歳以上の小児患者
流産、婦人科手術後感染症を含む急性 静脈内投与の調整:
骨盤内感染症
エルタペネムを他の薬剤と混合または混注しないこと。
エルタペネムは、Streptococcus
デキストロース(α-D-グルコース)を含む希釈剤を使用しないこと。
agalactiae、Escherichia coli、
エルタペネムは、必ず投与前に溶解し、更に希釈して使用すること。
Bacteroides fragilis、Porphyromonas
1. エルタペネムの1gバイアルを10mLの注射用水、0.9% 塩化ナトリウム注
asaccharolytica、Peptostreptococcus
射液、または注射用静菌水のいずれかで溶解する。注射器には21ゲー
species、Prevotella biviaに起因する分娩 ジ以下の注射針を用いる。注:針のない静注システムの使用は推奨され
後子宮内膜筋層炎、敗血症性流産、婦 ない。
人科手術後感染症を含む急性骨盤内感 推奨されない。
染症の成人患者および小児患者(生後 2. よく振って溶解したバイアル内容物を直ちに0.9%塩化ナトリウム注射液
3ヵ月以上)の治療に適応される。
50mLに移す。
1.6 待機的大腸手術後の手術部位感染 3. 点滴は、溶解後6時間以内に完了すること。
の予防
筋肉内投与の調整
エルタペネムは、成人において、待機 エルタペネムは、必ず投与前に溶解して使用すること。
的大腸手術後の手術部位感染の予防に 1. エルタペネムの1gバイアルを3.2mLの1.0%塩酸リドカイン注射液 (エピ
適応される。
ネフリンを含まない)に溶解する。バイアルをよく振って溶液にする。
1.7 使用法
2. 直ちにバイアルから内容物を抜き取り、大型の筋肉(臀筋や大腿外側
薬剤耐性菌の発生を抑え、エルタペネ など)に深部筋肉内注射する。
ムや他の抗菌薬の効果を維持するた
3. 溶解した筋肉注射液は、調製後1時間以内に使用すること。注:溶解
め、エルタペネムは、感受性菌が原因で 液は静脈内に投与しないこと。
あることが証明されているか、強く疑われ 生後3ヵ月から12歳までの小児患者
12
16 / 190
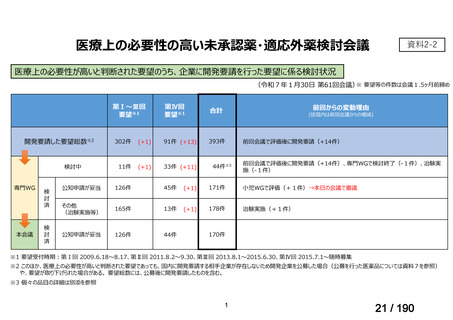
検討状況等