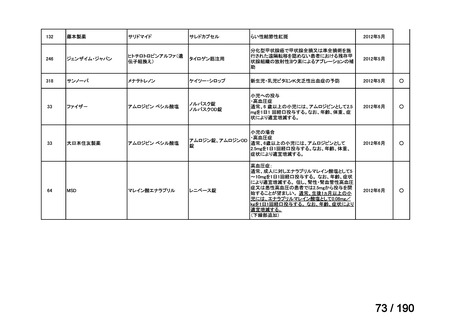
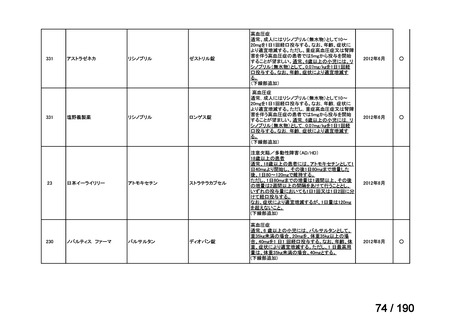
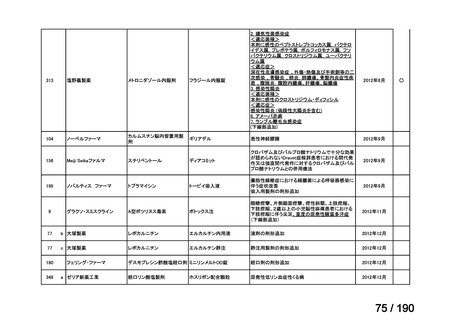
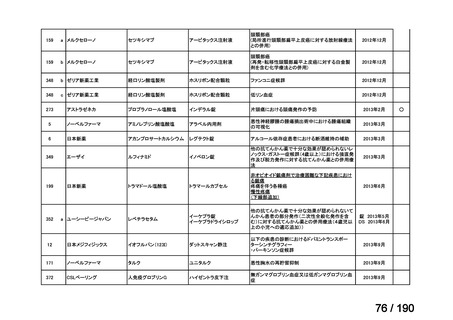
会議資料 (38 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00035.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第61回 1/29)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
代表的な公表論文の概略について、以下に示す。
<海外における報告>
1) Assadi F, et al. Randomized controlled trial to compare safety and efficacy of mycophenolate
vs. cyclosporine after rituximab in children with steroid-resistant nephrotic syndrome.
Pharmacotherapy 2022; 42: 690-6.5)
2~6 歳のステロイド抵抗性ネフローゼ症候群患者 66 例(本薬群 32 例、シクロスポリン
(以下、「CsA」)群 34 例)を対象に、無作為化比較試験が実施された。
リツキシマブ 375 mg/m2 による導入療法後に、本薬 1,000 mg/m2/日又は CsA 5 mg/kg/日が
12 カ月間投与された。
有効性について、主要評価項目とされた 12 カ月時点で完全寛解が認められた被験者の割
合は、本薬群で 81.3%(26/32 例)、CsA 群で 61.7%(21/34 例)であった(p = 0.02、マンホイットニー検定、有意水準両側 5%)。また、寛解までの期間(中央値)は本薬群で 2.64
カ月、CsA 群で 3.4 カ月(ハザード比[95%信頼区間(以下、「CI」)]:0.61[0.74, 0.90])、
初回再発までの期間(中央値)は本薬群で 10.8 カ月、
CsA 群で 8.0 カ月(ハザード比[95%CI]
:
1.12[1.31, 1.54])であり、B 細胞数が回復するまでの期間(中央値)は本薬群 8.6 カ月、
CsA 群 5.2 カ月であった。
安全性について、有害事象の発現割合は本薬群で 59.3%(19/32 例)
、CsA 群 76.4%(26/34
例)であった。また、Grade 3 の有害事象は本薬群で 12.5%(4/32 例)、CsA 群 20.5%(7/34
例)に、Grade 4 の有害事象は本薬群で 9.3%(3/32 例)、CsA 群 14.7%(5/34 例)に認めら
れた。
<日本における報告>
2) Kamei K, et al. Single dose of rituximab for refractory steroid-dependent nephrotic syndrome in
children. Pediatr Nephrol 2009; 24: 1321-8.6)
20 歳未満の難治性 SDNS 患者 12 例を対象に、リツキシマブの有効性及び安全性を検討
する単群試験が実施された。
12 例全例でリツキシマブ 375 mg/m2(最大 500 mg)が単回投与され、そのうち 3 例でリ
ツキシマブ投与後に本薬が投与された。
本薬が投与された 3 例における有効性について、全例でステロイド投与を中止すること
ができ、ステロイド投与中止までの期間(個別値)はそれぞれ 120、123 及び 172 日であっ
た。また、3 例中 2 例では観察期間(1 年)中寛解を維持し、残りの 1 例では 353 日目に再
発が認められた。ステロイドフリー期間(個別値)は、リツキシマブ投与前 6 カ月間でそ
れぞれ 0、0 及び 7 日であったが、リツキシマブ投与後 6 カ月間ではそれぞれ 9、60 及び 64
日であった。
安全性について、試験中止に至る重篤な有害事象は認められなかった。
3) Ito S, et al. Maintenance therapy with mycophenolate mofetil after rituximab in pediatric patients
6
38 / 190