よむ、つかう、まなぶ。
総-2参考1○最適使用推進ガイドラインについて (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00190.html |
| 出典情報 | 中央社会保険医療協議会 総会(第546回 6/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
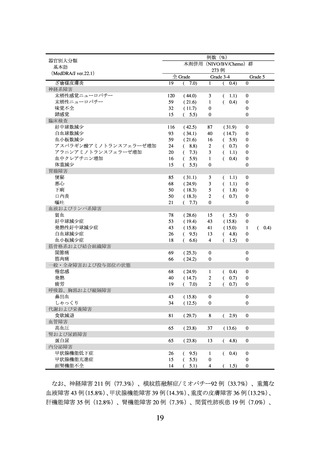
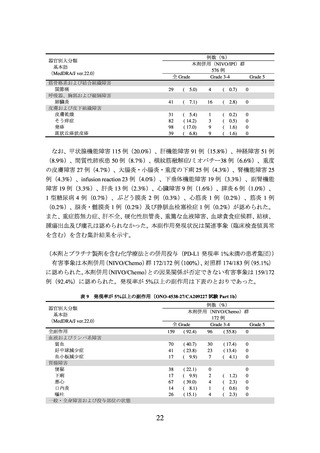
表4 発現率が5%以上の副作用(ONO-4538-06試験)
例数(%)
76 例
全 Grade
Grade 3-4
64
( 84.2)
16
( 21.1)
器官別大分類
基本語
(MedDRA/J ver.17.0)
全副作用
内分泌障害
甲状腺機能低下症
胃腸障害
便秘
下痢
悪心
口内炎
嘔吐
一般・全身障害および投与部位の状態
疲労
倦怠感
発熱
臨床検査
リンパ球数減少
代謝および栄養障害
低ナトリウム血症
食欲減退
神経系障害
浮動性めまい
呼吸器、胸郭および縦隔障害
間質性肺疾患
皮膚および皮下組織障害
そう痒症
発疹
斑状丘疹状皮疹
Grade 5
0
7
( 9.2)
0
0
5
4
8
4
4
( 6.6)
( 5.3)
( 10.5)
( 5.3)
( 5.3)
0
0
0
0
0
0
0
0
0
0
9
11
11
( 11.8)
( 14.5)
( 14.5)
1
0
0
( 1.3)
0
0
0
6
( 7.9)
2
( 2.6)
0
4
11
( 5.3)
( 14.5)
2
1
( 2.6)
( 1.3)
0
0
4
( 5.3)
1
( 1.3)
0
4
( 5.3)
2
( 2.6)
0
6
11
4
( 7.9)
( 14.5)
( 5.3)
1
0
0
( 1.3)
0
0
0
なお、間質性肺疾患4例(5.3%)、大腸炎・重度の下痢5例(6.6%)、神経障害(ギラ
ン・バレー症候群等)10例(13.2%)、肝機能障害5例(6.6%)、甲状腺機能障害10例(13.2%)、
副腎機能障害1例(1.3%)、腎機能障害(尿細管間質性腎炎等)4例(5.3%)及びinfusion
reaction 3例(3.9%)が認められた。また、重度の皮膚障害(皮膚粘膜眼症候群、多形紅
斑、類天疱瘡等)、下垂体機能障害、1型糖尿病、膵炎、重症筋無力症、脳炎・髄膜炎、
ぶどう膜炎及び心筋炎は認められなかった。本副作用発現状況は関連事象(臨床検査値
異常を含む)を含む集計結果を示す。
②海外第Ⅲ相試験(CA209057 試験)(N Engl J Med 2015; 373: 1627-39)
有害事象は本剤群 280/287 例(97.6%)
、ドセタキセル群 265/268 例(98.9%)に認めら
れ、本剤との因果関係が否定できない有害事象は 199/287 例(69.3%)に認められた。
発現率が 5%以上の副作用は下表のとおりであった。
17
例数(%)
76 例
全 Grade
Grade 3-4
64
( 84.2)
16
( 21.1)
器官別大分類
基本語
(MedDRA/J ver.17.0)
全副作用
内分泌障害
甲状腺機能低下症
胃腸障害
便秘
下痢
悪心
口内炎
嘔吐
一般・全身障害および投与部位の状態
疲労
倦怠感
発熱
臨床検査
リンパ球数減少
代謝および栄養障害
低ナトリウム血症
食欲減退
神経系障害
浮動性めまい
呼吸器、胸郭および縦隔障害
間質性肺疾患
皮膚および皮下組織障害
そう痒症
発疹
斑状丘疹状皮疹
Grade 5
0
7
( 9.2)
0
0
5
4
8
4
4
( 6.6)
( 5.3)
( 10.5)
( 5.3)
( 5.3)
0
0
0
0
0
0
0
0
0
0
9
11
11
( 11.8)
( 14.5)
( 14.5)
1
0
0
( 1.3)
0
0
0
6
( 7.9)
2
( 2.6)
0
4
11
( 5.3)
( 14.5)
2
1
( 2.6)
( 1.3)
0
0
4
( 5.3)
1
( 1.3)
0
4
( 5.3)
2
( 2.6)
0
6
11
4
( 7.9)
( 14.5)
( 5.3)
1
0
0
( 1.3)
0
0
0
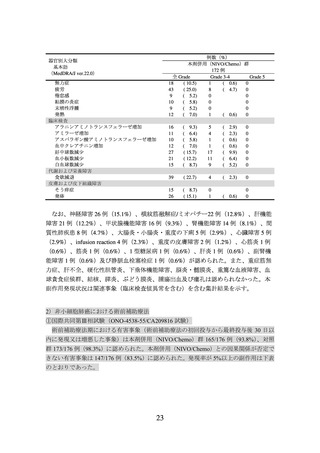
なお、間質性肺疾患4例(5.3%)、大腸炎・重度の下痢5例(6.6%)、神経障害(ギラ
ン・バレー症候群等)10例(13.2%)、肝機能障害5例(6.6%)、甲状腺機能障害10例(13.2%)、
副腎機能障害1例(1.3%)、腎機能障害(尿細管間質性腎炎等)4例(5.3%)及びinfusion
reaction 3例(3.9%)が認められた。また、重度の皮膚障害(皮膚粘膜眼症候群、多形紅
斑、類天疱瘡等)、下垂体機能障害、1型糖尿病、膵炎、重症筋無力症、脳炎・髄膜炎、
ぶどう膜炎及び心筋炎は認められなかった。本副作用発現状況は関連事象(臨床検査値
異常を含む)を含む集計結果を示す。
②海外第Ⅲ相試験(CA209057 試験)(N Engl J Med 2015; 373: 1627-39)
有害事象は本剤群 280/287 例(97.6%)
、ドセタキセル群 265/268 例(98.9%)に認めら
れ、本剤との因果関係が否定できない有害事象は 199/287 例(69.3%)に認められた。
発現率が 5%以上の副作用は下表のとおりであった。
17