よむ、つかう、まなぶ。
資料1-2 ベポタスチンベシル酸塩のリスク評価について[4.5MB] (40 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_35991.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和5年度第12回 10/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
タリオン AR 有害事象調査票
一般調査用
「タリオン AR」のご使用を始めてからあらわれたすべての症状(有害事象)について記入してください。
1) 調査内容は先生ご自身でご記入いただき、薬局・販売店名・管理責任者名欄に署名・捺印をお願い致します。
2) 記載は黒か青のボールペンで記入してください(鉛筆不可)。訂正があれば二重線で消し、訂正印をお願い致します。
修正液は使用しないでください。選択肢のあるものは、あてはまるものにチェック(☑)をつけてください。
(西暦)
イニシャル
名:
姓:
□ 男性
生年月日
□ 女性
又は年齢
性別
(例:田辺花子⇒H.T. )
年
月
日
生年月日をご記入いただけない場合 ⇒
□ 不明
歳
□ 提供不可
【本製品の使用状況】
1日使用量(1回量、1日回数)、使用期間
使用理由
□花粉、ハウスダスト(室
タリオン AR
(通常、1 回 1 錠を 1 日 2 回使用)
□ 1回1錠を1日2回、
□ その他(1回
年
錠を1日
今までに発疹、発赤、かゆみ、かぶ
れ等を起こしたことがありますか?
日~
年
月
日
回、
年
【お客様の背景】
アレルギー歴
月
月
日~
年
月
日)
内塵)などによるアレ
ルギー症状
(症状: □くしゃみ、
□鼻みず、□鼻づまり)
□上記以外(
)
□ なし
□ あり
□ 不明
□ なし
□ あり
□ 不明
□ なし
□ あり
□ 不明
既往歴
今までに大きな病気をしたことがあ
りますか?
合併症
現在治療をしている病気や症状が
ありますか?
併用薬(製品)名
使用期間
併用薬
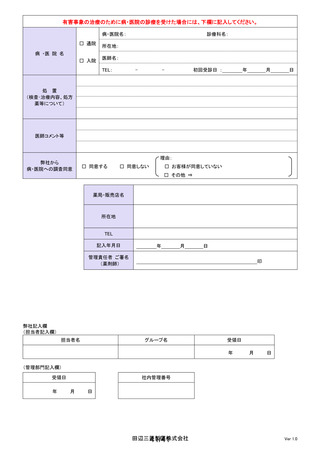
タリオン AR を使用中に、他に使用
していた薬はありましたか?
使用理由
年
月
日~
年
月
日
年
月
日~
年
月
日
年
月
日~
年
月
日
年
月
日~
年
月
日
【有害事象】 (「タリオン AR」使用後にあらわれたすべての症状)
症状が複数ある場合には、それぞれ発現日・発現状況をできるだけ詳しく記入してください。
有害事象名
発現日
□上記有害事象について、受診勧奨した。
日 付(年月日)
転
帰
程
度
参考:添付文書「使用上の注
意」に記載の副作用症状
月
日
症状、発現状況、経過等
転帰日(
年
月
日) :
□ 回復
□ 軽快
□ 未回復
□ 不明
□ 軽度(症状が一時的で軽いもの)
□ 中等度(症状の治療の為に通院を要する程度のもの)
□ 高度(症状が重く、治療の為に入院を要する程度のもの)
□ なし
薬剤師の因果関係
判定及びコメント
年
□ あり
□ 関連不明
コメント:
皮膚(発疹、はれ、じんましん)、消化器(吐き気・嘔吐、胃痛、胃部不快感、舌炎、腹痛、口のかわき、便秘、下痢)、精神神経系(倦怠感、
倦
頭痛、頭重感、めまい、眠気)、泌尿器(血尿、尿量減少、排尿困難)、その他(月経異常、むくみ、動悸、息苦しい、しびれ、味覚異常)
次ページにつづく
田辺三菱製薬株式会社
40/41
Ver 1.0
一般調査用
「タリオン AR」のご使用を始めてからあらわれたすべての症状(有害事象)について記入してください。
1) 調査内容は先生ご自身でご記入いただき、薬局・販売店名・管理責任者名欄に署名・捺印をお願い致します。
2) 記載は黒か青のボールペンで記入してください(鉛筆不可)。訂正があれば二重線で消し、訂正印をお願い致します。
修正液は使用しないでください。選択肢のあるものは、あてはまるものにチェック(☑)をつけてください。
(西暦)
イニシャル
名:
姓:
□ 男性
生年月日
□ 女性
又は年齢
性別
(例:田辺花子⇒H.T. )
年
月
日
生年月日をご記入いただけない場合 ⇒
□ 不明
歳
□ 提供不可
【本製品の使用状況】
1日使用量(1回量、1日回数)、使用期間
使用理由
□花粉、ハウスダスト(室
タリオン AR
(通常、1 回 1 錠を 1 日 2 回使用)
□ 1回1錠を1日2回、
□ その他(1回
年
錠を1日
今までに発疹、発赤、かゆみ、かぶ
れ等を起こしたことがありますか?
日~
年
月
日
回、
年
【お客様の背景】
アレルギー歴
月
月
日~
年
月
日)
内塵)などによるアレ
ルギー症状
(症状: □くしゃみ、
□鼻みず、□鼻づまり)
□上記以外(
)
□ なし
□ あり
□ 不明
□ なし
□ あり
□ 不明
□ なし
□ あり
□ 不明
既往歴
今までに大きな病気をしたことがあ
りますか?
合併症
現在治療をしている病気や症状が
ありますか?
併用薬(製品)名
使用期間
併用薬
タリオン AR を使用中に、他に使用
していた薬はありましたか?
使用理由
年
月
日~
年
月
日
年
月
日~
年
月
日
年
月
日~
年
月
日
年
月
日~
年
月
日
【有害事象】 (「タリオン AR」使用後にあらわれたすべての症状)
症状が複数ある場合には、それぞれ発現日・発現状況をできるだけ詳しく記入してください。
有害事象名
発現日
□上記有害事象について、受診勧奨した。
日 付(年月日)
転
帰
程
度
参考:添付文書「使用上の注
意」に記載の副作用症状
月
日
症状、発現状況、経過等
転帰日(
年
月
日) :
□ 回復
□ 軽快
□ 未回復
□ 不明
□ 軽度(症状が一時的で軽いもの)
□ 中等度(症状の治療の為に通院を要する程度のもの)
□ 高度(症状が重く、治療の為に入院を要する程度のもの)
□ なし
薬剤師の因果関係
判定及びコメント
年
□ あり
□ 関連不明
コメント:
皮膚(発疹、はれ、じんましん)、消化器(吐き気・嘔吐、胃痛、胃部不快感、舌炎、腹痛、口のかわき、便秘、下痢)、精神神経系(倦怠感、
倦
頭痛、頭重感、めまい、眠気)、泌尿器(血尿、尿量減少、排尿困難)、その他(月経異常、むくみ、動悸、息苦しい、しびれ、味覚異常)
次ページにつづく
田辺三菱製薬株式会社
40/41
Ver 1.0