よむ、つかう、まなぶ。
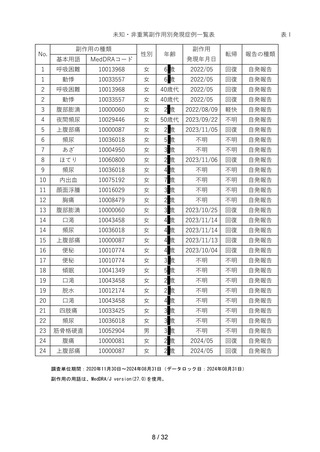
資料1-2 セイヨウトチノキ種子エキスのリスク評価について[4.6MB] (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44431.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会安全対策調査会(令和6年度第8回 10/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
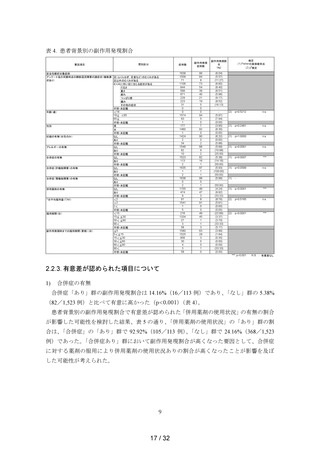
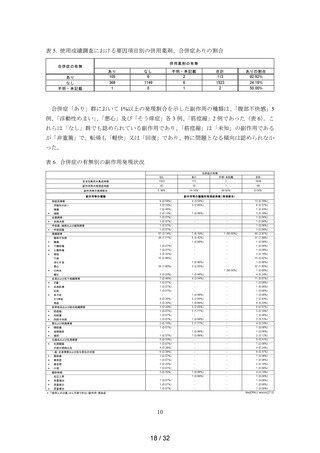
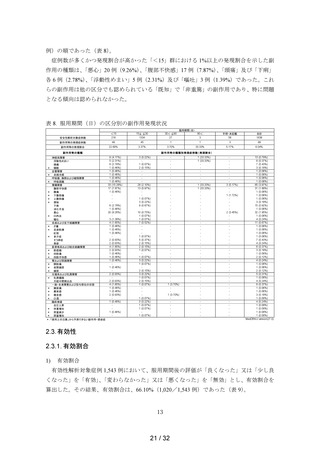
表 5. 使用成績調査における要因項目別の併用薬剤、合併症ありの割合
併用薬剤の有無
合併症の有無
あり
なし
不明・未記載
あり
105
なし
6
不明・未記載
2
合計
113
ありの割合
92.92%
368
1
1149
0
6
1
1523
2
24.16%
50.00%
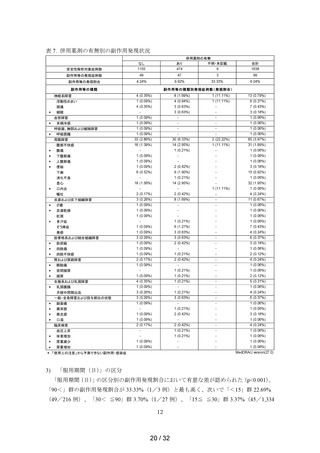
合併症「あり」群において 1%以上の発現割合を示した副作用の種類は、
「腹部不快感」5
例、
「浮動性めまい」、
「悪心」及び「そう痒症」各 3 例、
「筋痙縮」2 例であった(表 6)。こ
れらは「なし」群でも認められている副作用であり、
「筋痙縮」は「未知」の副作用である
が「非重篤」で、転帰も「軽快」又は「回復」であり、特に問題となる傾向は認められなか
った。
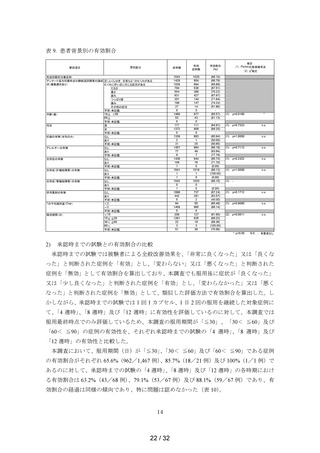
表 6. 合併症の有無別の副作用発現状況
合併症の有無
安全性解析対象症例数
なし
1523
*
*
不明・未記載
2
合計
1638
副作用等の発現症例数
82
16
1
99
副作用等の発現割合
5.38%
14.16%
50.00%
6.04%
副作用等の種類
*
あり
113
副作用等の種類別発現症例数( 発現割合)
神経系障害
9 (0.59%)
4 (3.54%)
-
13 (0.79%)
浮動性めまい
3 (0.20%)
3 (2.65%)
-
6 (0.37%)
頭痛
7 (0.46%)
傾眠
2 (0.13%)
血管障害
1 (0.07%)
末梢冷感
1 (0.07%)
呼吸器、胸郭および縦隔障害
1 (0.07%)
-
-
7 (0.43%)
-
3 (0.18%)
-
-
1 (0.06%)
-
-
1 (0.06%)
-
-
1 (0.88%)
呼吸困難
1 (0.07%)
胃腸障害
57 (3.74%)
7 (6.19%)
腹部不快感
26 (1.71%)
5 (4.42%)
-
1 (0.06%)
1 (0.06%)
65 (3.97%)
31 (1.89%)
腹痛
-
1 (0.06%)
*
下腹部痛
1 (0.07%)
-
-
1 (0.06%)
*
上腹部痛
1 (0.07%)
-
-
1 (0.06%)
*
便秘
3 (0.20%)
-
-
3 (0.18%)
下痢
15 (0.98%)
-
-
15 (0.92%)
消化不良
*
口内炎
29 (1.90%)
-
1 (0.88%)
1 (50.00%)
*
悪心
-
-
1 (0.88%)
-
1 (0.06%)
3 (2.65%)
-
32 (1.95%)
-
1 (50.00%)
1 (0.06%)
嘔吐
3 (0.20%)
1 (0.88%)
-
4 (0.24%)
皮膚および皮下組織障害
7 (0.46%)
4 (3.54%)
-
11 (0.67%)
*
ざ瘡
1 (0.07%)
-
-
1 (0.06%)
*
皮膚乾燥
1 (0.07%)
-
-
1 (0.06%)
紅斑
1 (0.07%)
-
-
1 (0.06%)
*
多汗症
-
1 (0.88%)
-
1 (0.06%)
そう痒症
4 (0.26%)
3 (2.65%)
-
7 (0.43%)
発疹
3 (0.20%)
1 (0.88%)
-
4 (0.24%)
筋骨格系および結合組織障害
3 (0.20%)
3 (2.65%)
-
6 (0.37%)
*
筋痙縮
1 (0.07%)
2 (1.77%)
-
3 (0.18%)
*
四肢痛
1 (0.07%)
*
四肢不快感
1 (0.07%)
腎および尿路障害
2 (0.13%)
*
膀胱痛
1 (0.07%)
*
夜間頻尿
*
頻尿
1 (0.07%)
生殖系および乳房障害
5 (0.33%)
乳房腫脹
1 (0.07%)
月経中間期出血
4 (0.26%)
-
1 (0.06%)
1 (0.88%)
-
2 (0.12%)
2 (1.77%)
-
4 (0.24%)
-
1 (0.06%)
1 (0.88%)
-
1 (0.06%)
1 (0.88%)
-
2 (0.12%)
-
-
5 (0.31%)
-
-
1 (0.06%)
-
-
4 (0.24%)
一般・全身障害および投与部位の状態
6 (0.39%)
-
-
6 (0.37%)
*
顔面痛
1 (0.07%)
-
-
1 (0.06%)
*
異常感
1 (0.07%)
-
-
1 (0.06%)
*
倦怠感
3 (0.20%)
-
-
3 (0.18%)
*
口渇
1 (0.07%)
-
-
1 (0.06%)
臨床検査
3 (0.20%)
-
4 (0.24%)
*
-
-
-
1 (0.06%)
*
体重増加
1 (0.07%)
-
-
1 (0.06%)
*
尿量減少
1 (0.07%)
-
-
*
尿量増加
1 (0.07%)
-
-
血圧上昇
-
1 (0.88%)
1 (0.88%)
1 (0.06%)
1 (0.06%)
MedDRA/J version(27.0)
*:「使用上の注意」から予測できない副作用・感染症
10
18 / 32
併用薬剤の有無
合併症の有無
あり
なし
不明・未記載
あり
105
なし
6
不明・未記載
2
合計
113
ありの割合
92.92%
368
1
1149
0
6
1
1523
2
24.16%
50.00%
合併症「あり」群において 1%以上の発現割合を示した副作用の種類は、
「腹部不快感」5
例、
「浮動性めまい」、
「悪心」及び「そう痒症」各 3 例、
「筋痙縮」2 例であった(表 6)。こ
れらは「なし」群でも認められている副作用であり、
「筋痙縮」は「未知」の副作用である
が「非重篤」で、転帰も「軽快」又は「回復」であり、特に問題となる傾向は認められなか
った。
表 6. 合併症の有無別の副作用発現状況
合併症の有無
安全性解析対象症例数
なし
1523
*
*
不明・未記載
2
合計
1638
副作用等の発現症例数
82
16
1
99
副作用等の発現割合
5.38%
14.16%
50.00%
6.04%
副作用等の種類
*
あり
113
副作用等の種類別発現症例数( 発現割合)
神経系障害
9 (0.59%)
4 (3.54%)
-
13 (0.79%)
浮動性めまい
3 (0.20%)
3 (2.65%)
-
6 (0.37%)
頭痛
7 (0.46%)
傾眠
2 (0.13%)
血管障害
1 (0.07%)
末梢冷感
1 (0.07%)
呼吸器、胸郭および縦隔障害
1 (0.07%)
-
-
7 (0.43%)
-
3 (0.18%)
-
-
1 (0.06%)
-
-
1 (0.06%)
-
-
1 (0.88%)
呼吸困難
1 (0.07%)
胃腸障害
57 (3.74%)
7 (6.19%)
腹部不快感
26 (1.71%)
5 (4.42%)
-
1 (0.06%)
1 (0.06%)
65 (3.97%)
31 (1.89%)
腹痛
-
1 (0.06%)
*
下腹部痛
1 (0.07%)
-
-
1 (0.06%)
*
上腹部痛
1 (0.07%)
-
-
1 (0.06%)
*
便秘
3 (0.20%)
-
-
3 (0.18%)
下痢
15 (0.98%)
-
-
15 (0.92%)
消化不良
*
口内炎
29 (1.90%)
-
1 (0.88%)
1 (50.00%)
*
悪心
-
-
1 (0.88%)
-
1 (0.06%)
3 (2.65%)
-
32 (1.95%)
-
1 (50.00%)
1 (0.06%)
嘔吐
3 (0.20%)
1 (0.88%)
-
4 (0.24%)
皮膚および皮下組織障害
7 (0.46%)
4 (3.54%)
-
11 (0.67%)
*
ざ瘡
1 (0.07%)
-
-
1 (0.06%)
*
皮膚乾燥
1 (0.07%)
-
-
1 (0.06%)
紅斑
1 (0.07%)
-
-
1 (0.06%)
*
多汗症
-
1 (0.88%)
-
1 (0.06%)
そう痒症
4 (0.26%)
3 (2.65%)
-
7 (0.43%)
発疹
3 (0.20%)
1 (0.88%)
-
4 (0.24%)
筋骨格系および結合組織障害
3 (0.20%)
3 (2.65%)
-
6 (0.37%)
*
筋痙縮
1 (0.07%)
2 (1.77%)
-
3 (0.18%)
*
四肢痛
1 (0.07%)
*
四肢不快感
1 (0.07%)
腎および尿路障害
2 (0.13%)
*
膀胱痛
1 (0.07%)
*
夜間頻尿
*
頻尿
1 (0.07%)
生殖系および乳房障害
5 (0.33%)
乳房腫脹
1 (0.07%)
月経中間期出血
4 (0.26%)
-
1 (0.06%)
1 (0.88%)
-
2 (0.12%)
2 (1.77%)
-
4 (0.24%)
-
1 (0.06%)
1 (0.88%)
-
1 (0.06%)
1 (0.88%)
-
2 (0.12%)
-
-
5 (0.31%)
-
-
1 (0.06%)
-
-
4 (0.24%)
一般・全身障害および投与部位の状態
6 (0.39%)
-
-
6 (0.37%)
*
顔面痛
1 (0.07%)
-
-
1 (0.06%)
*
異常感
1 (0.07%)
-
-
1 (0.06%)
*
倦怠感
3 (0.20%)
-
-
3 (0.18%)
*
口渇
1 (0.07%)
-
-
1 (0.06%)
臨床検査
3 (0.20%)
-
4 (0.24%)
*
-
-
-
1 (0.06%)
*
体重増加
1 (0.07%)
-
-
1 (0.06%)
*
尿量減少
1 (0.07%)
-
-
*
尿量増加
1 (0.07%)
-
-
血圧上昇
-
1 (0.88%)
1 (0.88%)
1 (0.06%)
1 (0.06%)
MedDRA/J version(27.0)
*:「使用上の注意」から予測できない副作用・感染症
10
18 / 32