よむ、つかう、まなぶ。
資料1-2 セイヨウトチノキ種子エキスのリスク評価について[4.6MB] (22 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44431.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会安全対策調査会(令和6年度第8回 10/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
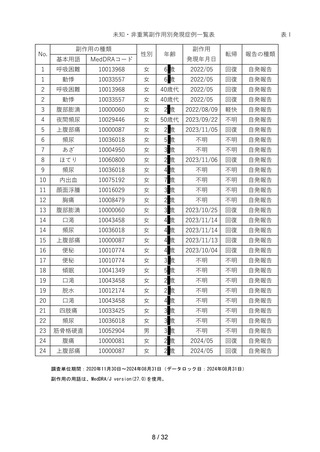
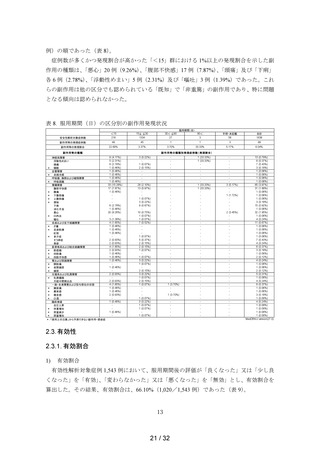
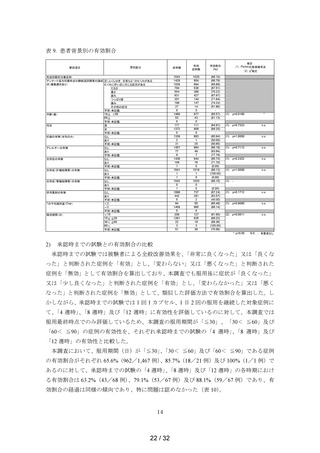
表 9. 患者背景別の有効割合
要因項目
層別区分
有効性解析対象症例
アンケート協力同意時点の静脈還流障害の諸症 足(ふくらはぎ,足首など)のむくみがある
状(複数選択あり)
むくみに伴い足に生じる症状がある
だるさ
重さ
疲れ
つっぱり感
痛み
その他の症状
不明・未記載
18≦ <65
年齢(歳)
65≦
不明・未記載
性別
男
女
不明・未記載
なし
妊娠の有無(女性のみ)
あり
不明・未記載
なし
アレルギーの有無
あり
不明・未記載
なし
合併症の有無
あり
不明・未記載
なし
合併症(肝機能障害)の有無
あり
不明・未記載
なし
合併症(腎機能障害)の有無
あり
不明・未記載
なし
併用薬剤の有無
あり
不明・未記載
1日平均服用量(Cap)
<2
=2
不明・未記載
<15
服用期間(日)
15≦ ≦30
30< ≦90
90<
不明・未記載
症例数
有効
症例数
有効割合
(%)
1543
1429
1038
794
554
631
201
198
27
0
1490
53
0
171
1372
0
1339
2
31
1457
77
9
1436
106
1
1541
1
1
1542
0
1
1096
442
5
84
1459
0
206
1261
22
3
51
1020
954
694
536
389
427
144
147
14
0
977
43
0
111
909
0
883
1
25
964
49
7
944
76
0
1019
1
0
1020
0
0
737
281
2
55
965
0
127
835
19
3
36
(66.10)
(66.76)
(66.86)
(67.51)
(70.22)
(67.67)
(71.64)
(74.24)
(51.85)
(65.57)
(81.13)
(64.91)
(66.25)
(65.94)
(50.00)
(80.65)
(66.16)
(63.64)
(77.78)
(65.74)
(71.70)
(0.00)
(66.13)
(100.00)
(0.00)
(66.15)
(0.00)
(67.24)
(63.57)
(40.00)
(65.48)
(66.14)
(61.65)
(66.22)
(86.36)
(100.00)
(70.59)
検定
(1 )Fisherの直接確率法
2
(2)χ 検定
(1)
p=0.0180
*
(1)
p=0.7323
n.s.
(1)
p=1.0000
n.s.
(1)
p=0.7112
n.s.
(1)
p=0.2422
n.s.
(1)
p=1.0000
n.s.
(1)
-
(1)
p=0.1712
n.s.
(1)
p=0.9060
n.s.
(2)
p=0.0611
n.s.
*:p<0.05
2)
N.S. : 有意差なし
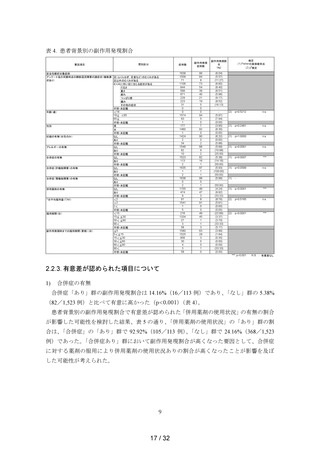
承認時までの試験との有効割合の比較
承認時までの試験では被験者による全般改善効果を、
「非常に良くなった」又は「良くな
った」と判断された症例を「有効」とし、
「変わらない」又は「悪くなった」と判断された
症例を「無効」として有効割合を算出しており、本調査でも服用後に症状が「良くなった」
又は「少し良くなった」と判断された症例を「有効」とし、
「変わらなかった」又は「悪く
なった」と判断された症例を「無効」として、類似した評価方法で有効割合を算出した。し
かしながら、承認時までの試験では 1 回 1 カプセル、1 日 2 回の服用を継続した対象症例に
て、「4 週時」、「8 週時」及び「12 週時」に有効性を評価しているのに対して、本調査では
服用最終時点でのみ評価しているため、本調査の服用期間が「≦30」、「30< ≦60」及び
「60< ≦90」の症例の有効性を、それぞれ承認時までの試験の「4 週時」、「8 週時」及び
「12 週時」の有効性と比較した。
本調査において、服用期間(日)が「≦30」、
「30< ≦60」及び「60< ≦90」である症例
の有効割合がそれぞれ 65.6%(962/1,467 例)、85.7%(18/21 例)及び 100%(1/1 例)で
「8 週時」及び「12 週時」の各時期におけ
あるのに対して、承認時までの試験の「4 週時」、
る有効割合は 63.2%(43/68 例)、79.1%(53/67 例)及び 88.1%(59/67 例)であり、有
効割合の経過は同様の傾向であり、特に問題は認めなかった(表 10)
。
14
22 / 32
要因項目
層別区分
有効性解析対象症例
アンケート協力同意時点の静脈還流障害の諸症 足(ふくらはぎ,足首など)のむくみがある
状(複数選択あり)
むくみに伴い足に生じる症状がある
だるさ
重さ
疲れ
つっぱり感
痛み
その他の症状
不明・未記載
18≦ <65
年齢(歳)
65≦
不明・未記載
性別
男
女
不明・未記載
なし
妊娠の有無(女性のみ)
あり
不明・未記載
なし
アレルギーの有無
あり
不明・未記載
なし
合併症の有無
あり
不明・未記載
なし
合併症(肝機能障害)の有無
あり
不明・未記載
なし
合併症(腎機能障害)の有無
あり
不明・未記載
なし
併用薬剤の有無
あり
不明・未記載
1日平均服用量(Cap)
<2
=2
不明・未記載
<15
服用期間(日)
15≦ ≦30
30< ≦90
90<
不明・未記載
症例数
有効
症例数
有効割合
(%)
1543
1429
1038
794
554
631
201
198
27
0
1490
53
0
171
1372
0
1339
2
31
1457
77
9
1436
106
1
1541
1
1
1542
0
1
1096
442
5
84
1459
0
206
1261
22
3
51
1020
954
694
536
389
427
144
147
14
0
977
43
0
111
909
0
883
1
25
964
49
7
944
76
0
1019
1
0
1020
0
0
737
281
2
55
965
0
127
835
19
3
36
(66.10)
(66.76)
(66.86)
(67.51)
(70.22)
(67.67)
(71.64)
(74.24)
(51.85)
(65.57)
(81.13)
(64.91)
(66.25)
(65.94)
(50.00)
(80.65)
(66.16)
(63.64)
(77.78)
(65.74)
(71.70)
(0.00)
(66.13)
(100.00)
(0.00)
(66.15)
(0.00)
(67.24)
(63.57)
(40.00)
(65.48)
(66.14)
(61.65)
(66.22)
(86.36)
(100.00)
(70.59)
検定
(1 )Fisherの直接確率法
2
(2)χ 検定
(1)
p=0.0180
*
(1)
p=0.7323
n.s.
(1)
p=1.0000
n.s.
(1)
p=0.7112
n.s.
(1)
p=0.2422
n.s.
(1)
p=1.0000
n.s.
(1)
-
(1)
p=0.1712
n.s.
(1)
p=0.9060
n.s.
(2)
p=0.0611
n.s.
*:p<0.05
2)
N.S. : 有意差なし
承認時までの試験との有効割合の比較
承認時までの試験では被験者による全般改善効果を、
「非常に良くなった」又は「良くな
った」と判断された症例を「有効」とし、
「変わらない」又は「悪くなった」と判断された
症例を「無効」として有効割合を算出しており、本調査でも服用後に症状が「良くなった」
又は「少し良くなった」と判断された症例を「有効」とし、
「変わらなかった」又は「悪く
なった」と判断された症例を「無効」として、類似した評価方法で有効割合を算出した。し
かしながら、承認時までの試験では 1 回 1 カプセル、1 日 2 回の服用を継続した対象症例に
て、「4 週時」、「8 週時」及び「12 週時」に有効性を評価しているのに対して、本調査では
服用最終時点でのみ評価しているため、本調査の服用期間が「≦30」、「30< ≦60」及び
「60< ≦90」の症例の有効性を、それぞれ承認時までの試験の「4 週時」、「8 週時」及び
「12 週時」の有効性と比較した。
本調査において、服用期間(日)が「≦30」、
「30< ≦60」及び「60< ≦90」である症例
の有効割合がそれぞれ 65.6%(962/1,467 例)、85.7%(18/21 例)及び 100%(1/1 例)で
「8 週時」及び「12 週時」の各時期におけ
あるのに対して、承認時までの試験の「4 週時」、
る有効割合は 63.2%(43/68 例)、79.1%(53/67 例)及び 88.1%(59/67 例)であり、有
効割合の経過は同様の傾向であり、特に問題は認めなかった(表 10)
。
14
22 / 32