よむ、つかう、まなぶ。
【資料1】 これまでの意見及び論点案について (64 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_28536.html |
| 出典情報 | 医薬品の迅速・安定供給実現に向けた総合対策に関する有識者検討会(第3回 10/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
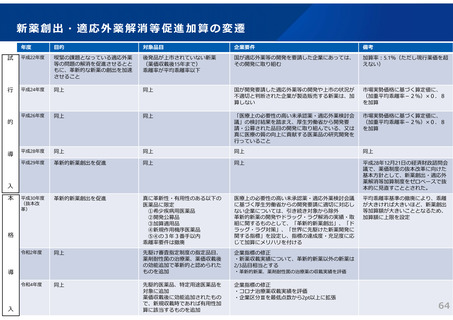
新薬創出・適応外薬解消等促進加算の変遷
年度
目的
対象品目
企業要件
備考
試
平成22年度
喫緊の課題となっている適応外薬
等の問題の解消を促進させるとと
もに、革新的な新薬の創出を加速
させること
後発品が上市されていない新薬
(薬価収載後15年まで)
乖離率が平均乖離率以下
国が適応外薬等の開発を要請した企業にあっては、
その開発に取り組む
加算率:5.1%(ただし現行薬価を超
えない)
行
平成24年度
同上
同上
国が開発要請した適応外薬等の開発や上市の状況が
不適切と判断された企業が製造販売する新薬は、加
算しない
市場実勢価格に基づく算定値に、
(加重平均乖離率-2%)×0.8
を加算
平成26年度
同上
同上
「医療上の必要性の高い未承認薬・適応外薬検討会
議」の検討結果を踏まえ、厚生労働省から開発要
請・公募された品目の開発に取り組んでいる、又は
真に医療の質の向上に貢献する医薬品の研究開発を
行っていること
市場実勢価格に基づく算定値に、
(加重平均乖離率-2%)×0.8
を加算
平成28年度
同上
同上
同上
同上
平成29年度
革新的新薬創出を促進
同上
同上
平成28年12月21日の経済財政諮問会
議で、薬価制度の抜本改革に向けた
基本方針として、新薬創出・適応外
薬解消等加算制度をゼロベースで抜
本的に見直すこととされた。
平成30年度
(抜本改
革)
革新的新薬創出を促進
真に革新性・有用性のある以下の
医薬品に限定
①希少疾病用医薬品
②開発公募品
③加算適用品
④新規作用機序医薬品
⑤④の3年3番手以内
乖離率要件は撤廃
医療上の必要性の高い未承認薬・適応外薬検討会議
に基づく厚生労働省からの開発要請に適切に対応し
ない企業については、引き続き対象から除外
革新的新薬の開発やドラッグ・ラグ解消の実績・取
組に関するものとして、「革新的新薬創出」、「ド
ラッグ・ラグ対策」、「世界に先駆けた新薬開発に
関する指標」を設定し、指標の達成度・充足度に応
じて加算にメリハリを付ける
平均乖離率基準の撤廃により、乖離
が大きければ大きいほど、新薬創出
等加算額が大きいこととなるため、
加算額に上限を設定
令和2年度
同上
先駆け審査指定制度の指定品目、
薬剤耐性菌の治療薬、薬価収載後
の効能追加で革新的と認められた
ものを追加
企業指標の修正
・新薬収載実績について、革新的新薬以外の新薬は
2/3品目相当とする
・革新的新薬、薬剤耐性菌の治療薬の収載実績を評価
令和4年度
同上
先駆的医薬品、特定用途医薬品を
対象に追加
薬価収載後に効能追加されたもの
で、新規収載時であれば有用性加
算に該当するものを追加
企業指標の修正
・コロナ治療薬収載実績を評価
・企業区分Ⅲを最低点数から2pt以上に拡張
的
導
入
本
格
導
入
64 64
年度
目的
対象品目
企業要件
備考
試
平成22年度
喫緊の課題となっている適応外薬
等の問題の解消を促進させるとと
もに、革新的な新薬の創出を加速
させること
後発品が上市されていない新薬
(薬価収載後15年まで)
乖離率が平均乖離率以下
国が適応外薬等の開発を要請した企業にあっては、
その開発に取り組む
加算率:5.1%(ただし現行薬価を超
えない)
行
平成24年度
同上
同上
国が開発要請した適応外薬等の開発や上市の状況が
不適切と判断された企業が製造販売する新薬は、加
算しない
市場実勢価格に基づく算定値に、
(加重平均乖離率-2%)×0.8
を加算
平成26年度
同上
同上
「医療上の必要性の高い未承認薬・適応外薬検討会
議」の検討結果を踏まえ、厚生労働省から開発要
請・公募された品目の開発に取り組んでいる、又は
真に医療の質の向上に貢献する医薬品の研究開発を
行っていること
市場実勢価格に基づく算定値に、
(加重平均乖離率-2%)×0.8
を加算
平成28年度
同上
同上
同上
同上
平成29年度
革新的新薬創出を促進
同上
同上
平成28年12月21日の経済財政諮問会
議で、薬価制度の抜本改革に向けた
基本方針として、新薬創出・適応外
薬解消等加算制度をゼロベースで抜
本的に見直すこととされた。
平成30年度
(抜本改
革)
革新的新薬創出を促進
真に革新性・有用性のある以下の
医薬品に限定
①希少疾病用医薬品
②開発公募品
③加算適用品
④新規作用機序医薬品
⑤④の3年3番手以内
乖離率要件は撤廃
医療上の必要性の高い未承認薬・適応外薬検討会議
に基づく厚生労働省からの開発要請に適切に対応し
ない企業については、引き続き対象から除外
革新的新薬の開発やドラッグ・ラグ解消の実績・取
組に関するものとして、「革新的新薬創出」、「ド
ラッグ・ラグ対策」、「世界に先駆けた新薬開発に
関する指標」を設定し、指標の達成度・充足度に応
じて加算にメリハリを付ける
平均乖離率基準の撤廃により、乖離
が大きければ大きいほど、新薬創出
等加算額が大きいこととなるため、
加算額に上限を設定
令和2年度
同上
先駆け審査指定制度の指定品目、
薬剤耐性菌の治療薬、薬価収載後
の効能追加で革新的と認められた
ものを追加
企業指標の修正
・新薬収載実績について、革新的新薬以外の新薬は
2/3品目相当とする
・革新的新薬、薬剤耐性菌の治療薬の収載実績を評価
令和4年度
同上
先駆的医薬品、特定用途医薬品を
対象に追加
薬価収載後に効能追加されたもの
で、新規収載時であれば有用性加
算に該当するものを追加
企業指標の修正
・コロナ治療薬収載実績を評価
・企業区分Ⅲを最低点数から2pt以上に拡張
的
導
入
本
格
導
入
64 64