よむ、つかう、まなぶ。
別紙4○先進医療Bに係る新規技術の科学的評価等について (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00066.html |
| 出典情報 | 先進医療会議(第129回 2/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
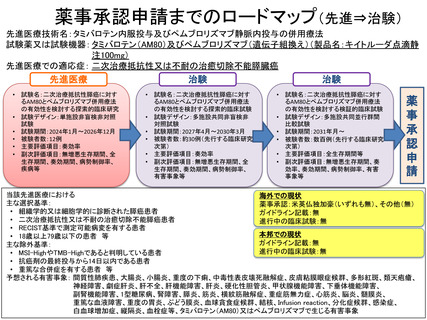
先進医療技術の名称:タミバロテン内服投与及びペムブロリズマブ静脈内投与の併用療法
対象患者
•
二次治療抵抗性(2種類の標準的治療に対して抵抗性)又は不耐の治癒切除不能膵癌患者
全体スケジュール
治療期(21日を1コースとし、8コース)
Day 1
2コース
Day 22
3コース
Day 43
4コース
Day 64
~
~
投与開始日
1コース
前観察期
同意取得
8コース
Day 148
それぞれのコース開始:AM80(タミバロテン)+ペムブロリズマブを順次投与
追跡調査期間
1年間
Day 169
• 画像検査は適宜評価
評価項目
1.
2.
3.
主要評価項目
•
奏効率(RR)
副次評価項目
① 無増悪生存期間(PFS)
② 全生存期間(OS)
③ 奏効期間(DOR)及び完全奏効期間
④ 病勢制御率(DCR)
安全性評価項目
① 特定臨床研究の実施に起因するものと疑われる疾病、障害もしくは死亡又は感染症(疾病等)
② バイタルサイン・臨床検査値・酸素飽和度
膵癌に対し、AM80(タミバロテン)が免疫チェックポイント阻害剤の感受性を増強させることを確認
46
対象患者
•
二次治療抵抗性(2種類の標準的治療に対して抵抗性)又は不耐の治癒切除不能膵癌患者
全体スケジュール
治療期(21日を1コースとし、8コース)
Day 1
2コース
Day 22
3コース
Day 43
4コース
Day 64
~
~
投与開始日
1コース
前観察期
同意取得
8コース
Day 148
それぞれのコース開始:AM80(タミバロテン)+ペムブロリズマブを順次投与
追跡調査期間
1年間
Day 169
• 画像検査は適宜評価
評価項目
1.
2.
3.
主要評価項目
•
奏効率(RR)
副次評価項目
① 無増悪生存期間(PFS)
② 全生存期間(OS)
③ 奏効期間(DOR)及び完全奏効期間
④ 病勢制御率(DCR)
安全性評価項目
① 特定臨床研究の実施に起因するものと疑われる疾病、障害もしくは死亡又は感染症(疾病等)
② バイタルサイン・臨床検査値・酸素飽和度
膵癌に対し、AM80(タミバロテン)が免疫チェックポイント阻害剤の感受性を増強させることを確認
46