よむ、つかう、まなぶ。
【資料1-1】 医薬品等行政評価・監視委員会における海外調査の状況 (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24538.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第7回 3/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
医薬品等行政評価・ 監視委員会
欧米の市販後安全対策を中心とした
薬事制度に関する調査
2022年3月4日
国立衛研 医薬安全科学部
1
欧米の 薬事制度
FDAおよびEMAの以下の情報について調査した
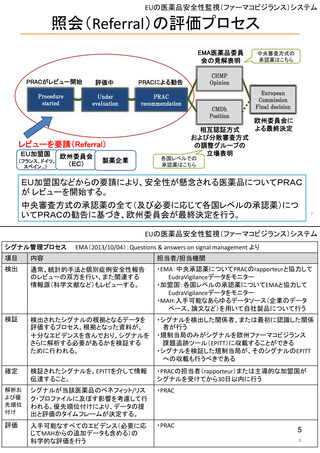
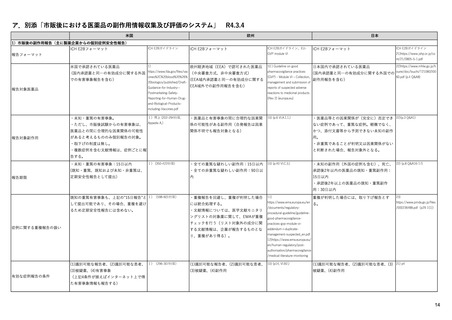
ア 市販後における医薬品の副作用情報収集および評価のシステム
1.
(日米欧における副作用情報の報告対象範囲の比較を含む)
2.
イ 市販後安全対策に関連する安全性の評価および措置の検討を
行う会議体
(具体的な議題内容の最近の例を含む)
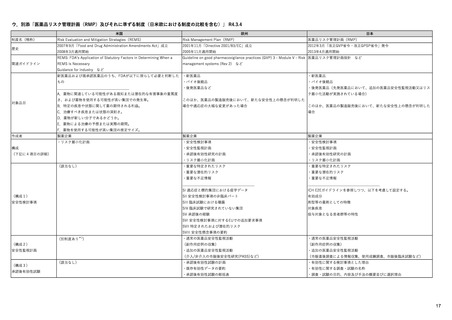
ウ 医薬品リスク管理計画(RMP)およびそれに準ずる制度
3.
(日米欧における制度の比較を含む)
2
2
欧米の市販後安全対策を中心とした
薬事制度に関する調査
2022年3月4日
国立衛研 医薬安全科学部
1
欧米の 薬事制度
FDAおよびEMAの以下の情報について調査した
ア 市販後における医薬品の副作用情報収集および評価のシステム
1.
(日米欧における副作用情報の報告対象範囲の比較を含む)
2.
イ 市販後安全対策に関連する安全性の評価および措置の検討を
行う会議体
(具体的な議題内容の最近の例を含む)
ウ 医薬品リスク管理計画(RMP)およびそれに準ずる制度
3.
(日米欧における制度の比較を含む)
2
2