よむ、つかう、まなぶ。
【資料1】テーマ①(ドラッグロスや供給不足などの医薬品等へのアクセスの課題に対応した安全かつ迅速な承認制度の確立)について.pdf (29 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40580.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和6年度第3回 6/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
参考
現行制度のスキーム
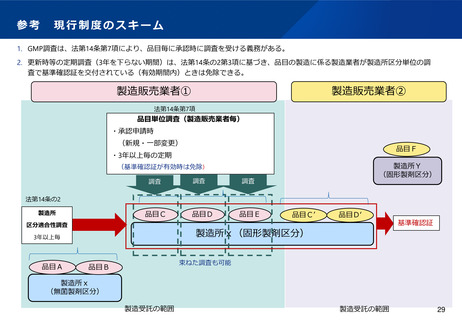
1. GMP調査は、法第14条第7項により、品目毎に承認時に調査を受ける義務がある。
2. 更新時等の定期調査(3年を下らない期間)は、法第14条の2第3項に基づき、品目の製造に係る製造業者が製造所区分単位の調
査で基準確認証を交付されている(有効期間内)ときは免除できる。
製造販売業者②
製造販売業者①
法第14条第7項
品目単位調査(製造販売業者毎)
・承認申請時
(新規・一部変更)
品目F
・3年以上毎の定期
製造所Y
(固形製剤区分)
(基準確認証が有効時は免除)
調査
調査
調査
品目C
品目D
品目E
法第14条の2
製造所
区分適合性調査
品目D‘
基準確認証
製造所x(固形製剤区分)
3年以上毎
品目A
品目C’
束ねた調査も可能
品目B
製造所x
(無菌製剤区分)
製造受託の範囲
製造受託の範囲
29
現行制度のスキーム
1. GMP調査は、法第14条第7項により、品目毎に承認時に調査を受ける義務がある。
2. 更新時等の定期調査(3年を下らない期間)は、法第14条の2第3項に基づき、品目の製造に係る製造業者が製造所区分単位の調
査で基準確認証を交付されている(有効期間内)ときは免除できる。
製造販売業者②
製造販売業者①
法第14条第7項
品目単位調査(製造販売業者毎)
・承認申請時
(新規・一部変更)
品目F
・3年以上毎の定期
製造所Y
(固形製剤区分)
(基準確認証が有効時は免除)
調査
調査
調査
品目C
品目D
品目E
法第14条の2
製造所
区分適合性調査
品目D‘
基準確認証
製造所x(固形製剤区分)
3年以上毎
品目A
品目C’
束ねた調査も可能
品目B
製造所x
(無菌製剤区分)
製造受託の範囲
製造受託の範囲
29