よむ、つかう、まなぶ。
【資料1】テーマ①(ドラッグロスや供給不足などの医薬品等へのアクセスの課題に対応した安全かつ迅速な承認制度の確立)について.pdf (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40580.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和6年度第3回 6/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(7)国家検定制度の見直しについて①(検定手法の合理化)
背景・課題
•
厚生労働大臣が指定する医薬品等(ワクチン、血液製剤等)は、検定を受け、かつ、これに合格したものでなけ
れば販売、授与等をしてはならないとされている(医薬品医療機器等法第43条)。そのため、これらの医薬品の
製造時には、企業が全てのロットの試験検査(自家試験)を実施するとともに、国家検定として、国立感染症研
究所が試験検査及び書面審査(自家試験の確認を含む。)を実施している。
•
検定制度が創設された1940年代とは状況が異なり、現在、医薬品の製造過程における品質確保の行政による監督
として、GMP省令の策定及びGMP調査が行われており、企業の品質管理・試験技術も大幅に向上し、国の機関に
より重ねて実地試験を実施せずとも、品質の確認・確保が可能となっている。
•
そのため、これまでにも、検定手法の合理化を進めており、厚生労働科学研究班による科学的な検討を踏まえ、
書面審査を中心とした審査手法で評価が可能と考えられる品目※については、当該手法への移行や承認当初から当
該手法で検定を行っている。
※ ワクチン67品目中5品目(組織培養不活化ダニ媒介性脳炎ワクチン、20価肺炎球菌ワクチン、23価肺炎球菌ワクチン、コロナウ
イルス(SARS-CoV-2)RNAワクチン、組換えコロナウイルス(SARS-CoV-2)ワクチン;2024年5月末時点)
•
一方で、書面審査のみで検定が可能と考えられる品目であっても、同法上の「検定」の文言については、法令上
現物を検査するものと解されることから、現状、試験品を採取し、現物を確認することが必要となっている。
検討の方向性(案)
•
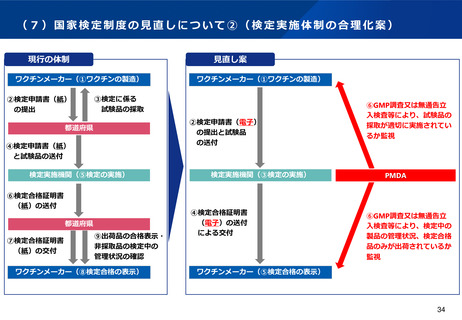
厚生労働科学研究班による科学的な検討の結果、書面審査で検定が可能と考えられる品目に対しては、順次実地試
験を不要とする※。また、書面審査が可能となったものから順次検定機関をPMDAに移管する。
※ ただし、製品の品質や安全性が疑われる場合など必要時には、実地試験をJIHSに委託し実施する予定。
•
検定手法の更なる合理化を図るため、同法上の「検定」の文言の見直しを行い、書面審査のみでの検定手法も可能
となる文言に改める。
31
背景・課題
•
厚生労働大臣が指定する医薬品等(ワクチン、血液製剤等)は、検定を受け、かつ、これに合格したものでなけ
れば販売、授与等をしてはならないとされている(医薬品医療機器等法第43条)。そのため、これらの医薬品の
製造時には、企業が全てのロットの試験検査(自家試験)を実施するとともに、国家検定として、国立感染症研
究所が試験検査及び書面審査(自家試験の確認を含む。)を実施している。
•
検定制度が創設された1940年代とは状況が異なり、現在、医薬品の製造過程における品質確保の行政による監督
として、GMP省令の策定及びGMP調査が行われており、企業の品質管理・試験技術も大幅に向上し、国の機関に
より重ねて実地試験を実施せずとも、品質の確認・確保が可能となっている。
•
そのため、これまでにも、検定手法の合理化を進めており、厚生労働科学研究班による科学的な検討を踏まえ、
書面審査を中心とした審査手法で評価が可能と考えられる品目※については、当該手法への移行や承認当初から当
該手法で検定を行っている。
※ ワクチン67品目中5品目(組織培養不活化ダニ媒介性脳炎ワクチン、20価肺炎球菌ワクチン、23価肺炎球菌ワクチン、コロナウ
イルス(SARS-CoV-2)RNAワクチン、組換えコロナウイルス(SARS-CoV-2)ワクチン;2024年5月末時点)
•
一方で、書面審査のみで検定が可能と考えられる品目であっても、同法上の「検定」の文言については、法令上
現物を検査するものと解されることから、現状、試験品を採取し、現物を確認することが必要となっている。
検討の方向性(案)
•
厚生労働科学研究班による科学的な検討の結果、書面審査で検定が可能と考えられる品目に対しては、順次実地試
験を不要とする※。また、書面審査が可能となったものから順次検定機関をPMDAに移管する。
※ ただし、製品の品質や安全性が疑われる場合など必要時には、実地試験をJIHSに委託し実施する予定。
•
検定手法の更なる合理化を図るため、同法上の「検定」の文言の見直しを行い、書面審査のみでの検定手法も可能
となる文言に改める。
31