よむ、つかう、まなぶ。
【資料1】テーマ①(ドラッグロスや供給不足などの医薬品等へのアクセスの課題に対応した安全かつ迅速な承認制度の確立)について.pdf (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40580.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和6年度第3回 6/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
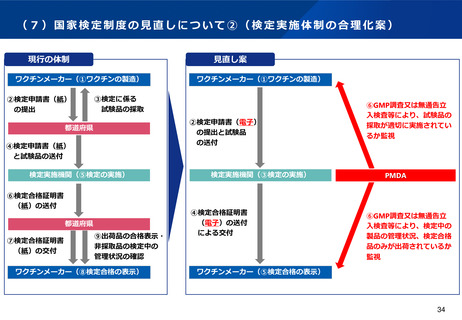
(7)国家検定制度の見直しについて②(検定実施体制の合理化)
背景・課題
•
検定制度については、令和7年4月の国立健康危機管理研究機構(JIHS)の設立以降、JIHSからPMDAに順次品目を移管し、
PMDAが書面審査をしつつも、実地試験が必要な品目の実地試験は引き続きJIHSが実施する体制とすることで、両機関の専門
性を活かした、より合理的な検定体制とすることとしている。
•
しかしながら、検定用の試験品の採取及び検定機関への送付、申請・合格通知の送付、検定合格表示の確認等の作業について
は、行政による中立的な確認を行うため、企業ではなく都道府県が実施している。検定実施数が多い都道府県にとっては業務
負担となっており、都道府県の関与の廃止が要望されている。
•
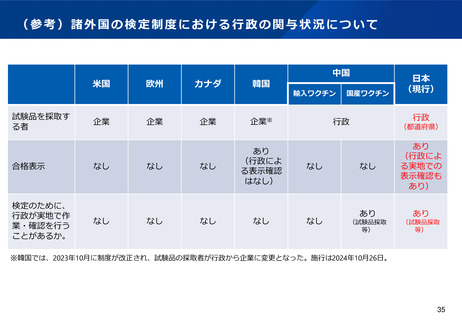
また、検定制度における行政(都道府県)の関与状況については、検定用の試験品の採取等を行政が担当する日本と、企業が
担当する欧米諸国との間で、役割分担が異なっており、国際整合性の観点から合理化が図られていないとの指摘もある(次々
スライド参照)。
•
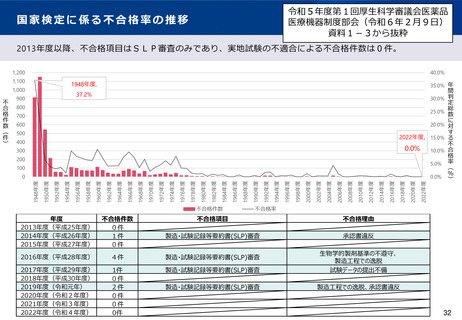
また、「検定合格」の表示については、過去は一定の不合格品が発生し、製造所内に合格品及び非合格品が混在する状況で
あったため、合格品を間違えることなく識別・出荷するため、検定合格品のみに合格証紙で封をし、行政がそれを確認するこ
とに意義があった。一方、現在は、不合格品が生じることは極めて稀であり、また、製品に合格した旨の表示をあらかじめ印
字することで対応されているため、合格表示及び確認作業は形骸化している。さらに、現在は、検定合格ロットの情報を公開
しており、第三者が合格表示によらずとも検定結果を把握することが可能となっている。
検討の方向性(案)
原則書面審査による検定制度に移行する過程、また制度移行後も試験品を用いた実地試験が一部必要な品目が残存するため、
企業の不正防止を図りつつも、実地試験の実施体制の合理化を図る観点から、試験品採取等の都道府県の受託事務について、
以下の方向性で見直しを進める(次スライド参照)。
•
①
都道府県がロット出荷の都度、試験品の採取等を行う体制から、企業が試験品の採取を行った上で、PMDAがGMP調査(実
地)又は無通告立入検査等により企業による適切な作業実施を監視する体制に見直すことで、都道府県の業務の合理化を図り
つつ、企業の作業監視が可能な体制とする。
②
合格表示は廃止し、PMDAによるGMP調査又は無通告立入検査等により合格品のみが出荷されているかの確認で対応する。33
背景・課題
•
検定制度については、令和7年4月の国立健康危機管理研究機構(JIHS)の設立以降、JIHSからPMDAに順次品目を移管し、
PMDAが書面審査をしつつも、実地試験が必要な品目の実地試験は引き続きJIHSが実施する体制とすることで、両機関の専門
性を活かした、より合理的な検定体制とすることとしている。
•
しかしながら、検定用の試験品の採取及び検定機関への送付、申請・合格通知の送付、検定合格表示の確認等の作業について
は、行政による中立的な確認を行うため、企業ではなく都道府県が実施している。検定実施数が多い都道府県にとっては業務
負担となっており、都道府県の関与の廃止が要望されている。
•
また、検定制度における行政(都道府県)の関与状況については、検定用の試験品の採取等を行政が担当する日本と、企業が
担当する欧米諸国との間で、役割分担が異なっており、国際整合性の観点から合理化が図られていないとの指摘もある(次々
スライド参照)。
•
また、「検定合格」の表示については、過去は一定の不合格品が発生し、製造所内に合格品及び非合格品が混在する状況で
あったため、合格品を間違えることなく識別・出荷するため、検定合格品のみに合格証紙で封をし、行政がそれを確認するこ
とに意義があった。一方、現在は、不合格品が生じることは極めて稀であり、また、製品に合格した旨の表示をあらかじめ印
字することで対応されているため、合格表示及び確認作業は形骸化している。さらに、現在は、検定合格ロットの情報を公開
しており、第三者が合格表示によらずとも検定結果を把握することが可能となっている。
検討の方向性(案)
原則書面審査による検定制度に移行する過程、また制度移行後も試験品を用いた実地試験が一部必要な品目が残存するため、
企業の不正防止を図りつつも、実地試験の実施体制の合理化を図る観点から、試験品採取等の都道府県の受託事務について、
以下の方向性で見直しを進める(次スライド参照)。
•
①
都道府県がロット出荷の都度、試験品の採取等を行う体制から、企業が試験品の採取を行った上で、PMDAがGMP調査(実
地)又は無通告立入検査等により企業による適切な作業実施を監視する体制に見直すことで、都道府県の業務の合理化を図り
つつ、企業の作業監視が可能な体制とする。
②
合格表示は廃止し、PMDAによるGMP調査又は無通告立入検査等により合格品のみが出荷されているかの確認で対応する。33