よむ、つかう、まなぶ。
【資料1】テーマ①(ドラッグロスや供給不足などの医薬品等へのアクセスの課題に対応した安全かつ迅速な承認制度の確立)について.pdf (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40580.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和6年度第3回 6/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
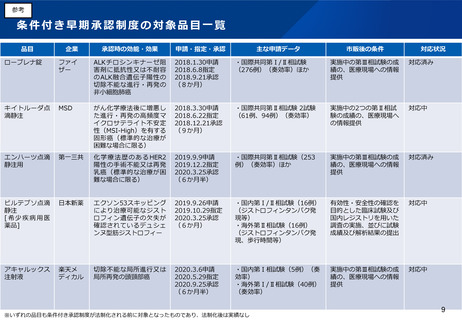
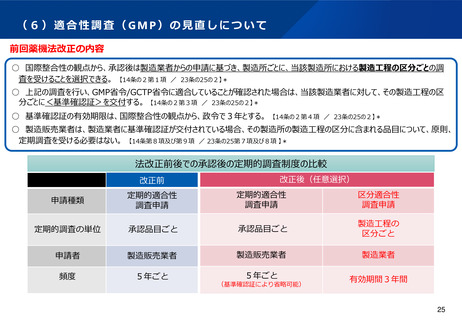
参考
医薬品の早期承認に関する日米欧の制度と米国の運用状況
出典:令和5年度厚生労働科学特別研究事業「臨床試験が実施困難な希少疾患等に対する医薬品の迅速な国内導入を
図るための薬事承認審査制度の構築に向けた調査研究」(中間報告)(研究代表者:北里大学薬学部成川衛教授)
▍医薬品の早期承認に関する日米欧の制度
日本
条件付き承認制度
⚫
適用条件
希少疾病用医薬品、先駆的医薬品など医療上特にそ
の必要性が高く*、検証的臨床試験の実施が困難又は
相当の時間を要する
米国
Accelerated Approval
⚫
⚫
重篤又は生命を脅かす疾患を対象とする
適切な代替エンドポイントにおいて、既存治療を上
回る有益な治療効果が示される
⚫
⚫
⚫
⚫
臨床効果を証明する試験の実施
市販後臨床試験の実施状況を定期的にFDAに報告
Labelingに迅速承認された医薬品である旨を記載
迅速な承認取り下げ手続きの規定あり
* 重篤な疾患を対象とし、既存の治療法がない又はそれと比較して
有効性又は安全性が優れる
⚫
市販後
適用件数
⚫
使用成績に関する調査、適正使用確保のために必要
な措置等の実施
承認時に指定された期間内に調査成績等を提出し、
中間評価を実施
EU
Conditional Marketing Authorization
5件(法制化後は0件)
重篤又は生命を脅かす疾患を対象とする(パンデ
ミック等の緊急な状況も含む)
データが不完全ではあるもののベネフィットがリス
クを上回る(当該医薬品を迅速に提供することによ
る国民の健康への利益が大きい)
⚫
⚫
ベネフィットがリスクを上回ることを確認する試験
の実施
条件付き承認の有効期間は1年(更新は可能)
添付文書に条件付き承認である旨を記載
⚫
⚫
⚫
295品目(2023年3月まで)
82品目(2022年まで)
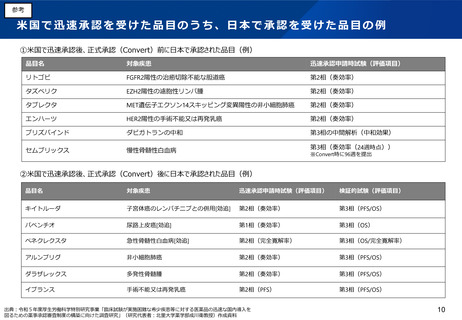
▍米国の迅速承認制度(AA)の運用状況
AA承認後の正式承認への移行、取消
AA承認品目合計 295品目、平均審査期間 7.8ヶ月
60
承
認
品
目
数
20
50
15
40
30
10
20
5
10
0
0
審
査
期
間
(
月
)
Not yet
33%
Withdrawn
Converted
Withdrawn
Not yet
295
品目
Converted
55%
12%
:正式承認へ移行
:AA承認の取消
:未判断(検証試験実施中/審査中)
7
医薬品の早期承認に関する日米欧の制度と米国の運用状況
出典:令和5年度厚生労働科学特別研究事業「臨床試験が実施困難な希少疾患等に対する医薬品の迅速な国内導入を
図るための薬事承認審査制度の構築に向けた調査研究」(中間報告)(研究代表者:北里大学薬学部成川衛教授)
▍医薬品の早期承認に関する日米欧の制度
日本
条件付き承認制度
⚫
適用条件
希少疾病用医薬品、先駆的医薬品など医療上特にそ
の必要性が高く*、検証的臨床試験の実施が困難又は
相当の時間を要する
米国
Accelerated Approval
⚫
⚫
重篤又は生命を脅かす疾患を対象とする
適切な代替エンドポイントにおいて、既存治療を上
回る有益な治療効果が示される
⚫
⚫
⚫
⚫
臨床効果を証明する試験の実施
市販後臨床試験の実施状況を定期的にFDAに報告
Labelingに迅速承認された医薬品である旨を記載
迅速な承認取り下げ手続きの規定あり
* 重篤な疾患を対象とし、既存の治療法がない又はそれと比較して
有効性又は安全性が優れる
⚫
市販後
適用件数
⚫
使用成績に関する調査、適正使用確保のために必要
な措置等の実施
承認時に指定された期間内に調査成績等を提出し、
中間評価を実施
EU
Conditional Marketing Authorization
5件(法制化後は0件)
重篤又は生命を脅かす疾患を対象とする(パンデ
ミック等の緊急な状況も含む)
データが不完全ではあるもののベネフィットがリス
クを上回る(当該医薬品を迅速に提供することによ
る国民の健康への利益が大きい)
⚫
⚫
ベネフィットがリスクを上回ることを確認する試験
の実施
条件付き承認の有効期間は1年(更新は可能)
添付文書に条件付き承認である旨を記載
⚫
⚫
⚫
295品目(2023年3月まで)
82品目(2022年まで)
▍米国の迅速承認制度(AA)の運用状況
AA承認後の正式承認への移行、取消
AA承認品目合計 295品目、平均審査期間 7.8ヶ月
60
承
認
品
目
数
20
50
15
40
30
10
20
5
10
0
0
審
査
期
間
(
月
)
Not yet
33%
Withdrawn
Converted
Withdrawn
Not yet
295
品目
Converted
55%
12%
:正式承認へ移行
:AA承認の取消
:未判断(検証試験実施中/審査中)
7