よむ、つかう、まなぶ。
資料2-2 日本製薬工業協会 御提出資料 (13 ページ)
出典
| 公開元URL | https://www8.cao.go.jp/kisei-kaikaku/kisei/meeting/wg/2409_04medical/241125/medical03_agenda.html |
| 出典情報 | 規制改革推進会議 健康・医療・介護ワーキング・グループ(第3回 11/25)《内閣府》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
個人情報保護制度の課題
データの利活用には原則として本人同意が必要
• 同意説明と取得を行う医療機関の手間や手続き等の負担は非常に大きい。
• 将来のために情報を蓄積する場合(レジストリ、バイオバンク等)同意取得時点で詳細な説明が困難
• 製薬企業はグローバルに活動しており、令和2年改正法による外国への第三者への提供に関する説明事項の増加が大
きな負担
• 個人情報保護法や医学系倫理指針が複雑であり、何をどこまで説明すればよいか理解困難
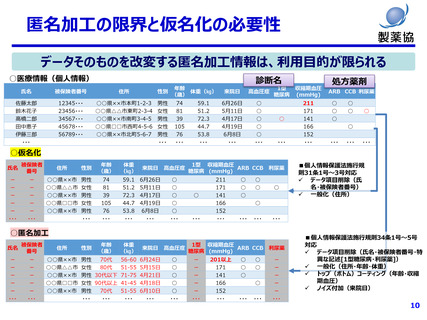
匿名加工だけでは不十分
• データそのものが加工され真正性が失われる匿名加工はそもそも医学研究に馴染まない
• データの真正性が確認できず、薬事申請等の利活用が困難
• 症状等の追加情報収集や経時的追跡が不可能
• 希少な症例や外れ値の活用ができない
• ゲノムデータは匿名加工、仮名加工できない(個人識別符号のため)
• 次世代医療基盤法の「丁寧なオプトアウト」は通常の同意取得と大差なく医療機関の負担大
• 次世代医療基盤法では、認定された民間事業者が自らデータ収集をする取り組みであり、全人口をカバーするデータ基
盤になる見込みはない
その他
• 公衆衛生例外規定では革新的な医薬品の研究目的(開発は対象外)のみしか活用できず限定的。
• 医薬品開発は10年以上要するが、その間も個情法は3年毎に見直される。過去に取得したデータが利用できなくならない
よう、適切な経過措置や予見性が必要。
13
データの利活用には原則として本人同意が必要
• 同意説明と取得を行う医療機関の手間や手続き等の負担は非常に大きい。
• 将来のために情報を蓄積する場合(レジストリ、バイオバンク等)同意取得時点で詳細な説明が困難
• 製薬企業はグローバルに活動しており、令和2年改正法による外国への第三者への提供に関する説明事項の増加が大
きな負担
• 個人情報保護法や医学系倫理指針が複雑であり、何をどこまで説明すればよいか理解困難
匿名加工だけでは不十分
• データそのものが加工され真正性が失われる匿名加工はそもそも医学研究に馴染まない
• データの真正性が確認できず、薬事申請等の利活用が困難
• 症状等の追加情報収集や経時的追跡が不可能
• 希少な症例や外れ値の活用ができない
• ゲノムデータは匿名加工、仮名加工できない(個人識別符号のため)
• 次世代医療基盤法の「丁寧なオプトアウト」は通常の同意取得と大差なく医療機関の負担大
• 次世代医療基盤法では、認定された民間事業者が自らデータ収集をする取り組みであり、全人口をカバーするデータ基
盤になる見込みはない
その他
• 公衆衛生例外規定では革新的な医薬品の研究目的(開発は対象外)のみしか活用できず限定的。
• 医薬品開発は10年以上要するが、その間も個情法は3年毎に見直される。過去に取得したデータが利用できなくならない
よう、適切な経過措置や予見性が必要。
13