よむ、つかう、まなぶ。
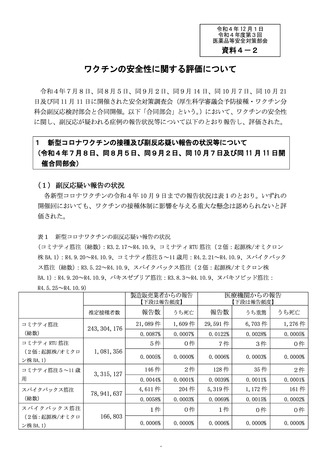
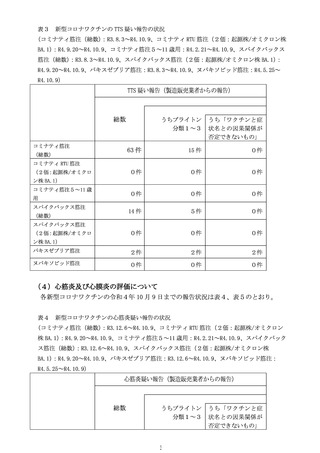
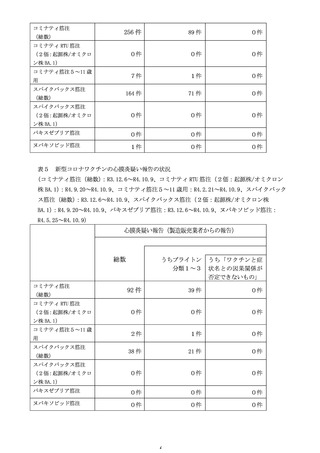
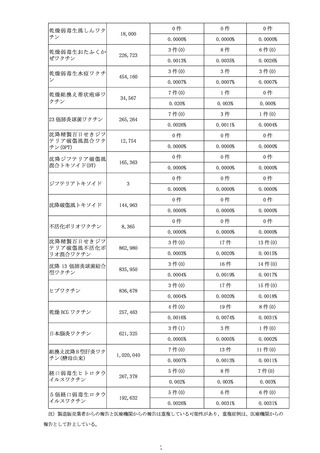
資料4-2 ワクチンの安全性に関する評価について (27 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29460.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第3回 12/1)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別添3
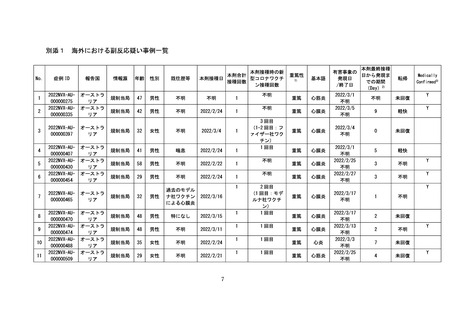
海外添付文書の記載状況
オーストラリア添付文書(2022 年6月)
4.8 ADVERSE EFFECTS (UNDESIRABLE EFFECTS)
Post-marketing experience
The following adverse reactions have been spontaneously reported during post-authorisation use of NUVAXOVID. As these reactions
were derived from spontaneous reports, the frequencies could not be determined and are thus considered as not known.
Table 2: Adverse reactions from post-marketing experience
Cardiac disorders
Pericarditis
16
海外添付文書の記載状況
オーストラリア添付文書(2022 年6月)
4.8 ADVERSE EFFECTS (UNDESIRABLE EFFECTS)
Post-marketing experience
The following adverse reactions have been spontaneously reported during post-authorisation use of NUVAXOVID. As these reactions
were derived from spontaneous reports, the frequencies could not be determined and are thus considered as not known.
Table 2: Adverse reactions from post-marketing experience
Cardiac disorders
Pericarditis
16