よむ、つかう、まなぶ。
資料2-2 精製ヒアルロン酸ナトリウムのリスク評価について (36 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34324.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会 医薬品等安全対策部会 安全対策調査会(令和5年度第4回 7/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別紙(1)
調査結果の概要
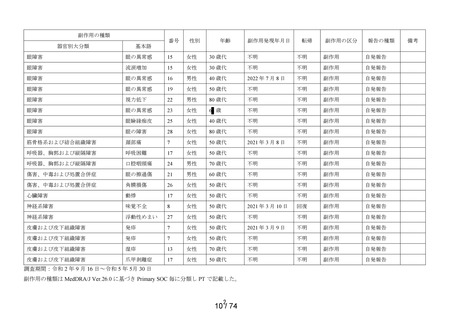
本剤の調査結果(調査期間:令和 3 年 9 月 16 日~令和 4 年 9 月 15 日)を以下の通り示す。
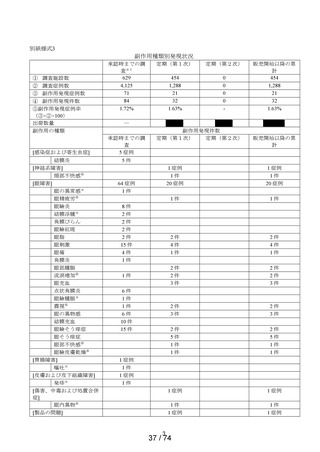
(1) 副作用頻度調査
副作用頻度調査において、別紙様式4に示すとおり、前回調査期間(令和 2 年 9 月 16 日~令和 3
年 9 月 15 日)に調査が完了していたため、当該調査期間(令和 3 年 9 月 16 日~令和 4 年 9 月 15
日)に収集された副作用はなかった。なお、これまでの副作用種類別発現状況は別紙様式3に示すと
おりである。
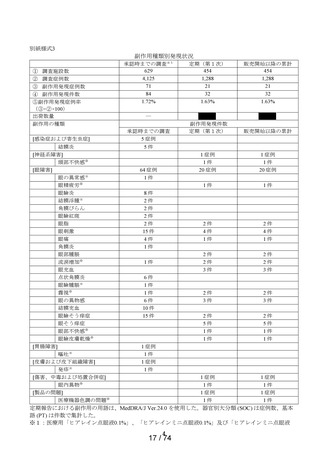
(2) 一般調査
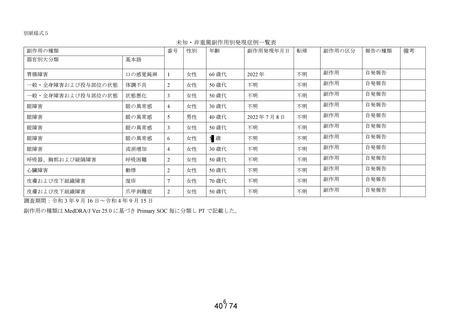
一般調査における副作用発現症例数は14例で、副作用発現件数は20件であった。重篤な副作用の報告
はなかった(別紙様式6)。未知の副作用は7例12件で、「眼の異常感」が4 件、「呼吸困難」、「口
の感覚鈍麻」、「湿疹」、「状態悪化」、「体調不良」、「爪甲剥離症」、「動悸」及び「流涙増加」
が各1 件であった。これらの一般調査における未知・非重篤副作用別発現症例一覧表は、別紙様式5に
示すとおりである。
(3) 研究報告および外国での規制措置情報
本剤の承認日以降、当該調査期間終了日(令和 4 年9 月15 日)までに研究報告、外国措置報告の対
象となるものはなかった。
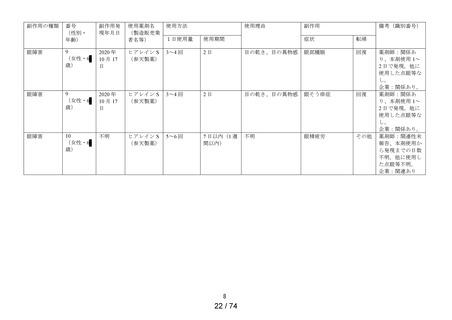
(4) 適正 使用状況(「してはいけないこと」「相談すること」「効能・効果」「用法・用量」等の遵守)
一般調査の結果から、「してはいけないこと」に該当する症例は、ドライアイ患者の使用報告が7
件あり、いずれも副作用は確認されなかった。またスティ-ブンス・ジョンソン症候群の患者の使用
報告が1件あり、副作用として体調不良、動悸、 呼吸困難、 爪甲剥離症が報告された。
1日の使用回数については、過少量投与(1日1~2回使用)の報告が4件、過量投与(1日10回程度)
の報告が1件であった。いずれの症例においても副作用は確認されなかった。
投与日数が15日以上の症例は3件報告され、医師または薬剤師への相談の有無は、1件はあり、1件
はなし、1件は不明であった。いずれの症例においても副作用は確認されなかった。
2
36 / 74
調査結果の概要
本剤の調査結果(調査期間:令和 3 年 9 月 16 日~令和 4 年 9 月 15 日)を以下の通り示す。
(1) 副作用頻度調査
副作用頻度調査において、別紙様式4に示すとおり、前回調査期間(令和 2 年 9 月 16 日~令和 3
年 9 月 15 日)に調査が完了していたため、当該調査期間(令和 3 年 9 月 16 日~令和 4 年 9 月 15
日)に収集された副作用はなかった。なお、これまでの副作用種類別発現状況は別紙様式3に示すと
おりである。
(2) 一般調査
一般調査における副作用発現症例数は14例で、副作用発現件数は20件であった。重篤な副作用の報告
はなかった(別紙様式6)。未知の副作用は7例12件で、「眼の異常感」が4 件、「呼吸困難」、「口
の感覚鈍麻」、「湿疹」、「状態悪化」、「体調不良」、「爪甲剥離症」、「動悸」及び「流涙増加」
が各1 件であった。これらの一般調査における未知・非重篤副作用別発現症例一覧表は、別紙様式5に
示すとおりである。
(3) 研究報告および外国での規制措置情報
本剤の承認日以降、当該調査期間終了日(令和 4 年9 月15 日)までに研究報告、外国措置報告の対
象となるものはなかった。
(4) 適正 使用状況(「してはいけないこと」「相談すること」「効能・効果」「用法・用量」等の遵守)
一般調査の結果から、「してはいけないこと」に該当する症例は、ドライアイ患者の使用報告が7
件あり、いずれも副作用は確認されなかった。またスティ-ブンス・ジョンソン症候群の患者の使用
報告が1件あり、副作用として体調不良、動悸、 呼吸困難、 爪甲剥離症が報告された。
1日の使用回数については、過少量投与(1日1~2回使用)の報告が4件、過量投与(1日10回程度)
の報告が1件であった。いずれの症例においても副作用は確認されなかった。
投与日数が15日以上の症例は3件報告され、医師または薬剤師への相談の有無は、1件はあり、1件
はなし、1件は不明であった。いずれの症例においても副作用は確認されなかった。
2
36 / 74