よむ、つかう、まなぶ。
【先進医療合同会議】議題1 別紙1先進医療Bに係る新規技術の科学的評価等について (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_50847.html |
| 出典情報 | 先進医療合同会議(第140回先進医療会議、第171回先進医療技術審査部会 2/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
10.有効性及び安全性の評価方法
適
・
不適
11.モニタリング体制及び実施方法
適
・
不適
12.被験者等に対して重大な事態が生じた場合の
対処方法
適
・
不適
13.試験に係る記録の取扱い及び管理・保存方法
適
・
不適
14.患者負担の内容
適
・
不適
15.起こりうる利害の衝突及び研究者等の関連組織
との関わり
適
・
不適
16.個人情報保護の方法
適
・
不適
コメント欄:(「不適」とした場合には必ず記載ください。)
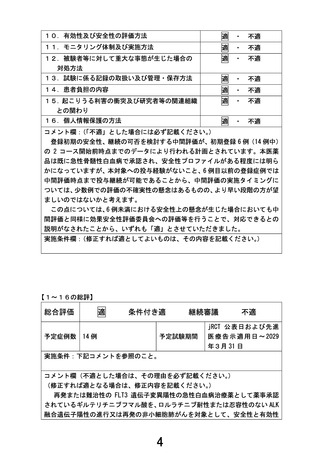
登録初期の安全性、継続の可否を検討する中間評価が、初期登録 6 例(14 例中)
の 2 コース開始前時点までのデータにより行われる計画とされています。本医薬
品は既に急性骨髄性白血病で承認され、安全性プロファイルがある程度には明ら
かになっていますが、本対象への投与経験がないこと、6 例目以前の登録症例では
中間評価時点まで投与継続が可能であることから、中間評価の実施タイミングに
ついては、少数例での評価の不確実性の懸念はあるものの、より早い段階の方が望
ましいのではないかと考えます。
この点については、6 例未満における安全性上の懸念が生じた場合においても中
間評価と同様に効果安全性評価委員会への評価等を行うことで、対応できるとの
説明がなされたことから、いずれも「適」とさせていただきました。
実施条件欄:(修正すれば適としてよいものは、その内容を記載ください。)
【1~16の総評】
総合評価
予定症例数 14 例
適
条件付き適
継続審議
予定試験期間
不適
jRCT 公表日および先進
医 療 告 示 適 用 日 ~ 2029
年3月 31 日
実施条件:下記コメントを参照のこと。
コメント欄(不適とした場合は、その理由を必ず記載ください。)
(修正すれば適となる場合は、修正内容を記載ください。)
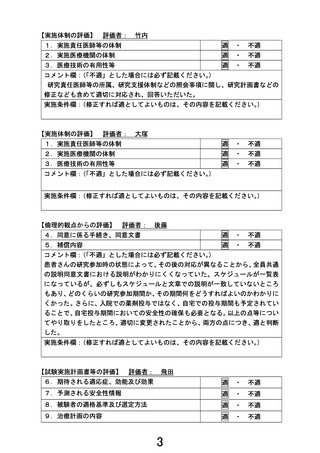
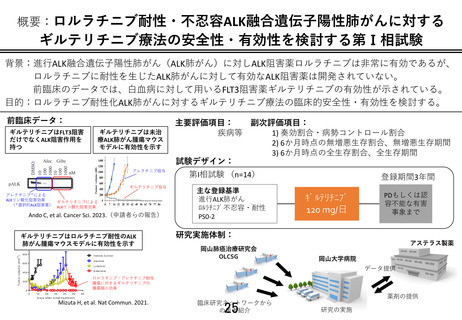
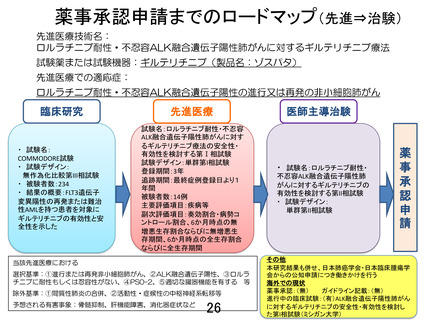
再発または難治性の FLT3 遺伝子変異陽性の急性白血病治療薬として薬事承認
されているギルテリチニブフマル酸を、ロルラチニブ耐性または忍容性のない ALK
融合遺伝子陽性の進行又は再発の非小細胞肺がんを対象として、安全性と有効性
4
適
・
不適
11.モニタリング体制及び実施方法
適
・
不適
12.被験者等に対して重大な事態が生じた場合の
対処方法
適
・
不適
13.試験に係る記録の取扱い及び管理・保存方法
適
・
不適
14.患者負担の内容
適
・
不適
15.起こりうる利害の衝突及び研究者等の関連組織
との関わり
適
・
不適
16.個人情報保護の方法
適
・
不適
コメント欄:(「不適」とした場合には必ず記載ください。)
登録初期の安全性、継続の可否を検討する中間評価が、初期登録 6 例(14 例中)
の 2 コース開始前時点までのデータにより行われる計画とされています。本医薬
品は既に急性骨髄性白血病で承認され、安全性プロファイルがある程度には明ら
かになっていますが、本対象への投与経験がないこと、6 例目以前の登録症例では
中間評価時点まで投与継続が可能であることから、中間評価の実施タイミングに
ついては、少数例での評価の不確実性の懸念はあるものの、より早い段階の方が望
ましいのではないかと考えます。
この点については、6 例未満における安全性上の懸念が生じた場合においても中
間評価と同様に効果安全性評価委員会への評価等を行うことで、対応できるとの
説明がなされたことから、いずれも「適」とさせていただきました。
実施条件欄:(修正すれば適としてよいものは、その内容を記載ください。)
【1~16の総評】
総合評価
予定症例数 14 例
適
条件付き適
継続審議
予定試験期間
不適
jRCT 公表日および先進
医 療 告 示 適 用 日 ~ 2029
年3月 31 日
実施条件:下記コメントを参照のこと。
コメント欄(不適とした場合は、その理由を必ず記載ください。)
(修正すれば適となる場合は、修正内容を記載ください。)
再発または難治性の FLT3 遺伝子変異陽性の急性白血病治療薬として薬事承認
されているギルテリチニブフマル酸を、ロルラチニブ耐性または忍容性のない ALK
融合遺伝子陽性の進行又は再発の非小細胞肺がんを対象として、安全性と有効性
4