よむ、つかう、まなぶ。
別紙3 (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00042.html |
| 出典情報 | 先進医療会議(第108回先進医療会議、第129回先進医療技術審査部会 3/3)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
先進医療会議事前評価構成員からの指摘事項に対する回答1
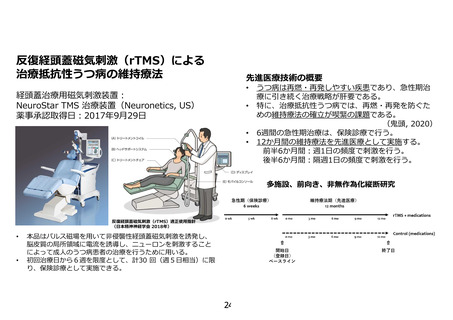
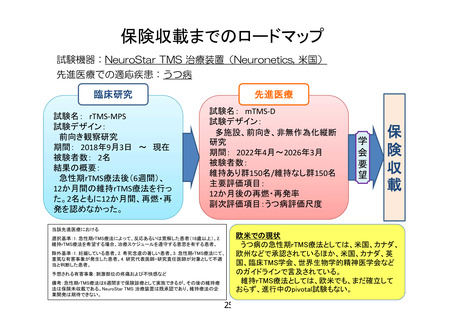
先進医療技術名: 反復経頭蓋磁気刺激による治療抵抗性うつ病の維持療法
令和4年2月15日
所属・氏名:国立精神・神経医療研究センター・鬼頭伸輔
以下の点について検討し,必要に応じて関連書類についても修正してください.
1.研究計画では、急性期 rTMS 療法に反応あるいは寛解した患者を維持 rTMS 治療あり群
と維持 rTMS 治療なし群(対照)に非無作為に振り分けるとあります。そして、二重盲検無
作為化については、「実現可能性および盲検妥当性、また、研究実施にかかる費用の問題
から実施せず、維持 rTMS 治療なし群を対照とし維持 rTMS 治療あり群の有効性を検証」
と記載があります。
① 維持 rTMS 治療あり群の有効性をしっかりと検証するためには二重盲検無作為化が必
要と考えますが、いかがでしょうか。ご記載いただいた二重盲検無作為化をしない理由
のみでは、説得力が十分とは言えません。
② 維持 rTMS 治療あり群、維持 rTMS 治療なし群ともに、薬物治療の有無やその内容に
ついての言及がありません。両群ともに薬物療法はなしという理解で良いのでしょうか。
あるいは薬物療法の内容は問わないということなのでしょうか。薬物療法の併用を認め
るならば、それについて標準化するなどの配慮が必要と考えますが、いかがでしょうか。
【回答】
①に対する回答
ご指摘いただき、ありがとうございました。当初、本研究計画は二重盲検無作為化試
験にて、維持 rTMS 療法の有効性を検証することを予定しておりましたが、以下の理由
から、非盲検非無作為化試験としました。
現在、申請者らは、別途 EASyS-BD(jRCTs032180138)を先進医療として進めていま
すが、こちらの研究では、週 5 日、4 週間の rTMS 療法を二重盲検無作為化で実施して
います(急性期療法)
。試験デザインは計 20 回のセッション、4 週間の介入期間です。
一方、本研究では、計 40 回のセッション、12 か月間の維持療法期間となっており、
EASyS-BD(jRCTs032180138)の経験を通して、セッション数の多さ(計 40 回)、12 か
月間にわたる二重盲検無作為化であること、また、一番の理由としては、本研究では維
持 rTMS 療法期間に入る前に、全例、急性期 rTMS 療法を受けていることから(実刺激
を受けた患者が、実刺激あるいは偽刺激に割り付けされるため、シャム刺激システムを
使用しても判別できる可能性がある)、実現可能性および盲検妥当性の観点から、本研
究で二重盲検無作為化を実施することは困難であると判断しました。
次に、急性期 rTMS 療法に使用する NeuroStar TMS 治療装置はシャム刺激を実施でき
ず、シャム刺激を実施できる研究用の装置を入手できないことも理由に挙げられます。
21
先進医療技術名: 反復経頭蓋磁気刺激による治療抵抗性うつ病の維持療法
令和4年2月15日
所属・氏名:国立精神・神経医療研究センター・鬼頭伸輔
以下の点について検討し,必要に応じて関連書類についても修正してください.
1.研究計画では、急性期 rTMS 療法に反応あるいは寛解した患者を維持 rTMS 治療あり群
と維持 rTMS 治療なし群(対照)に非無作為に振り分けるとあります。そして、二重盲検無
作為化については、「実現可能性および盲検妥当性、また、研究実施にかかる費用の問題
から実施せず、維持 rTMS 治療なし群を対照とし維持 rTMS 治療あり群の有効性を検証」
と記載があります。
① 維持 rTMS 治療あり群の有効性をしっかりと検証するためには二重盲検無作為化が必
要と考えますが、いかがでしょうか。ご記載いただいた二重盲検無作為化をしない理由
のみでは、説得力が十分とは言えません。
② 維持 rTMS 治療あり群、維持 rTMS 治療なし群ともに、薬物治療の有無やその内容に
ついての言及がありません。両群ともに薬物療法はなしという理解で良いのでしょうか。
あるいは薬物療法の内容は問わないということなのでしょうか。薬物療法の併用を認め
るならば、それについて標準化するなどの配慮が必要と考えますが、いかがでしょうか。
【回答】
①に対する回答
ご指摘いただき、ありがとうございました。当初、本研究計画は二重盲検無作為化試
験にて、維持 rTMS 療法の有効性を検証することを予定しておりましたが、以下の理由
から、非盲検非無作為化試験としました。
現在、申請者らは、別途 EASyS-BD(jRCTs032180138)を先進医療として進めていま
すが、こちらの研究では、週 5 日、4 週間の rTMS 療法を二重盲検無作為化で実施して
います(急性期療法)
。試験デザインは計 20 回のセッション、4 週間の介入期間です。
一方、本研究では、計 40 回のセッション、12 か月間の維持療法期間となっており、
EASyS-BD(jRCTs032180138)の経験を通して、セッション数の多さ(計 40 回)、12 か
月間にわたる二重盲検無作為化であること、また、一番の理由としては、本研究では維
持 rTMS 療法期間に入る前に、全例、急性期 rTMS 療法を受けていることから(実刺激
を受けた患者が、実刺激あるいは偽刺激に割り付けされるため、シャム刺激システムを
使用しても判別できる可能性がある)、実現可能性および盲検妥当性の観点から、本研
究で二重盲検無作為化を実施することは困難であると判断しました。
次に、急性期 rTMS 療法に使用する NeuroStar TMS 治療装置はシャム刺激を実施でき
ず、シャム刺激を実施できる研究用の装置を入手できないことも理由に挙げられます。
21