よむ、つかう、まなぶ。
別紙3 (29 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00042.html |
| 出典情報 | 先進医療会議(第108回先進医療会議、第129回先進医療技術審査部会 3/3)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
【別添4】
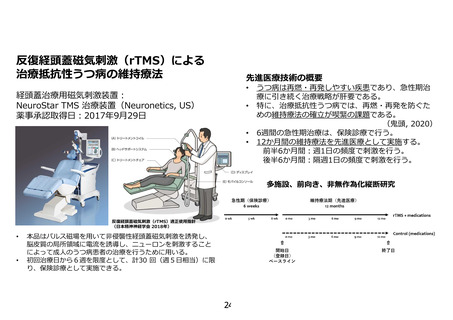
「反復経頭蓋磁気刺激による治療抵抗性うつ病の維持療法」の有効性
及び安全性の評価(申請書類より抜粋)
7-1.有効性及び安全性の評価
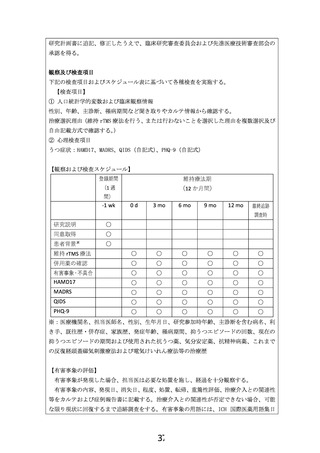
評価項目、評価方法
<用語の定義>
本研究の評価項目に関する用語を次のように定義する。
反応:急性期 rTMS 療法開始前と比較して HAMD17 の総得点が 50%以上減少するものを反
応と定義する。
反応率:反応した患者の割合を反応率とする。
寛解:HAMD17 の総得点が 7 以下を寛解と定義する。
寛解率:寛解した患者の割合を寛解率とする。
再燃・再発:HAMD17 の総得点が 14 以上を再燃・再発と定義する。
再燃・再発率:再燃・再発した患者の割合を再燃・再発率とする。
1)primary endpoint
登録後 12 ヵ月までの再燃・再発率
2)secondary endpoint(s)
登録後 3 ヵ月、6 ヵ月、9 ヵ月の再燃・再発率
(ただし、各評価時期より前に再燃・再発している対象者は以降も再燃・再発と
して扱う)
登録後 3 ヵ月、6 ヵ月、9 ヵ月、12 ヵ月の反応率
登録後 3 ヵ月、6 ヵ月、9 ヵ月、12 ヵ月の寛解率
登録後の HAMD17、MADRS、QIDS、PHQ-9 の変化量
登録後、再燃・再発までの期間
有害事象
不具合
安全性評価
有害事象の確認
頭痛、刺激部位の疼痛、刺激部位の不快感、筋収縮、躁病・軽躁病エピソード(DSM-5 の診
断基準に合致)
、希死念慮、けいれん発作(急性期治療期間および観察期間)
HAMD17、MADRS については評価信頼性の観点から、経験豊富な臨床試験に携わった経験の
ある評価者(臨床心理士あるいは公認心理師)を選定する。原則、同一被験者に対して同一
評価者が実施し、評価者間一致に関しては、本試験開始前に DVD 等を用いた模擬患者による
評価一致度を確認する。
統計解析の方法
29
「反復経頭蓋磁気刺激による治療抵抗性うつ病の維持療法」の有効性
及び安全性の評価(申請書類より抜粋)
7-1.有効性及び安全性の評価
評価項目、評価方法
<用語の定義>
本研究の評価項目に関する用語を次のように定義する。
反応:急性期 rTMS 療法開始前と比較して HAMD17 の総得点が 50%以上減少するものを反
応と定義する。
反応率:反応した患者の割合を反応率とする。
寛解:HAMD17 の総得点が 7 以下を寛解と定義する。
寛解率:寛解した患者の割合を寛解率とする。
再燃・再発:HAMD17 の総得点が 14 以上を再燃・再発と定義する。
再燃・再発率:再燃・再発した患者の割合を再燃・再発率とする。
1)primary endpoint
登録後 12 ヵ月までの再燃・再発率
2)secondary endpoint(s)
登録後 3 ヵ月、6 ヵ月、9 ヵ月の再燃・再発率
(ただし、各評価時期より前に再燃・再発している対象者は以降も再燃・再発と
して扱う)
登録後 3 ヵ月、6 ヵ月、9 ヵ月、12 ヵ月の反応率
登録後 3 ヵ月、6 ヵ月、9 ヵ月、12 ヵ月の寛解率
登録後の HAMD17、MADRS、QIDS、PHQ-9 の変化量
登録後、再燃・再発までの期間
有害事象
不具合
安全性評価
有害事象の確認
頭痛、刺激部位の疼痛、刺激部位の不快感、筋収縮、躁病・軽躁病エピソード(DSM-5 の診
断基準に合致)
、希死念慮、けいれん発作(急性期治療期間および観察期間)
HAMD17、MADRS については評価信頼性の観点から、経験豊富な臨床試験に携わった経験の
ある評価者(臨床心理士あるいは公認心理師)を選定する。原則、同一被験者に対して同一
評価者が実施し、評価者間一致に関しては、本試験開始前に DVD 等を用いた模擬患者による
評価一致度を確認する。
統計解析の方法
29