よむ、つかう、まなぶ。
資料1-2 アムロジピンベシル酸塩 調査結果報告書及び添付文書 (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29305.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第19回 11/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
した。
III. WG における検討
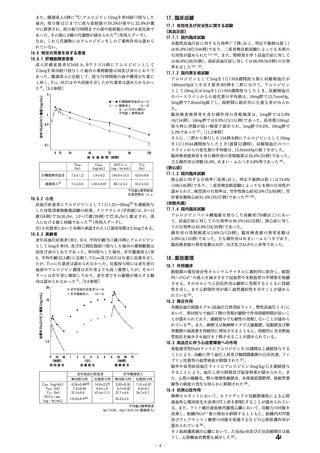
本薬の添付文書における「妊婦又は妊娠している可能性のある女性」への注意事項の適切
性について、表 1 に示す項目を含む WG 報告書(別添 2)が取りまとめられた。
表 1.
WG 報告書の項目
1.品目の概要
5.臨床使用に関する報告
2.背景
6.国内外のガイドライン
3.海外添付文書における記載状況
7.禁忌解除の妥当性
4.動物試験
8.添付文書改訂案
IV. 機構における調査
機構は、WG 報告書を踏まえ、以下の点について検討を行った。
1. 臨床使用に基づく情報(WG 報告書「5. 臨床使用に関する報告」参照)
1-1. 公表文献
WG により、Ca 拮抗薬と妊娠に関する文献が抽出された(検索日:2018 年 8 月 7 日)
。抽
出された 7 報(ニフェジピン単独研究を除く)及びハンドサーチで特定された 1 報の計 8 報
が臨床使用における催奇形性を検討した公表文献であった(WG 報告書「5. 臨床使用に関
する報告」参照)
。なお、妊娠期間及び分娩時間の延長については、通常の診療内において
も発生することであり、本邦のガイドライン等も参考にして、対応することが可能であると
判断され、検討されていない。
当該 8 報のうち、7 報は先天異常のリスク推定指標(リスク比、オッズ比等)が記述され
ている研究報告であり、1 報はリスク推定指標が記述されていない研究報告であった。リス
ク推定指標が記述されている研究報告 7 報のうち、6 報は妊娠初期における Ca 拮抗薬(う
ち 2 報は本薬を含むことが記載)の使用による先天異常のリスク増加は認められなかった
という報告であった(WG 報告書文献番号 1~4、7、8)
。1 報は、妊娠初期の Ca 拮抗薬の使
用による先天異常全体(先天異常の種類は問わない)のリスク増加は認められなかった一方、
先天異常の種類別の検討では上部消化管奇形のリスク増加が認められたという報告であっ
た(WG 報告書文献番号 5)。リスク推定指標が記述されていない研究報告は、妊娠判明時
に Ca 拮抗薬の曝露があった 8 例の女性を追跡した結果、全症例健康な児を出産したという
報告であった(WG 報告書文献番号 6)
。
本薬の先発医薬品の製造販売承認取得者により、
WG 報告書と同様の検索条件 2を用いて、
WG 報告書の検索日以降に公表された本薬を含む Ca 拮抗薬と妊娠に関する文献が抽出され
2
WG 報告書 p.22 参照
2
2
III. WG における検討
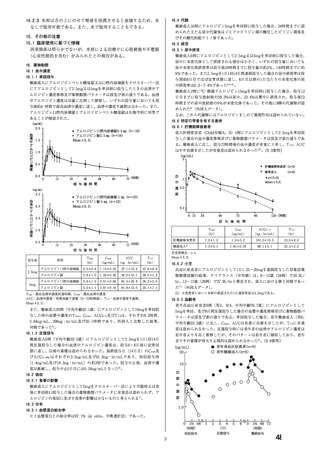
本薬の添付文書における「妊婦又は妊娠している可能性のある女性」への注意事項の適切
性について、表 1 に示す項目を含む WG 報告書(別添 2)が取りまとめられた。
表 1.
WG 報告書の項目
1.品目の概要
5.臨床使用に関する報告
2.背景
6.国内外のガイドライン
3.海外添付文書における記載状況
7.禁忌解除の妥当性
4.動物試験
8.添付文書改訂案
IV. 機構における調査
機構は、WG 報告書を踏まえ、以下の点について検討を行った。
1. 臨床使用に基づく情報(WG 報告書「5. 臨床使用に関する報告」参照)
1-1. 公表文献
WG により、Ca 拮抗薬と妊娠に関する文献が抽出された(検索日:2018 年 8 月 7 日)
。抽
出された 7 報(ニフェジピン単独研究を除く)及びハンドサーチで特定された 1 報の計 8 報
が臨床使用における催奇形性を検討した公表文献であった(WG 報告書「5. 臨床使用に関
する報告」参照)
。なお、妊娠期間及び分娩時間の延長については、通常の診療内において
も発生することであり、本邦のガイドライン等も参考にして、対応することが可能であると
判断され、検討されていない。
当該 8 報のうち、7 報は先天異常のリスク推定指標(リスク比、オッズ比等)が記述され
ている研究報告であり、1 報はリスク推定指標が記述されていない研究報告であった。リス
ク推定指標が記述されている研究報告 7 報のうち、6 報は妊娠初期における Ca 拮抗薬(う
ち 2 報は本薬を含むことが記載)の使用による先天異常のリスク増加は認められなかった
という報告であった(WG 報告書文献番号 1~4、7、8)
。1 報は、妊娠初期の Ca 拮抗薬の使
用による先天異常全体(先天異常の種類は問わない)のリスク増加は認められなかった一方、
先天異常の種類別の検討では上部消化管奇形のリスク増加が認められたという報告であっ
た(WG 報告書文献番号 5)。リスク推定指標が記述されていない研究報告は、妊娠判明時
に Ca 拮抗薬の曝露があった 8 例の女性を追跡した結果、全症例健康な児を出産したという
報告であった(WG 報告書文献番号 6)
。
本薬の先発医薬品の製造販売承認取得者により、
WG 報告書と同様の検索条件 2を用いて、
WG 報告書の検索日以降に公表された本薬を含む Ca 拮抗薬と妊娠に関する文献が抽出され
2
WG 報告書 p.22 参照
2
2