よむ、つかう、まなぶ。
【資料3】医薬品等行政評価・監視委員会における海外調査(令和4年度・欧米の薬事制度に関する調査) (32 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32109.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第11回 3/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
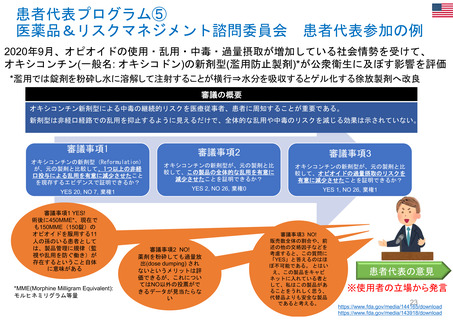
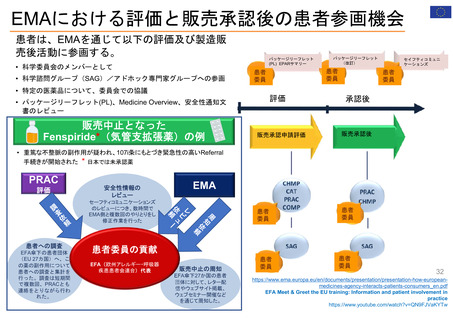
EMAにおける評価と販売承認後の患者参画機会
患者は、EMAを通じて以下の評価及び製造販
売後活動に参画する。
• 科学委員会のメンバーとして
• 科学諮問グループ(SAG)/アドホック専門家グループへの参画
パッケージリーフレット
(PL) EPARサマリー
評価
• パッケージリーフレット(PL)、Medicine Overview、安全性通知文
書のレビュー
販売中止となった
Fenspiride*(気管支拡張薬)の例
患者
委員
患者
委員
• 特定の医薬品について、委員会での協議
パッケージリーフレット
(改訂)
セイフティコミュニ
ケーションズ
患者
委員
承認後
販売承認申請評価
販売承認後
患者
委員
患者
委員
• 重篤な不整脈の副作用が疑われ、107i条にもとづき緊急性の高いReferral
手続きが開始された * 日本では未承認薬
PRAC
評価
安全性情報の
レビュー
EMA
セーフティコミュ二ケーションズ
のレビューにつき、数時間で
EMA側と複数回のやりとりをし
修正作業を行った
患者への調査
EFA傘下の患者団体
(EU 27カ国)へ、こ
の薬の副作用について
患者への調査と集計を
行った。調査は短期間
で複数回、PRACとも
連絡をとりながら行わ
れた。
患者委員の貢献
EFA(欧州アレルギー・呼吸器
疾患患者会連合)代表
販売中止の周知
EFA傘下27か国の患者
団体に対して、レター配
信やウェブサイト掲載、
ウェブセミナー開催など
を通じて周知した。
患者
委員
患者
委員
32
https://www.ema.europa.eu/en/documents/presentation/presentation-how-europeanmedicines-agency-interacts-patients-consumers_en.pdf
EFA Meet & Greet the EU training: Information and patient involvement in
practice
https://www.youtube.com/watch?v=QN9FJVaKYTw
患者は、EMAを通じて以下の評価及び製造販
売後活動に参画する。
• 科学委員会のメンバーとして
• 科学諮問グループ(SAG)/アドホック専門家グループへの参画
パッケージリーフレット
(PL) EPARサマリー
評価
• パッケージリーフレット(PL)、Medicine Overview、安全性通知文
書のレビュー
販売中止となった
Fenspiride*(気管支拡張薬)の例
患者
委員
患者
委員
• 特定の医薬品について、委員会での協議
パッケージリーフレット
(改訂)
セイフティコミュニ
ケーションズ
患者
委員
承認後
販売承認申請評価
販売承認後
患者
委員
患者
委員
• 重篤な不整脈の副作用が疑われ、107i条にもとづき緊急性の高いReferral
手続きが開始された * 日本では未承認薬
PRAC
評価
安全性情報の
レビュー
EMA
セーフティコミュ二ケーションズ
のレビューにつき、数時間で
EMA側と複数回のやりとりをし
修正作業を行った
患者への調査
EFA傘下の患者団体
(EU 27カ国)へ、こ
の薬の副作用について
患者への調査と集計を
行った。調査は短期間
で複数回、PRACとも
連絡をとりながら行わ
れた。
患者委員の貢献
EFA(欧州アレルギー・呼吸器
疾患患者会連合)代表
販売中止の周知
EFA傘下27か国の患者
団体に対して、レター配
信やウェブサイト掲載、
ウェブセミナー開催など
を通じて周知した。
患者
委員
患者
委員
32
https://www.ema.europa.eu/en/documents/presentation/presentation-how-europeanmedicines-agency-interacts-patients-consumers_en.pdf
EFA Meet & Greet the EU training: Information and patient involvement in
practice
https://www.youtube.com/watch?v=QN9FJVaKYTw