よむ、つかう、まなぶ。
【資料3】医薬品等行政評価・監視委員会における海外調査(令和4年度・欧米の薬事制度に関する調査) (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32109.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第11回 3/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
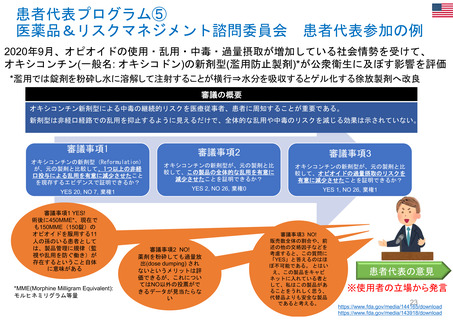
販売承認申請審査「科学的諮問グループ(SAG)」&
「アドホック専門家グループ」での患者参画
EMAの科学委員会は、
医薬品の科学的評価を強化するた
め、専門家や患者、医療従事者に
相談している。
これらの外部専門家は、
SAGやアドホック専門家グループ
に参画している。
協議事項
SAGおよびアドホック専門家グループ会議
ウイルス性疾患/HIV
アドホック専門家
グループ
腫瘍学
42名
2020年のSAG
会議に参加した
患者委員の数
神経学
抗感染症
対照薬選択
循環器疾患
• 患者は疾患領域における特定の医薬品に関連した実生活の視点や経験を
持っている。
• 患者が何を重要視しているか、許容できる安全性プロファイルはどんなもの
か、委員会がよりよく理解するのに役立つ。
EFA Meet & Greet the EU training:
Authorisation of Medicines in Europe and
Patient Involvement
https://www.youtube.com/watch?v=BeV_k_0L6Ws
33
https://www.ema.europa.eu/en/documents/other/involvement-patients-scientific-advisory-group-ad-hoc-expert-meetings-ema_en.pdf
「アドホック専門家グループ」での患者参画
EMAの科学委員会は、
医薬品の科学的評価を強化するた
め、専門家や患者、医療従事者に
相談している。
これらの外部専門家は、
SAGやアドホック専門家グループ
に参画している。
協議事項
SAGおよびアドホック専門家グループ会議
ウイルス性疾患/HIV
アドホック専門家
グループ
腫瘍学
42名
2020年のSAG
会議に参加した
患者委員の数
神経学
抗感染症
対照薬選択
循環器疾患
• 患者は疾患領域における特定の医薬品に関連した実生活の視点や経験を
持っている。
• 患者が何を重要視しているか、許容できる安全性プロファイルはどんなもの
か、委員会がよりよく理解するのに役立つ。
EFA Meet & Greet the EU training:
Authorisation of Medicines in Europe and
Patient Involvement
https://www.youtube.com/watch?v=BeV_k_0L6Ws
33
https://www.ema.europa.eu/en/documents/other/involvement-patients-scientific-advisory-group-ad-hoc-expert-meetings-ema_en.pdf