よむ、つかう、まなぶ。
【資料3】医薬品等行政評価・監視委員会における海外調査(令和4年度・欧米の薬事制度に関する調査) (42 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32109.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第11回 3/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
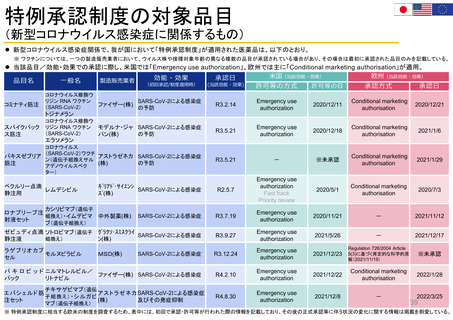
緊急使用許可(Emergency Use Authorization(EUA))
• 正式承認ではない
※ 通常の承認プロセスを経た医薬品の使用とは区別して、未承認薬の使用や適応外の使用を許可するもの。
※ 緊急使用許可を行った際の状況が終結するか、正式承認等が行われた場合には、当該緊急使用許可は失効する。
• 添付文書(ラベリング)が公開されていない
• 「安全性/有効性低下が確認された場合⇒許可取消し」が比較的速やかに行われる
(COVID-19治療薬・ワクチンで20近く許可されたうち、4製品が許可撤回)
EUAの条件注)(安全性情報の収集に関する内容)
※ 新型コロナウイルス感染症の治療薬でEUAが適用されたもの
• 製造販売業者に報告された、当該治療薬の使用に関係するすべての重篤な有害事象等についてFDAに報告
すること
• 当該治療薬の使用に関係する、すべての重篤な有害事象等について、MedWatch等を使用してFDAに報告す
ること
※ 品目によっては、個別の状況に応じて、この他に追加の臨床試験のデータの提出を求めている。
注) 緊急使用許可が効力を有する間又はその後妥当な期間、緊急使用許可を受けた製品の安全性や有効性に関する情報の収集・分析のための条
件を設定できるとされている。
https://www.fda.gov/media/97321/download
● ソトロビマブ[ゼビュディ]の例
https://www.fda.gov/drugs/drug-safety-and-availability/fda-updates-sotrovimab-emergency-use-authorization
• 2021/5/26 米国で緊急使用許可(EUA)
• 2022/2/23 FDAはソトロビマブの緊急使用許可を変更,ソトロビマブ耐性株による感染の割合が高い(50%以上)一部の地
域(州)での使用を制限
• 2022/4/5 オミクロンBA.2株の増加により、全米でEUA取消し
日本
⇒ 欧州及び日本では、警告及び使用上の注意で対応
EMAの緊急タスクフォース(ETF)が警告を通知
添付文書冒頭 枠囲み
• 本剤はオミクロン株(B1.1.529系統/BA.2系統,BA.4系統お
• 現在COVID-19に対して承認されているモノクローナル
よびBA.5系統)に対して有効性が減弱するおそれがあること
抗体がSARS-CoV-2の新興株に対して有効である可能
から,他の治療薬が使用できない場合に本剤の投与を検討
性は低い
42
欧州
すること.
• 正式承認ではない
※ 通常の承認プロセスを経た医薬品の使用とは区別して、未承認薬の使用や適応外の使用を許可するもの。
※ 緊急使用許可を行った際の状況が終結するか、正式承認等が行われた場合には、当該緊急使用許可は失効する。
• 添付文書(ラベリング)が公開されていない
• 「安全性/有効性低下が確認された場合⇒許可取消し」が比較的速やかに行われる
(COVID-19治療薬・ワクチンで20近く許可されたうち、4製品が許可撤回)
EUAの条件注)(安全性情報の収集に関する内容)
※ 新型コロナウイルス感染症の治療薬でEUAが適用されたもの
• 製造販売業者に報告された、当該治療薬の使用に関係するすべての重篤な有害事象等についてFDAに報告
すること
• 当該治療薬の使用に関係する、すべての重篤な有害事象等について、MedWatch等を使用してFDAに報告す
ること
※ 品目によっては、個別の状況に応じて、この他に追加の臨床試験のデータの提出を求めている。
注) 緊急使用許可が効力を有する間又はその後妥当な期間、緊急使用許可を受けた製品の安全性や有効性に関する情報の収集・分析のための条
件を設定できるとされている。
https://www.fda.gov/media/97321/download
● ソトロビマブ[ゼビュディ]の例
https://www.fda.gov/drugs/drug-safety-and-availability/fda-updates-sotrovimab-emergency-use-authorization
• 2021/5/26 米国で緊急使用許可(EUA)
• 2022/2/23 FDAはソトロビマブの緊急使用許可を変更,ソトロビマブ耐性株による感染の割合が高い(50%以上)一部の地
域(州)での使用を制限
• 2022/4/5 オミクロンBA.2株の増加により、全米でEUA取消し
日本
⇒ 欧州及び日本では、警告及び使用上の注意で対応
EMAの緊急タスクフォース(ETF)が警告を通知
添付文書冒頭 枠囲み
• 本剤はオミクロン株(B1.1.529系統/BA.2系統,BA.4系統お
• 現在COVID-19に対して承認されているモノクローナル
よびBA.5系統)に対して有効性が減弱するおそれがあること
抗体がSARS-CoV-2の新興株に対して有効である可能
から,他の治療薬が使用できない場合に本剤の投与を検討
性は低い
42
欧州
すること.