よむ、つかう、まなぶ。
【資料3】日米欧における医薬品の品質管理・製造管理に関する調査の状況(令和4年度欧米の薬事制度に関する調査・整理業務 調査結果) (35 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_30030.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第10回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
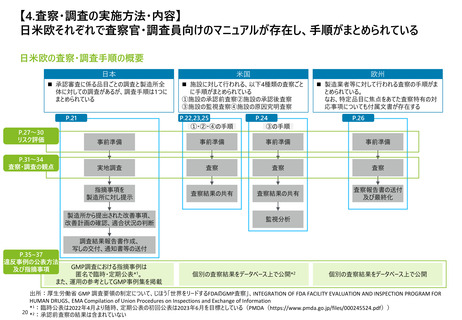
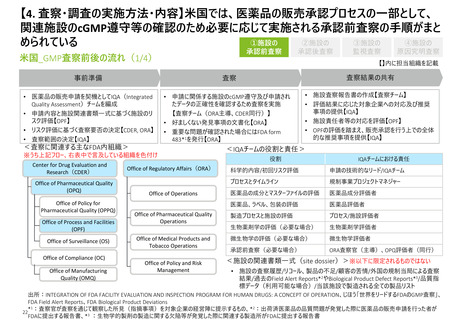
【4. 査察・調査の実施方法・内容】
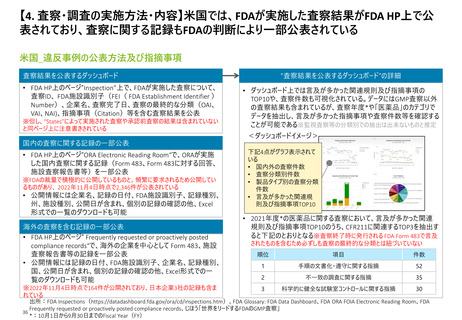
日本では、GMP調査における指摘事例等が公表されている
日本_違反事例の公表方法及び指摘事項
“指摘事例の公表”における、”臨時公表”
GMP事例集(2022年版)
• 厚生労働省が各都道府県衛生主管部向けに、GMPに関連する具
体的な運用をQ&A形式でとりまとめたGMP事例集(2022年版)
を公表
2022年11月末時点で以下4件の指摘事例が公表されている
発行年月日
事例
2022年4月
原料の受入時に供給元の確認を適切に行わなかった事例
指摘事例の公表
2022年5月
医薬品を製造する作業室で、薬理作用・毒性が不明な治験薬
を製造していた事例
• PMDAが、2022年4月より、各製造所における品質向上等を目的
としてPMDAが実施したGMP調査における指摘事例の公表を開始
2022年7月
試験検査が規格に適合しない場合の処理において他のロットへ
の影響評価が不十分であった事例
2022年9月
試験業務の委託に際し、外部試験検査機関の適正・能力の確
認が不十分であった事例
都道府県の指摘事項
“その他公表資料”における、”GMP事例研究会資料(2018年度)”
• 都道府県により異なるが、例えば大阪府では、他の製造業者にも
有益な指摘事項を「大阪府におけるGMP指摘事項ノート」として、
指摘のランク、指摘事項、指摘の背景、根拠省令等を公表
2016年にPMDAが実施したGMP調査における指摘事項が、件数と合
わせて公表されている
※現時点では指摘事項別に件数を確認できるものは本資料が最新
その他公表資料
• 医薬品等行政評価・監視委員会資料やGMP事例研究会資料に
おいて、最近の指摘事例や指摘件数等を公表
順位
項目
件数
1
文書管理・記録
41
2
製品の汚染防止
18
3
バリデーション
15
出所:厚生労働省 事例集(2022年度版)について、PMDA 医薬品品質管理部からのお知らせ(https://www.pmda.go.jp/files/000245524.pdf)、PMDA 品質確保に関す
る取り組み(https://www.pmda.go.jp/review-services/gmp-qms-gctp/gmp/0011.html)、大阪府健康医療部薬務課 大阪府におけるGMP指摘事項ノート、2020年度GMP事
例研究会 最近の指導事例と規制の動向(https://www.jpma.or.jp/information/quality/jirei/pdf/pdf_200909_01.pdf)、第6回 医薬品等行政評価・監視委員会資料
35 (https://www.mhlw.go.jp/content/10601000/000869784.pdf)、 2018年度GMP事例研究会 GMP省令改正案とPMDA査察の事例及び今後の方向性について
(https://www.jpma.or.jp/information/quality/jirei/pdf/pdf_180925_01.pdf)
日本では、GMP調査における指摘事例等が公表されている
日本_違反事例の公表方法及び指摘事項
“指摘事例の公表”における、”臨時公表”
GMP事例集(2022年版)
• 厚生労働省が各都道府県衛生主管部向けに、GMPに関連する具
体的な運用をQ&A形式でとりまとめたGMP事例集(2022年版)
を公表
2022年11月末時点で以下4件の指摘事例が公表されている
発行年月日
事例
2022年4月
原料の受入時に供給元の確認を適切に行わなかった事例
指摘事例の公表
2022年5月
医薬品を製造する作業室で、薬理作用・毒性が不明な治験薬
を製造していた事例
• PMDAが、2022年4月より、各製造所における品質向上等を目的
としてPMDAが実施したGMP調査における指摘事例の公表を開始
2022年7月
試験検査が規格に適合しない場合の処理において他のロットへ
の影響評価が不十分であった事例
2022年9月
試験業務の委託に際し、外部試験検査機関の適正・能力の確
認が不十分であった事例
都道府県の指摘事項
“その他公表資料”における、”GMP事例研究会資料(2018年度)”
• 都道府県により異なるが、例えば大阪府では、他の製造業者にも
有益な指摘事項を「大阪府におけるGMP指摘事項ノート」として、
指摘のランク、指摘事項、指摘の背景、根拠省令等を公表
2016年にPMDAが実施したGMP調査における指摘事項が、件数と合
わせて公表されている
※現時点では指摘事項別に件数を確認できるものは本資料が最新
その他公表資料
• 医薬品等行政評価・監視委員会資料やGMP事例研究会資料に
おいて、最近の指摘事例や指摘件数等を公表
順位
項目
件数
1
文書管理・記録
41
2
製品の汚染防止
18
3
バリデーション
15
出所:厚生労働省 事例集(2022年度版)について、PMDA 医薬品品質管理部からのお知らせ(https://www.pmda.go.jp/files/000245524.pdf)、PMDA 品質確保に関す
る取り組み(https://www.pmda.go.jp/review-services/gmp-qms-gctp/gmp/0011.html)、大阪府健康医療部薬務課 大阪府におけるGMP指摘事項ノート、2020年度GMP事
例研究会 最近の指導事例と規制の動向(https://www.jpma.or.jp/information/quality/jirei/pdf/pdf_200909_01.pdf)、第6回 医薬品等行政評価・監視委員会資料
35 (https://www.mhlw.go.jp/content/10601000/000869784.pdf)、 2018年度GMP事例研究会 GMP省令改正案とPMDA査察の事例及び今後の方向性について
(https://www.jpma.or.jp/information/quality/jirei/pdf/pdf_180925_01.pdf)