よむ、つかう、まなぶ。
【資料3】日米欧における医薬品の品質管理・製造管理に関する調査の状況(令和4年度欧米の薬事制度に関する調査・整理業務 調査結果) (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_30030.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第10回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
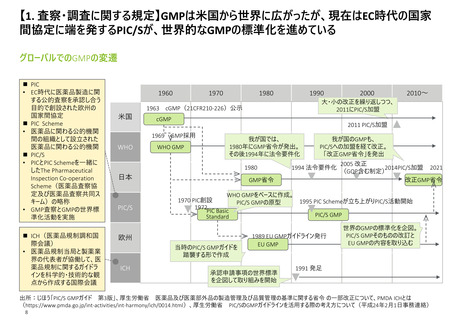
【1. 査察・調査に関する規定】海外拠点のGMP査察・調査の”位置づけ”に関しても、法令
や規制当局のHP上で言及されている
日米欧における海外拠点のGMP査察・調査の位置づけ
日本
◼ 薬機法
⇒ 第13条の3第1項 外国において本邦に輸出
される医薬品を製造しようとする者は厚生労
働大臣の認定を受けることができる
特に、海外拠点の ⇒ 第14条第2項第2号 申請(=品目ごとの
製造販売承認についての申請)に係る製
GMP査察・調査の
造所が第13条の3第1項の認定を受けていな
位置づけに関する
いとき、製造販売の承認は与えられない
言及概要
※前述の第14条第7項や第14条の2第2項は
海外拠点についても同様に適用される
米国
欧州
◼ FDA HP-Imported Drugs Raise Safety
◼ Directive 2001/83/EC(指令)
Concerns
⇒ Article 40 Paragraph 3 医薬品の製造許
⇒ 米国内で販売される医薬品はGMPを遵守し
可は第三国から加盟国に輸入される場合に
ている必要があり、国内であるか海外である
も求められる
かに関わらず、FDAに登録されている施設だ ⇒ Article 111 Paragraph 4 共同体と第三国
けが医薬品の製造を行うことができる
との間で締結された、いかなる取り決めにも
⇒ 新薬に関する海外製造所は通常FDAが査
影響を与えることなく、加盟国・委員会・機
察を行う
関は、第三国の製造業者に対して、
paragraph1に規定する査察を受けることを求
⇒ 医薬品承認後も、製造業者はFDA査察の
めることができる
対象となり、GMPを遵守しなければならない
※FDA HP上で海外製造所に対する査察につ
いてまとめられているページより抜粋
出所:医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律施行令、FDA HP
(https://www.fda.gov/drugs/information-consumers-and-patients-drugs/imported-drugs-raise-safetyconcerns#:~:text=If%20a%20foreign%20firm%20is%20listed%20as%20a,must%20continue%20to%20comply%20with%20good%20manufacturing%20practices)、
7 Directive 2001/83/EC
や規制当局のHP上で言及されている
日米欧における海外拠点のGMP査察・調査の位置づけ
日本
◼ 薬機法
⇒ 第13条の3第1項 外国において本邦に輸出
される医薬品を製造しようとする者は厚生労
働大臣の認定を受けることができる
特に、海外拠点の ⇒ 第14条第2項第2号 申請(=品目ごとの
製造販売承認についての申請)に係る製
GMP査察・調査の
造所が第13条の3第1項の認定を受けていな
位置づけに関する
いとき、製造販売の承認は与えられない
言及概要
※前述の第14条第7項や第14条の2第2項は
海外拠点についても同様に適用される
米国
欧州
◼ FDA HP-Imported Drugs Raise Safety
◼ Directive 2001/83/EC(指令)
Concerns
⇒ Article 40 Paragraph 3 医薬品の製造許
⇒ 米国内で販売される医薬品はGMPを遵守し
可は第三国から加盟国に輸入される場合に
ている必要があり、国内であるか海外である
も求められる
かに関わらず、FDAに登録されている施設だ ⇒ Article 111 Paragraph 4 共同体と第三国
けが医薬品の製造を行うことができる
との間で締結された、いかなる取り決めにも
⇒ 新薬に関する海外製造所は通常FDAが査
影響を与えることなく、加盟国・委員会・機
察を行う
関は、第三国の製造業者に対して、
paragraph1に規定する査察を受けることを求
⇒ 医薬品承認後も、製造業者はFDA査察の
めることができる
対象となり、GMPを遵守しなければならない
※FDA HP上で海外製造所に対する査察につ
いてまとめられているページより抜粋
出所:医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律施行令、FDA HP
(https://www.fda.gov/drugs/information-consumers-and-patients-drugs/imported-drugs-raise-safetyconcerns#:~:text=If%20a%20foreign%20firm%20is%20listed%20as%20a,must%20continue%20to%20comply%20with%20good%20manufacturing%20practices)、
7 Directive 2001/83/EC