よむ、つかう、まなぶ。
【参考資料6】成人と合わせて評価可能な小児(10歳又は12歳以上の小児)の臨床評価の留意点について(令和2年6月30日医薬品審査管理課事務連絡) (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00028.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(第1回 7/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
た科学的妥当性を検討の上、成人の試験に、小児を組み込むことを検討するこ
とが望まれる。
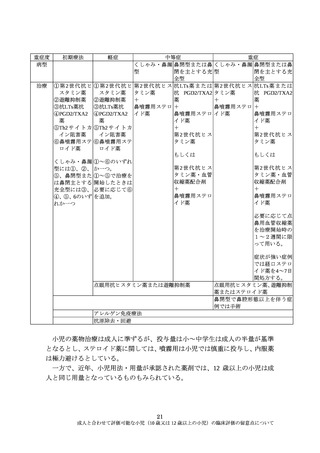
例えば腫瘍化の成因が明らかとなった、慢性骨髄性白血病やフィラデルフィ
ア染色体陽性急性リンパ性白血病ではチロシンキナーゼ阻害剤の小児用法・用
量は成人の用法・用量と同様となるように設定されている。
なお FDA は、病理学的、生物学的特徴が成人と Adolescent で類似している
と考えられる悪性腫瘍については、Adolescent を成人の臨床試験に含めるべき
とするガイダンス案 2)を公表している。
(5)対象となる年齢層について
本留意事項では、総論“2.対象年齢について”で記載した通り、成人と同一
の用法・用量の適用となる年齢を想定し、原則 10 歳や 12 歳以上としている。
一方で、造血器腫瘍は致死的で、幼少期から発症することから、低年齢にお
いても新しい薬剤が求められている。しかしながら、造血器腫瘍に対する薬物
治療の目的が増殖した腫瘍細胞の死滅であるものの、腫瘍化の成因が必ずしも
明らかになっていないものも多く、用法・用量も含めた有効性、安全性につい
ては慎重な検討が必要であることから、対象となる年齢層については 12 歳以
上とすることが妥当と考えられる。
ただし、慢性骨髄性白血病など発症機構が解明され、常時活性化したチロシ
ンキナーゼを阻害する薬剤のように、作用機序が明確で、開発初期の成人での
安全性データ及び類薬情報等から安全性についても成人と大きく異なることは
想定されない場合は、12 歳未満のより低年齢も含めることも可能である。な
お、より低年齢層も臨床試験に含める場合は、小児特有の安全性について幼若
動物を用いた試験などで検討することが必要である。
なお、FDA は抗悪性腫瘍剤の開発に関し、Adolescent も含めた2歳以上の小
児の成人臨床試験への登録について、早期臨床試験、後期臨床試験の開発段
階、2 歳以上 11 歳以下と 12 歳以上 17 歳以下の年齢に分けて、考え方を示して
いる 3)。
(6)臨床評価方法
本留意点の検討対象は、原則、成人の用法・用量が設定されたのち、成人と同
一、または成人の用法・用量の範囲内となる小児集団に対する臨床評価の考え方
である。
造血器悪性腫瘍には由来する細胞により様々な病型があり、その成因も不明
なものも多いが、薬物治療は薬剤により作用機序は異なるが腫瘍化した細胞を
結果として死滅させることであり、成人と小児で同じ病態であると想定され、
30
成人と合わせて評価可能な小児(10 歳又は 12 歳以上の小児)の臨床評価の留意点について
とが望まれる。
例えば腫瘍化の成因が明らかとなった、慢性骨髄性白血病やフィラデルフィ
ア染色体陽性急性リンパ性白血病ではチロシンキナーゼ阻害剤の小児用法・用
量は成人の用法・用量と同様となるように設定されている。
なお FDA は、病理学的、生物学的特徴が成人と Adolescent で類似している
と考えられる悪性腫瘍については、Adolescent を成人の臨床試験に含めるべき
とするガイダンス案 2)を公表している。
(5)対象となる年齢層について
本留意事項では、総論“2.対象年齢について”で記載した通り、成人と同一
の用法・用量の適用となる年齢を想定し、原則 10 歳や 12 歳以上としている。
一方で、造血器腫瘍は致死的で、幼少期から発症することから、低年齢にお
いても新しい薬剤が求められている。しかしながら、造血器腫瘍に対する薬物
治療の目的が増殖した腫瘍細胞の死滅であるものの、腫瘍化の成因が必ずしも
明らかになっていないものも多く、用法・用量も含めた有効性、安全性につい
ては慎重な検討が必要であることから、対象となる年齢層については 12 歳以
上とすることが妥当と考えられる。
ただし、慢性骨髄性白血病など発症機構が解明され、常時活性化したチロシ
ンキナーゼを阻害する薬剤のように、作用機序が明確で、開発初期の成人での
安全性データ及び類薬情報等から安全性についても成人と大きく異なることは
想定されない場合は、12 歳未満のより低年齢も含めることも可能である。な
お、より低年齢層も臨床試験に含める場合は、小児特有の安全性について幼若
動物を用いた試験などで検討することが必要である。
なお、FDA は抗悪性腫瘍剤の開発に関し、Adolescent も含めた2歳以上の小
児の成人臨床試験への登録について、早期臨床試験、後期臨床試験の開発段
階、2 歳以上 11 歳以下と 12 歳以上 17 歳以下の年齢に分けて、考え方を示して
いる 3)。
(6)臨床評価方法
本留意点の検討対象は、原則、成人の用法・用量が設定されたのち、成人と同
一、または成人の用法・用量の範囲内となる小児集団に対する臨床評価の考え方
である。
造血器悪性腫瘍には由来する細胞により様々な病型があり、その成因も不明
なものも多いが、薬物治療は薬剤により作用機序は異なるが腫瘍化した細胞を
結果として死滅させることであり、成人と小児で同じ病態であると想定され、
30
成人と合わせて評価可能な小児(10 歳又は 12 歳以上の小児)の臨床評価の留意点について