よむ、つかう、まなぶ。
【資料4】モルヌピラビル(ラゲブリオカプセル200mg )の安全性について(医薬・生活衛生局の説明資料) (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24538.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第7回 3/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
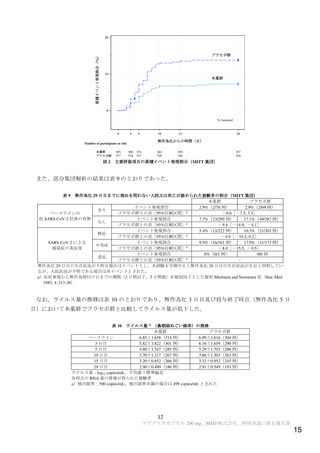
ベースラインのウイルスゲノムの塩基配列の情報が得られた被験者(277 例)において認められた
SARS-CoV-2 の株25)は、主に 21H(mu 株)
[本薬群 31.1%(41/132 例)、プラセボ群 38.6%(56/145 例)]、
21A(delta 株)[本薬群 25.0%(33/132 例)、プラセボ群 20.0%(29/145 例)]及び 20J(gamma 株)[本
薬群 20.5%(27/132 例)、プラセボ群 24.1%(35/145 例)]であった。
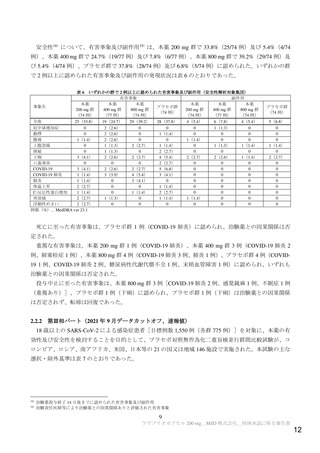
安全性26)について、有害事象及び副作用27)は、本薬群で 35.0%(135/386 例)及び 12.4%(48/386 例)、
プラセボ群で 39.6%(150/379 例)及び 11.1%(42/379 例)に認められた。いずれかの群で 2 例以上に認
められた有害事象及び副作用の発現状況は表 11 のとおりであった。
25)
Nextstrain Clade(https://nextstrain.org/)
治験薬投与終了 14 日後までに認められた有害事象及び副作用
27)
治験責任医師等により治験薬との因果関係ありと評価された有害事象
26)
13
ラゲブリオカプセル 200 mg_MSD 株式会社_特例承認に係る報告書
16
SARS-CoV-2 の株25)は、主に 21H(mu 株)
[本薬群 31.1%(41/132 例)、プラセボ群 38.6%(56/145 例)]、
21A(delta 株)[本薬群 25.0%(33/132 例)、プラセボ群 20.0%(29/145 例)]及び 20J(gamma 株)[本
薬群 20.5%(27/132 例)、プラセボ群 24.1%(35/145 例)]であった。
安全性26)について、有害事象及び副作用27)は、本薬群で 35.0%(135/386 例)及び 12.4%(48/386 例)、
プラセボ群で 39.6%(150/379 例)及び 11.1%(42/379 例)に認められた。いずれかの群で 2 例以上に認
められた有害事象及び副作用の発現状況は表 11 のとおりであった。
25)
Nextstrain Clade(https://nextstrain.org/)
治験薬投与終了 14 日後までに認められた有害事象及び副作用
27)
治験責任医師等により治験薬との因果関係ありと評価された有害事象
26)
13
ラゲブリオカプセル 200 mg_MSD 株式会社_特例承認に係る報告書
16