よむ、つかう、まなぶ。
【資料4】モルヌピラビル(ラゲブリオカプセル200mg )の安全性について(医薬・生活衛生局の説明資料) (35 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24538.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第7回 3/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
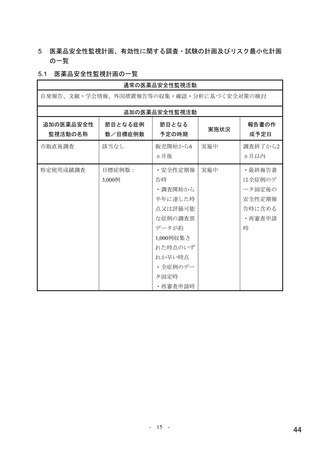
医薬品安全性監視活動の内容及びその選択理由:
【内容】
通常の医薬品安全性監視活動
追加の医薬品安全性監視活動として、特定使用成績調査を行う。
【選択理由】
通常の医薬品安全性監視活動に加え特定使用成績調査を通じて情報を収集するととも
に、骨髄抑制の発現状況を詳細に把握するため。
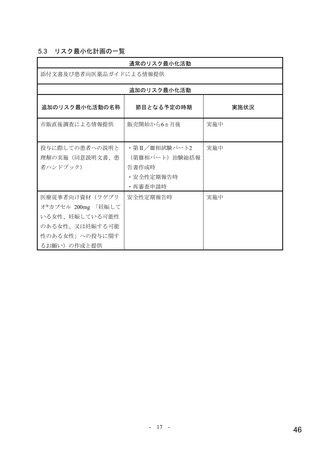
リスク最小化活動の内容及びその選択理由:
【内容】
通常のリスク最小化活動として、添付文書の「15. その他の注意」の項に動物実験
でみられた所見を記載し注意を喚起する。
【選択理由】
ヒトへの外挿性は明らかではないが、動物(イヌのみ)で骨髄抑制が認められている
ため、添付文書に記載する。
催奇形性
重要な潜在的リスクとした理由:
妊娠ラットの器官形成期に MOV を投与した実験において、ヒトに MOV 800 mg を12
時間間隔で投与したときの NHC の臨床曝露量の8倍に相当する用量で催奇形性及び
胚・胎児致死を含む発生毒性が、3倍以上に相当する用量で胎児の発育遅延が認めら
れた。一方で、妊娠ウサギの器官形成期に MOV を投与した実験においては、ヒトに
MOV 800 mg を12時間間隔で投与したときの NHC の臨床曝露量の18倍に相当する用
量で、催奇形性及び胚・胎児致死は認められなかった。
本剤の臨床試験では、妊娠している女性は組み入れ対象から除外されており、また、
妊娠可能な女性は NHC の全身曝露期間中は避妊することとしていたことから、妊娠
中の本剤の使用に関する臨床データはない。
以上より、催奇形性を重要な潜在的リスクとした。
医薬品安全性監視活動の内容及びその選択理由:
【内容】
通常の医薬品安全性監視活動
【選択理由】
妊婦に投与された場合、通常の医薬品安全性監視活動を通じて、質問票を用いて妊婦
における安全性と妊娠の転帰に関する情報を収集するため。
- 6 -
35
【内容】
通常の医薬品安全性監視活動
追加の医薬品安全性監視活動として、特定使用成績調査を行う。
【選択理由】
通常の医薬品安全性監視活動に加え特定使用成績調査を通じて情報を収集するととも
に、骨髄抑制の発現状況を詳細に把握するため。
リスク最小化活動の内容及びその選択理由:
【内容】
通常のリスク最小化活動として、添付文書の「15. その他の注意」の項に動物実験
でみられた所見を記載し注意を喚起する。
【選択理由】
ヒトへの外挿性は明らかではないが、動物(イヌのみ)で骨髄抑制が認められている
ため、添付文書に記載する。
催奇形性
重要な潜在的リスクとした理由:
妊娠ラットの器官形成期に MOV を投与した実験において、ヒトに MOV 800 mg を12
時間間隔で投与したときの NHC の臨床曝露量の8倍に相当する用量で催奇形性及び
胚・胎児致死を含む発生毒性が、3倍以上に相当する用量で胎児の発育遅延が認めら
れた。一方で、妊娠ウサギの器官形成期に MOV を投与した実験においては、ヒトに
MOV 800 mg を12時間間隔で投与したときの NHC の臨床曝露量の18倍に相当する用
量で、催奇形性及び胚・胎児致死は認められなかった。
本剤の臨床試験では、妊娠している女性は組み入れ対象から除外されており、また、
妊娠可能な女性は NHC の全身曝露期間中は避妊することとしていたことから、妊娠
中の本剤の使用に関する臨床データはない。
以上より、催奇形性を重要な潜在的リスクとした。
医薬品安全性監視活動の内容及びその選択理由:
【内容】
通常の医薬品安全性監視活動
【選択理由】
妊婦に投与された場合、通常の医薬品安全性監視活動を通じて、質問票を用いて妊婦
における安全性と妊娠の転帰に関する情報を収集するため。
- 6 -
35