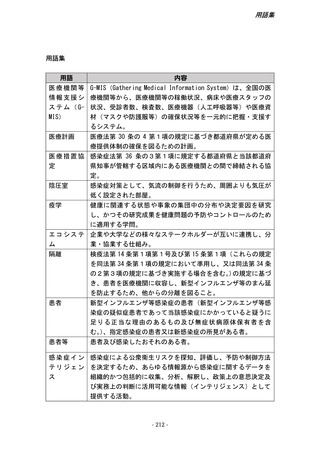
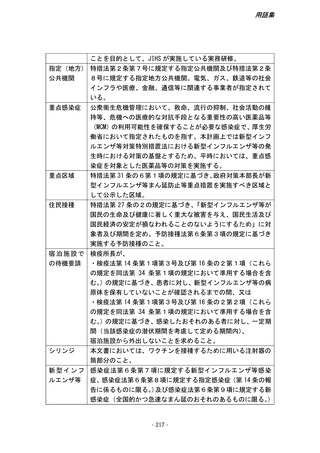
資料1参考資料1 新しい「新型インフルエンザ等対策政府行動計画」における各分野の取組(案) (156 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40139.html |
| 出典情報 | 厚生科学審議会 危機対応医薬品等に関する小委員会(第2回 5/13)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2-3-3. 臨床研究等の迅速な実施
国及び JIHS は、製薬関係企業、医療機関等とも連携し、準備期に構築し
た臨床研究等の実施に資する体制や人材を活用し、国内外で必要な臨床研究
等を迅速に開始するとともに、治療薬の研究開発や治療法の確立に資する科
学的知見の収集や共有を図る。(厚生労働省)
2-3-4. 研究開発企業との連携及び協力
① 国及び JIHS は、AMED を含む関係機関と連携し、研究試薬を含む治療薬・
治療法の研究開発企業の振興や、国産試薬の開発、国内製造の支援、創薬
ベンチャーによる開発を含め迅速な研究開発推進及び早期実用化のため
の必要な支援を実施する。(厚生労働省、健康・医療戦略推進事務局、経
済産業省)
② JIHS は、研究資金の確保を行い、また、戦略性を持った研究課題の設定
や研究費分配等の実施に資する情報提供等を国に対して行う。(厚生労働
省)
③ 国及び JIHS は、AMED と連携し、製薬関係企業等に対し、既存の治療薬
や化合物、開発シーズの新型インフルエンザ等に対する有効性等の検証を
速やかに行うよう要請するとともに、必要に応じて、研究開発の支援を行
う。(厚生労働省、健康・医療戦略推進事務局)
2-4. 緊急承認等の検討
国は、研究開発後の医薬品、医療機器等の早期普及のため、緊急承認 177や
特例承認 178の実施可能性の検討等を開始する。(厚生労働省)
2-5. 治療薬・治療法の活用に向けた体制の整備
2-5-1. 診療指針の確立
国及び JIHS は、大学等の研究機関や製薬関係企業等と連携し、既存の治
療薬の新型インフルエンザ等に対する有効性等の検証を速やかに行うとと
もに、流行初期における診療指針の策定を図る。その際に、必要に応じて、
準備期に構築した研究開発体制を活用し、治療薬の有効性等の精査を行う。
(厚生労働省)
177 医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和 35 年法律第 145 号)第
14 条の2の2
178 医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第 14 条の3
- 156 -