よむ、つかう、まなぶ。
03 資料1-1 帯状疱疹ワクチンファクトシート (43 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40826.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第26回 6/20)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
Grade3 の特定の有害事象(全身反応)**
全参加者
498/4,375
11.4 (10.5–12.4)
7,698
106/4,378
2.4 (2.0–2.9)
7,713
全研究期間
重篤な有害事象‡
689
9.0 (8.3–9.6)
686
8.9 (8.3–9.6)
免疫介在疾患
78
死亡
167
1.0 (0.8–1.3)
97
1.3 (1.0–1.5)
2.2 (1.9–2.5)
174
2.3 (1.9–2.6)
重篤な有害事象‡
87
1.1 (0.9–1.4)
97
1.3 (1.0–1.5)
重篤な有害事象(接種に関連)
1
0.0 (0.0–0.1)
3
0.0 (0.0–0.1)
死亡
8
0.1 (0.0–0.2)
7
0.1 (0.0–0.2)
接種 30 日以内
†
注射部位の発赤および腫脹における Grade は、直径 20mm 未満は 0、20mm 以上 50mm 未満を 1、50mm 以上 100mm 未満を 2、100mm 以上を 3 とした。体温は 37.5℃未
満を 0、37.5~38.0℃を 1 とした、39.0℃以上を 3 とした。(口腔内での測定を推奨)その他の症状は、0:なし、1:耐えられる、2:日常の活動に影響する、3:日常の活動
を妨げるとされた。
‡
重篤な有害事象は、死亡に至ったもの、生命を脅かすもの、入院を要するまたは入院の延長を要したもの、障害または能力喪失に至ったものとした。
70 歳以上の成人に対する乾燥組換え帯状疱疹ワクチン 146(海外、2016)
Cunningham らにより、18 か国の 70 歳以上の成人 13,900 例を対象とした組換え帯状疱疹ワクチン
(HZ/su;GSK Vaccine)の第Ⅲ相無作為化プラセボ対照比較試験が報告された。組入基準として、帯状疱
疹の罹患歴、水痘または帯状疱疹ワクチン、免疫抑制状態にないこととされた。参加者にはワクチン群又
はプラセボ群(0.9%食塩液)が 2 か月間隔で 2 回、0.5 mL を筋肉注射が行われた。
安全性評価のためのサブグループ 1,025 例(ワクチン群;512 例、プラセボ群;513 例)に対する安全
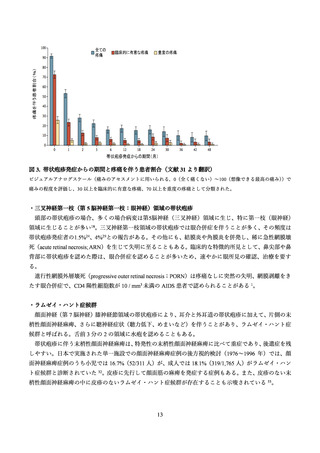
性評価について表 14 に記載した。接種 7 日以内に発生した特定の反応はワクチン群の 79.0%、プラセボ
群の 29.5%に認められた。接種部位の特定の反応(疼痛、発赤、腫脹)はワクチン群の 74.1%、プラセボ
群の 9.9%に認められ、ほとんどが軽度から中等度であった。グレード 3 の接種部位の反応はワクチン群
の 8.5%、プラセボ群の 0.2%に認められた。特定の全身反応(倦怠感、筋肉痛、頭痛、悪寒、発熱、消化
器障害)はワクチン群の 53%、プラセボ群の 25.1%に発現した(グレード 3 の反応はそれぞれ 6.0%と 2.0%
に報告された)
。最も多い接種部位反応は疼痛(ワクチン群の 68.7%)、全身反応は倦怠感(ワクチン群の
32.9%)であった。これらの反応は一過性であり、持続期間の中央値は接種部位の反応で 2~3 日、全身反
応で 1~2 日、グレード 3 の反応は 1~2 日であった。反応の頻度及び重症度は、2 回目の投与後に上昇は
見られなかった。80 歳以上の参加者では、70~79 歳の参加者と比較して特定の反応の頻度は低い傾向が
見られた。
本試験の平均追跡期間は 4 年間であり、重篤な有害事象や免疫介在疾患の発生頻度は両群で同等であ
った。全参加者において重篤な有害事象はワクチン群の 16.6%、プラセボ群の 17.5%に出現した。免疫介
在疾患は、ワクチン群の 1.3%、プラセボ群の 1.4%であった。治験責任者が本試験に関連するとした重篤
な有害事象は、ワクチン群で 12 例(0.2%)
、プラセボ群で 8 例(0.1%)であった。死亡はワクチン群で
426 例(6.1%)
、プラセボ群で 459 例(6.6%)に発生した。ワクチン群の死亡例のうち1例は、治験責任
者により本研究の介入に関連したものと考えられた。症例は 90 歳で血小板減少症の既往があり、初回接
種 75 日後に急性骨髄性白血病と診断され、2 回目の接種を受けることなく接種 97 日後に好中球減少性敗
血症で死亡した。
42
全参加者
498/4,375
11.4 (10.5–12.4)
7,698
106/4,378
2.4 (2.0–2.9)
7,713
全研究期間
重篤な有害事象‡
689
9.0 (8.3–9.6)
686
8.9 (8.3–9.6)
免疫介在疾患
78
死亡
167
1.0 (0.8–1.3)
97
1.3 (1.0–1.5)
2.2 (1.9–2.5)
174
2.3 (1.9–2.6)
重篤な有害事象‡
87
1.1 (0.9–1.4)
97
1.3 (1.0–1.5)
重篤な有害事象(接種に関連)
1
0.0 (0.0–0.1)
3
0.0 (0.0–0.1)
死亡
8
0.1 (0.0–0.2)
7
0.1 (0.0–0.2)
接種 30 日以内
†
注射部位の発赤および腫脹における Grade は、直径 20mm 未満は 0、20mm 以上 50mm 未満を 1、50mm 以上 100mm 未満を 2、100mm 以上を 3 とした。体温は 37.5℃未
満を 0、37.5~38.0℃を 1 とした、39.0℃以上を 3 とした。(口腔内での測定を推奨)その他の症状は、0:なし、1:耐えられる、2:日常の活動に影響する、3:日常の活動
を妨げるとされた。
‡
重篤な有害事象は、死亡に至ったもの、生命を脅かすもの、入院を要するまたは入院の延長を要したもの、障害または能力喪失に至ったものとした。
70 歳以上の成人に対する乾燥組換え帯状疱疹ワクチン 146(海外、2016)
Cunningham らにより、18 か国の 70 歳以上の成人 13,900 例を対象とした組換え帯状疱疹ワクチン
(HZ/su;GSK Vaccine)の第Ⅲ相無作為化プラセボ対照比較試験が報告された。組入基準として、帯状疱
疹の罹患歴、水痘または帯状疱疹ワクチン、免疫抑制状態にないこととされた。参加者にはワクチン群又
はプラセボ群(0.9%食塩液)が 2 か月間隔で 2 回、0.5 mL を筋肉注射が行われた。
安全性評価のためのサブグループ 1,025 例(ワクチン群;512 例、プラセボ群;513 例)に対する安全
性評価について表 14 に記載した。接種 7 日以内に発生した特定の反応はワクチン群の 79.0%、プラセボ
群の 29.5%に認められた。接種部位の特定の反応(疼痛、発赤、腫脹)はワクチン群の 74.1%、プラセボ
群の 9.9%に認められ、ほとんどが軽度から中等度であった。グレード 3 の接種部位の反応はワクチン群
の 8.5%、プラセボ群の 0.2%に認められた。特定の全身反応(倦怠感、筋肉痛、頭痛、悪寒、発熱、消化
器障害)はワクチン群の 53%、プラセボ群の 25.1%に発現した(グレード 3 の反応はそれぞれ 6.0%と 2.0%
に報告された)
。最も多い接種部位反応は疼痛(ワクチン群の 68.7%)、全身反応は倦怠感(ワクチン群の
32.9%)であった。これらの反応は一過性であり、持続期間の中央値は接種部位の反応で 2~3 日、全身反
応で 1~2 日、グレード 3 の反応は 1~2 日であった。反応の頻度及び重症度は、2 回目の投与後に上昇は
見られなかった。80 歳以上の参加者では、70~79 歳の参加者と比較して特定の反応の頻度は低い傾向が
見られた。
本試験の平均追跡期間は 4 年間であり、重篤な有害事象や免疫介在疾患の発生頻度は両群で同等であ
った。全参加者において重篤な有害事象はワクチン群の 16.6%、プラセボ群の 17.5%に出現した。免疫介
在疾患は、ワクチン群の 1.3%、プラセボ群の 1.4%であった。治験責任者が本試験に関連するとした重篤
な有害事象は、ワクチン群で 12 例(0.2%)
、プラセボ群で 8 例(0.1%)であった。死亡はワクチン群で
426 例(6.1%)
、プラセボ群で 459 例(6.6%)に発生した。ワクチン群の死亡例のうち1例は、治験責任
者により本研究の介入に関連したものと考えられた。症例は 90 歳で血小板減少症の既往があり、初回接
種 75 日後に急性骨髄性白血病と診断され、2 回目の接種を受けることなく接種 97 日後に好中球減少性敗
血症で死亡した。
42