よむ、つかう、まなぶ。
【参考資料5】抗微生物薬適正使用の手引き 第三版 別冊 (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_45318.html |
| 出典情報 | 厚生科学審議会 感染症部会 薬剤耐性(AMR)に関する小委員会 抗微生物薬適正使用(AMS)等に関する作業部会(第6回 11/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
抗微生物薬適正使用の手引き
第三版
別冊
(7) カンジダ
疫学の概要と臨床的特徴
侵襲性真菌感染症の約 70-90%はカンジダ感染症が占め、カンジダ血症や深在性カンジダ症あ
るいはいずれも認める侵襲性カンジダ症の死亡率は 40-60%と不良である 169,170。侵襲性カンジダ
症の主な侵入門戸は、皮膚や血管内カテーテル、消化管である 169。
カンジダの主要 5 菌種は Candida albicans、Candida glabrata、Candida tropicalis、Candida
parapsilosis、Candida krusei で、C. glabrata と C. krusei のアゾール耐性、C. parapsilosis のキャ
ンディン自然耐性やバイオフィルム形成による CRBSI が問題となっている 169,171,172。
国内で 2009 年に初めて耳道検体から検出された Candida auris は、その後世界各地で検出され
るようになり、アゾール耐性だけでなくポリエンへの耐性も問題となっている 173。
侵襲性カンジダ症のリスク因子は、広域抗菌薬使用、中心静脈カテーテル、中心静脈栄養、腹
部外科術後、APACHEII スコア高値、悪性腫瘍、好中球減少、化学療法、移植後、急性腎障害、
血液透析、糖尿病、長期入院や ICU 入室、未熟児・低出生体重等である 171,172。
微生物学的診断
スクリーニング検査としては血中 β-D-グルカン(感度 65-85%、特異度 75-85%)174,175、確定
診断には血液培養(感度~50%、特異度不明)169 がある。現在国内で使用可能な β-D-グルカン
の測定キットには複数のものがあるが、それぞれにカットオフ値が異なる点に留意する。陰性的
中率は高い一方、抗菌薬やアルブミン投与下で偽陽性になることに留意する 176。血液培養は陽
性化までに 2-3 日間必要で陽性率も低いことに留意する 169,171,172。
2023 年 2 月現在、国内では保険収載されていないが、全血 PCR(T2 Candida panel)が米国
等で用いられており、その感度と特異度はそれぞれ 91%と 94%である 169,171,172。カンジダスコ
アは侵襲性カンジダ症を予測するスクリーニング検査で、①中心静脈栄養(1 点)、②手術(1
点)
、③複数部位でのコロニゼーション(2 点)
、④敗血症(2 点)の 4 項目(計 6 点)中のうち 3
点以上で侵襲性カンジダ症発症を予測する(感度 81%、特異度 74%)177。
治療方針
治療は大きく抗真菌薬治療と感染巣コントロール(血管内カテーテルや人工物の抜去、外科的
ドレナージやデブリドマン)に分けられ、前者はさらに目的別で以下へ分類される 171。
① 予防的治療: 無症状で造血幹細胞や臓器移植後の持続する好中球減少症例に実施
② 経験的治療: 有症状で ICU に 96 時間以上滞在し、広域抗菌薬投与中で中心静脈栄養
もしくは消化管手術もしくは敗血症がある症例に実施
③ 先制治療:
経験的治療で挙げられた条件に加えて β-D-グルカン陽性あるいは
複数部位でのコロニゼーションが確認された症例に実施
④ 標的治療:
無菌部位から培養が検出された症例に対して実施
33
第三版
別冊
(7) カンジダ
疫学の概要と臨床的特徴
侵襲性真菌感染症の約 70-90%はカンジダ感染症が占め、カンジダ血症や深在性カンジダ症あ
るいはいずれも認める侵襲性カンジダ症の死亡率は 40-60%と不良である 169,170。侵襲性カンジダ
症の主な侵入門戸は、皮膚や血管内カテーテル、消化管である 169。
カンジダの主要 5 菌種は Candida albicans、Candida glabrata、Candida tropicalis、Candida
parapsilosis、Candida krusei で、C. glabrata と C. krusei のアゾール耐性、C. parapsilosis のキャ
ンディン自然耐性やバイオフィルム形成による CRBSI が問題となっている 169,171,172。
国内で 2009 年に初めて耳道検体から検出された Candida auris は、その後世界各地で検出され
るようになり、アゾール耐性だけでなくポリエンへの耐性も問題となっている 173。
侵襲性カンジダ症のリスク因子は、広域抗菌薬使用、中心静脈カテーテル、中心静脈栄養、腹
部外科術後、APACHEII スコア高値、悪性腫瘍、好中球減少、化学療法、移植後、急性腎障害、
血液透析、糖尿病、長期入院や ICU 入室、未熟児・低出生体重等である 171,172。
微生物学的診断
スクリーニング検査としては血中 β-D-グルカン(感度 65-85%、特異度 75-85%)174,175、確定
診断には血液培養(感度~50%、特異度不明)169 がある。現在国内で使用可能な β-D-グルカン
の測定キットには複数のものがあるが、それぞれにカットオフ値が異なる点に留意する。陰性的
中率は高い一方、抗菌薬やアルブミン投与下で偽陽性になることに留意する 176。血液培養は陽
性化までに 2-3 日間必要で陽性率も低いことに留意する 169,171,172。
2023 年 2 月現在、国内では保険収載されていないが、全血 PCR(T2 Candida panel)が米国
等で用いられており、その感度と特異度はそれぞれ 91%と 94%である 169,171,172。カンジダスコ
アは侵襲性カンジダ症を予測するスクリーニング検査で、①中心静脈栄養(1 点)、②手術(1
点)
、③複数部位でのコロニゼーション(2 点)
、④敗血症(2 点)の 4 項目(計 6 点)中のうち 3
点以上で侵襲性カンジダ症発症を予測する(感度 81%、特異度 74%)177。
治療方針
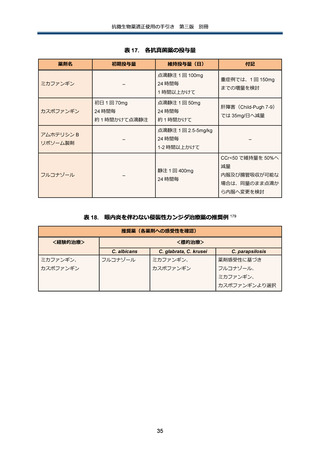
治療は大きく抗真菌薬治療と感染巣コントロール(血管内カテーテルや人工物の抜去、外科的
ドレナージやデブリドマン)に分けられ、前者はさらに目的別で以下へ分類される 171。
① 予防的治療: 無症状で造血幹細胞や臓器移植後の持続する好中球減少症例に実施
② 経験的治療: 有症状で ICU に 96 時間以上滞在し、広域抗菌薬投与中で中心静脈栄養
もしくは消化管手術もしくは敗血症がある症例に実施
③ 先制治療:
経験的治療で挙げられた条件に加えて β-D-グルカン陽性あるいは
複数部位でのコロニゼーションが確認された症例に実施
④ 標的治療:
無菌部位から培養が検出された症例に対して実施
33