よむ、つかう、まなぶ。
【参考資料6】抗微生物薬適正使用の手引き 第三版 補遺 (25 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_45318.html |
| 出典情報 | 厚生科学審議会 感染症部会 薬剤耐性(AMR)に関する小委員会 抗微生物薬適正使用(AMS)等に関する作業部会(第6回 11/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(別冊参考箇所:p.25-26)
1. 入院患者の感染症で問題となる微生物>(5) その他のグラム陰性桿菌(緑膿菌以外のブドウ糖
非発酵菌)>(i) アシネトバクター属(主に Acinetobacter baumannii)
<アシネトバクター属における薬剤耐性の問題とその機序>
A. baumannii は内因性の薬剤耐性機構を豊富に有し、同時に外因性の薬剤耐性機構を獲得する
能力も備える。そのため、世界的に薬剤耐性化が問題となっている 104。最も大きな問題はカル
バペネム耐性であり、世界保健機関は、新規抗菌薬の研究開発が急がれる薬剤耐性菌の中で、カ
ルバペネム耐性 A. baumannii(CRAB)を最も緊急性の高い”critical“に分類している 105。2019 年
の全世界における薬剤耐性菌関連死亡を推定した報告では、A. baumannii は関連死亡の多い上位
6 菌種に含まれ、関連死亡は約 42 万人と推定された 106。
特に、東南アジア・南アジア諸国、南米諸国、ロシアを含む東欧諸国における CRAB の広がり
が問題となっている 106-108。また、欧州・北米でも CRAB が問題で、臨床分離株におけるメロペ
ネム感性率は、1997〜2000 年に欧州で 55.7%、北米で 88.8%であったが、2013〜2016 年では
それぞれ 13.7%、54.9%まで悪化したと報告された 107。
カルバペネム耐性には主に β-ラクタマーゼ、特に Oxacillinase(OXA)が関わり、OXA-23、
40/24、51、58 が主要なものと知られる 109-111。このうち、OXA-51 は通常染色体性に保有しプロ
モーター活性を有す挿入配列を獲得することにより発現する。一方、OXA-23、40/24、5840 はプ
ラスミド性に伝播・獲得する。メタロ-β-ラクタマーゼ(MBL)も関与する 112。MBL は種を超え
て伝播可能で 113、カルバペネム耐性が広がる機序の一つとなっている。ペニシリン結合蛋白
(PBP)2 の変異、細胞外膜のポーリンの減少や排出ポンプが関与することもある 112。
一方、日本では CRAB ならびに多剤耐性アシネトバクター(MDRA)の頻度は諸外国と比べて
低い状態が維持されている 114。JANIS(Japan Nosocomial Infections Surveillance:院内感染対
策サーベイランス事業)による 2021 年データでは、検出された Acinetobacter 属のメロペネム非
感受性率は 1.7%、MDRA の分離された医療機関の割合は 0.8%であった 115。日本の CRAB が有
すカルバペネマーゼは、獲得型では OXA-23、IMP、OXA-51 の順に多かったと報告されている 115。
<微生物検査に関する留意事項>
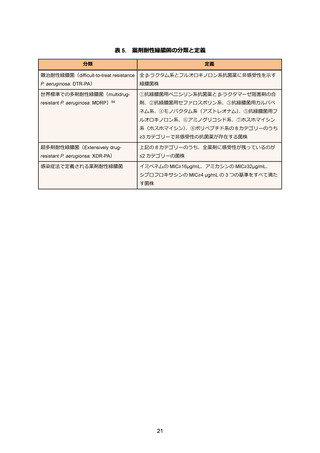
発生届上の「薬剤耐性」の定義は、広域 β-ラクタム系抗菌薬(基準上はカルバペネム系)・ア
ミノ配糖体(アミノグリコシド)・フルオロキノロン系抗菌薬の 3 系統の薬剤に対して耐性を示
す(イミペネムの MIC 値≥16µg/mL、アミカシンの MIC 値≥32 µg/mL、シプロフロキサシンの
MIC 値≥4 µg/mL)ことである 116。これらの耐性と判定される MIC のカットオフ値は、CLSI の定
める判定基準に照らし合わせると、2011 年まで利用されていた基準が採用されており、現行の
基準(CLSI. M100-S32)87 とは異なっている点には注意を要する 117。また、JANIS の MDRA の
基準では、イミペネム又はメロペネムの MIC 値≥16 µg/mL、アミカシンの MIC 値≥32 µg/mL、シ
プロフロキサシンの MIC 値≥4µg/mL 又はレボフロキサシンの MIC 値≥8µg/mL と規定されている
(厚生労働省院内感染対策サーベイランス:薬剤耐性菌判定基準[ver3.2]
)118。
25
1. 入院患者の感染症で問題となる微生物>(5) その他のグラム陰性桿菌(緑膿菌以外のブドウ糖
非発酵菌)>(i) アシネトバクター属(主に Acinetobacter baumannii)
<アシネトバクター属における薬剤耐性の問題とその機序>
A. baumannii は内因性の薬剤耐性機構を豊富に有し、同時に外因性の薬剤耐性機構を獲得する
能力も備える。そのため、世界的に薬剤耐性化が問題となっている 104。最も大きな問題はカル
バペネム耐性であり、世界保健機関は、新規抗菌薬の研究開発が急がれる薬剤耐性菌の中で、カ
ルバペネム耐性 A. baumannii(CRAB)を最も緊急性の高い”critical“に分類している 105。2019 年
の全世界における薬剤耐性菌関連死亡を推定した報告では、A. baumannii は関連死亡の多い上位
6 菌種に含まれ、関連死亡は約 42 万人と推定された 106。
特に、東南アジア・南アジア諸国、南米諸国、ロシアを含む東欧諸国における CRAB の広がり
が問題となっている 106-108。また、欧州・北米でも CRAB が問題で、臨床分離株におけるメロペ
ネム感性率は、1997〜2000 年に欧州で 55.7%、北米で 88.8%であったが、2013〜2016 年では
それぞれ 13.7%、54.9%まで悪化したと報告された 107。
カルバペネム耐性には主に β-ラクタマーゼ、特に Oxacillinase(OXA)が関わり、OXA-23、
40/24、51、58 が主要なものと知られる 109-111。このうち、OXA-51 は通常染色体性に保有しプロ
モーター活性を有す挿入配列を獲得することにより発現する。一方、OXA-23、40/24、5840 はプ
ラスミド性に伝播・獲得する。メタロ-β-ラクタマーゼ(MBL)も関与する 112。MBL は種を超え
て伝播可能で 113、カルバペネム耐性が広がる機序の一つとなっている。ペニシリン結合蛋白
(PBP)2 の変異、細胞外膜のポーリンの減少や排出ポンプが関与することもある 112。
一方、日本では CRAB ならびに多剤耐性アシネトバクター(MDRA)の頻度は諸外国と比べて
低い状態が維持されている 114。JANIS(Japan Nosocomial Infections Surveillance:院内感染対
策サーベイランス事業)による 2021 年データでは、検出された Acinetobacter 属のメロペネム非
感受性率は 1.7%、MDRA の分離された医療機関の割合は 0.8%であった 115。日本の CRAB が有
すカルバペネマーゼは、獲得型では OXA-23、IMP、OXA-51 の順に多かったと報告されている 115。
<微生物検査に関する留意事項>
発生届上の「薬剤耐性」の定義は、広域 β-ラクタム系抗菌薬(基準上はカルバペネム系)・ア
ミノ配糖体(アミノグリコシド)・フルオロキノロン系抗菌薬の 3 系統の薬剤に対して耐性を示
す(イミペネムの MIC 値≥16µg/mL、アミカシンの MIC 値≥32 µg/mL、シプロフロキサシンの
MIC 値≥4 µg/mL)ことである 116。これらの耐性と判定される MIC のカットオフ値は、CLSI の定
める判定基準に照らし合わせると、2011 年まで利用されていた基準が採用されており、現行の
基準(CLSI. M100-S32)87 とは異なっている点には注意を要する 117。また、JANIS の MDRA の
基準では、イミペネム又はメロペネムの MIC 値≥16 µg/mL、アミカシンの MIC 値≥32 µg/mL、シ
プロフロキサシンの MIC 値≥4µg/mL 又はレボフロキサシンの MIC 値≥8µg/mL と規定されている
(厚生労働省院内感染対策サーベイランス:薬剤耐性菌判定基準[ver3.2]
)118。
25